Калий гидроксид (KOH) - это щелочное вещество, широко используемое в промышленности и лабораториях. Одной из важных характеристик этого соединения является его способность образовывать окисные степени металлов.
Степень окисления металла - это числовое значение, которое показывает количество электронов, переданных металлом в процессе химической реакции. Калий гидроксид может повышать или понижать степень окисления металлов в зависимости от условий реакции.
Когда металл взаимодействует с калием гидроксидом, он может отдать или принять электроны. Если металл отдаёт электроны, его степень окисления повышается. Например, железо (Fe) может отдать два электрона и иметь степень окисления +2, а медь (Cu) может отдать один электрон и иметь степень окисления +1.
С другой стороны, если металл принимает электроны, его степень окисления понижается. Например, марганец (Mn) может принять два электрона и иметь степень окисления -2, а перекись марганца (MnO2) может принять четыре электрона и иметь степень окисления +4.
Степени окисления в химии
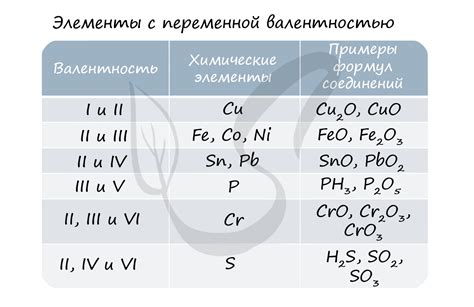
Степень окисления — это числовое значение, которое указывает на число электронов, переданных атомом при окислении или восстановлении в химической реакции. Она позволяет анализировать процессы окисления-восстановления и определять изменение структуры и свойств вещества.
Степени окисления металлов в соединениях могут быть различными и зависят от их электрохимической активности. Некоторые металлы, такие как натрий и калий, имеют одну степень окисления и образуют ион с положительным зарядом. Например, Na+ и K+, где степень окисления равна +1.
Однако большинство металлов может образовывать соединения с разными степенями окисления. Например, железо может иметь степени окисления +2 и +3, образуя соединения Fe2+ и Fe3+. Эти степени окисления определяются электрохимическими свойствами металла и условиями окружающей среды.
Степени окисления металлов играют важную роль в химических реакциях, так как они описывают изменение состояния металла и его способность образовывать соединения. Важно учитывать степени окисления в процессе балансировки химических уравнений и определения реакционных условий.
Список степеней окисления металлов может быть очень длинным, поэтому удобно использовать таблицу степеней окисления, чтобы быстро определить степень окисления вещества. Такая таблица позволяет химику более точно анализировать реакции и предсказывать их химическую активность.
Окисление металлов в растворе KOH

Раствор KOH (калиевый гидроксид) является сильным основанием и часто применяется для окисления различных металлов. Окисление металлов в растворе KOH происходит за счет образования гидроксидных и оксидных соединений.
Металлы, такие как литий (Li), натрий (Na), калий (K) и рубидий (Rb), способны реагировать с раствором KOH, образуя гидроксид металла. Например, литий с раствором KOH образует гидроксид лития (LiOH). Данный процесс сопровождается выделением водорода и образованием гидроксид-иона (OH-).
Также с помощью раствора KOH можно окислить металлы, такие как алюминий (Al) и магний (Mg). При окислении алюминия раствором KOH образуется гидроксид алюминия (Al(OH)3) и алюминат калия (KAl(OH)4). Окисление магния раствором KOH приводит к образованию гидроксида магния (Mg(OH)2) и магнат калия (K2Mg(OH)4).
Окисление металлов в растворе KOH является важным процессом, используемым в различных технологиях, таких как производство щелочных батарей или водорода.
Примеры степеней окисления металлов

Металлы могут образовывать различные степени окисления в химических соединениях. Некоторые примеры степеней окисления металлов:
- Железо (Fe) может образовать соединения с разными степенями окисления. В частности, в кислородсодержащих соединениях железо может иметь степени окисления +2 (Fe2+) или +3 (Fe3+). Например, в соединении Fe2O3 степень окисления железа равна +3.
- Мышьяк (As) может образовывать соединения с различными степенями окисления. Например, мышьяк может иметь степень окисления +3 (As3+) в соединении AsCl3 или степень окисления +5 (As5+) в соединении As2O5.
- Марганец (Mn) также может образовывать соединения с разными степенями окисления. В соединении KMnO4 степень окисления марганца равна +7 (Mn7+), а в Cr2O7^2− степень окисления марганца равна +6 (Mn6+).
Это лишь несколько примеров степеней окисления металлов в различных соединениях. Для каждого металла можно найти еще больше примеров, что демонстрирует многообразие химических свойств металлов и их способность формировать соединения с разными степенями окисления.
Значение степеней окисления металлов KOH

Степень окисления металлов в реакции с щелочью KOH играет важную роль в определении их химической активности и способности взаимодействовать с другими веществами. Калийная гидроксидная щелочь, KOH, является сильным основанием и может окислять некоторые металлы.
Степени окисления металлов KOH определяются на основе количества электронов, которые металл может потерять или передать в реакции с щелочью. Это важно для понимания структуры и свойств металлов, а также для прогнозирования их химической активности при взаимодействии с различными соединениями.
Степень окисления металлов в щелочной среде может быть определена с помощью электрохимического метода или путем анализа реакций, которые металлы образуют с KOH. Некоторые металлы, такие как натрий (Na) и калий (K), имеют степень окисления +1 в соединениях с KOH.
Однако, не все металлы имеют одну и ту же степень окисления в реакции с KOH. Например, некоторые металлы, такие как железо (Fe) и медь (Cu), могут иметь различные степени окисления в зависимости от условий реакции и окружающей среды. Это может быть связано с различием в электронной структуре и химических свойствах этих металлов.
Значение степеней окисления металлов KOH имеет практическое значение для различных процессов и приложений, таких как производство батарей, электролиз металлов, а также в процессах очистки воды и обработки сточных вод. Понимание и контроль степеней окисления металлов KOH помогает оптимизировать эти процессы и повысить их эффективность.
Вопрос-ответ

Какие могут быть степени окисления металлов в соединении KOH?
В соединении KOH металл может иметь степень окисления +1, так как гидроксид калия (KOH) является нейтральным соединением.
Как определить степень окисления металла в соединении KOH?
Степень окисления металла в соединении KOH можно определить, зная, что гидроксид калия (KOH) является нейтральным соединением и кислород всегда имеет степень окисления -2. Следовательно, степень окисления металла можно рассчитать по формуле: степень окисления металла = общий заряд соединения - заряд кислорода.
Какие ионы присутствуют в соединении KOH?
В соединении KOH присутствуют ионы калия (K+) и гидроксидные ионы (OH-).
В чем состоит роль металла в соединении KOH?
Металл в соединении KOH выполняет роль катиона и обладает положительным зарядом. Он участвует в образовании электролитического раствора и обеспечивает химическую активность соединения.
Может ли металл иметь степень окисления, отличную от +1, в соединении KOH?
В соединении KOH металл всегда имеет степень окисления +1, так как гидроксид калия (KOH) является нейтральным соединением, а кислород всегда имеет степень окисления -2. Поэтому, чтобы соединение было нейтральным, металл должен иметь степень окисления +1.
