Окисление и восстановление – важные процессы в химии, которые играют важную роль во многих химических реакциях. Металлы, благодаря своим особенностям, могут иметь различную степень окисления. Степень окисления металлов может быть как положительной, так и отрицательной, и она определяет их химическую активность и способность образовывать соединения.
Положительная степень окисления металлов указывает на то, что металл потерял электроны и образовал положительный ион. В результате положительной окислительной реакции металл становится окислителем и способен передавать электроны другим веществам. Металлы с положительной степенью окисления обычно образуют соли и восстанавливаются в реакциях с веществами, имеющими отрицательную степень окисления.
Отрицательная степень окисления металлов, напротив, характеризует их способность принимать электроны от других веществ. Металлы с отрицательной степенью окисления в реакциях восстановления выступают в качестве восстановителей и передают электроны другим веществам. Отрицательная окислительная реакция обусловлена способностью металла принимать электроны и образовывать отрицательные ионы.
Ясно, что степень окисления металлов может быть как положительной, так и отрицательной, в зависимости от их способности отдавать или принимать электроны в химических реакциях. Особенности степени окисления металлов имеют важное значение для понимания и изучения их химических свойств и влияния на окружающую среду.
Окисление металлов: положительная ли степень?

Степень окисления металлов может быть как положительной, так и отрицательной, в зависимости от конкретного металла и условий окисления.
Металлы, обладающие положительной степенью окисления, способны отдавать электроны и образовывать положительно заряженные ионы. Примерами таких металлов являются натрий, калий, магний и другие щелочные и щелочноземельные металлы.
С другой стороны, некоторые металлы имеют отрицательную степень окисления и способны принимать электроны, образуя отрицательно заряженные ионы. Примерами таких металлов являются хлор, фтор, кислород и другие неметаллы.
Однако следует отметить, что степень окисления металлов может изменяться в различных химических соединениях. Например, железо может образовывать соединения, в которых его степень окисления может быть и положительной, и отрицательной.
Для определения степени окисления металла в химическом соединении необходимо знание правил определения степени окисления и общую представленность о свойствах металлов и их соединениях.
Понимание степеней окисления металлов является важным аспектом в области химии и позволяет более глубоко изучать и понимать химические реакции и свойства веществ.
Определение степени окисления металлов
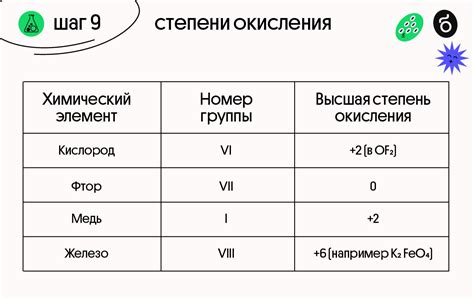
Степень окисления металлов – это числовое значение, которое указывает на количество электронов, переданных металлом в реакции окисления-восстановления. Степень окисления может быть как положительной, так и отрицательной величиной в зависимости от того, насколько металл отдает или принимает электроны.
Для определения степени окисления металлов необходимо знать валентность металла, то есть количество электронов, которое металл может потерять или принять при взаимодействии. Например, железо имеет валентность 2+ или 3+, что означает, что оно может отдать 2 или 3 электрона соответственно.
Определение степени окисления металлов может быть осуществлено с помощью различных методов анализа, таких как химический анализ, спектроскопия и электрохимические методы. Одним из распространенных методов является использование окислительно-восстановительных реакций, в которых происходят переход электронов от одного вещества к другому.
Важно отметить, что степень окисления металлов может меняться в зависимости от условий реакции и окружающей среды. Например, железо может иметь степень окисления 2+ в кислой среде и 3+ в щелочной среде. Поэтому при определении степени окисления необходимо учитывать все факторы, влияющие на реакцию.
Зависимость степени окисления от химической реакции

Степень окисления металлов в химической реакции зависит от их электрохимического потенциала и реактивности. Как правило, металлы имеют положительные степени окисления, так как они обычно отдают электроны и образуют положительные ионы.
Окисление металлов происходит во время реакции с кислотами, окислителями или другими веществами, которые могут принять электроны. В реакции металлы обычно образуют положительные ионы, что позволяет им вступать в дальнейшие химические реакции.
Степень окисления металлов может быть определена с использованием таблиц электрохимического потенциала. В таких таблицах каждый металл имеет свой потенциал окисления и восстановления, и степень окисления может быть вычислена по разнице между этими потенциалами.
Также степень окисления металла может быть определена по его нормальному потенциалу окисления. Нормальный потенциал окисления металлов измеряется в вольтах и показывает, насколько легко металл может отдать электроны в химической реакции.
Роль положительной и отрицательной степени окисления

Степень окисления металлов может быть как положительной, так и отрицательной, и каждая из них выполняет определенную роль в химических реакциях и процессах.
Положительная степень окисления металлов указывает на то, что металлу были переданы электроны другим веществом. Положительное значение степени окисления обусловлено тем, что металл имеет тенденцию отдавать электроны и образовывать положительные ионы. Это свойство металлов позволяет им служить хорошими окислителями, т.е. принимать участие в окислительно-восстановительных реакциях, передавая электроны другим веществам.
Отрицательная степень окисления металлов указывает на то, что металлу были переданы электроны от других веществ. Отрицательные значения степени окисления металлов обусловлены тем, что металл имеет тенденцию принимать электроны и образовывать отрицательные ионы. Это свойство металлов позволяет им служить восстановителями, т.е. принимать участие в окислительно-восстановительных реакциях, передавая электроны другим веществам.
Важно отметить, что положительная и отрицательная степень окисления металлов связаны с их электронной конфигурацией и возможностью образования ионов. Значение степени окисления металла может варьироваться в зависимости от среды, в которой происходит реакция, и от состава реагентов. Это позволяет металлам выполнять различные функции в различных химических реакциях и реакционных средах, и они являются важными компонентами многих химических процессов и промышленных производств.
Таким образом, положительная и отрицательная степень окисления металлов играют важную роль в химических реакциях, позволяя металлам участвовать в окислительно-восстановительных реакциях, передавая электроны другим веществам и определяя химические свойства и функции этих металлов.
Примеры металлов с положительной и отрицательной степенью окисления

Степень окисления металлов может быть как положительной, так и отрицательной, в зависимости от химических свойств элемента и окружающей среды. В данной статье рассмотрим примеры металлов с положительной и отрицательной степенью окисления.
Примеры металлов с положительной степенью окисления включают такие элементы, как железо (Fe), медь (Cu), цинк (Zn) и алюминий (Al). Вещества, содержащие эти металлы, имеют способность окисляться, то есть переходить в состояние с более высокой степенью окисления.
Например, железо может иметь степень окисления +2 и +3. В соединениях с более высокой степенью окисления, железо часто проявляет свойства катализаторов и участвует в реакциях окисления-восстановления. Медь также может иметь степень окисления +1 и +2. Многие реакции, связанные с окислением меди, используются в химическом анализе и промышленности.
Примеры металлов с отрицательной степенью окисления включают такие элементы, как водород (H), сурьма (Sb), золото (Au) и серебро (Ag). Вещества, содержащие эти металлы, могут выступать в качестве восстановителей, то есть переходить в состояние с более низкой степенью окисления.
Например, золото обычно имеет степень окисления 0, что означает, что оно находится в своем самом неприрастившем состоянии. Золото используется в ювелирном и промышленном производстве, благодаря своим уникальным свойствам и высокой стойкости к окислению. Серебро и сурьма также могут иметь отрицательную степень окисления в некоторых соединениях.
В заключение, степень окисления металлов может быть как положительной, так и отрицательной, и зависит от конкретного элемента и условий окружающей среды. Знание степени окисления металлов позволяет более точно понимать и предсказывать их химические реакции и свойства.
Вопрос-ответ

Какая степень окисления свойственна большинству металлов?
Большинство металлов имеют положительную степень окисления.
Может ли быть отрицательная степень окисления у металлов?
Нет, отрицательная степень окисления у металлов не возможна.

