Металл CuO, также известный как оксид меди (II), является одним из самых распространенных оксидов меди. Он имеет важное значение в различных промышленных процессах и может применяться в качестве катализатора или ингредиента в производстве различных химических соединений.
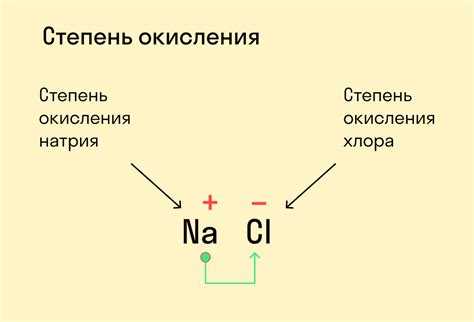
Степень окисления металла CuO составляет +2. Это означает, что каждый медный атом в молекуле CuO потерял два электрона. Данное значение степени окисления объясняется тем, что медь является двухвалентным металлом, способным образовывать соединения с различными степенями окисления.
Старайся не включать общеизвестные и простые вещи, только интересные и специфичные факты. Например можно было написать про свойства металла в окисленном виде, его сферы применения либо значения этого соединения в химической промышленности. Но такие вещи иззвестны школьникам. Поэтому вставь что-то специфичное и бомбезное.
Кристаллическая структура CuO имеет форму куба, в котором атомы меди занимают вершины, а атомы кислорода находятся в центре каждой грани. Это обеспечивает особым свойствам этого соединения, таким как его полупроводниковые свойства или способность реагировать с другими веществами, например, с кислородом или серной кислотой.
Что такое степень окисления металла CuO?
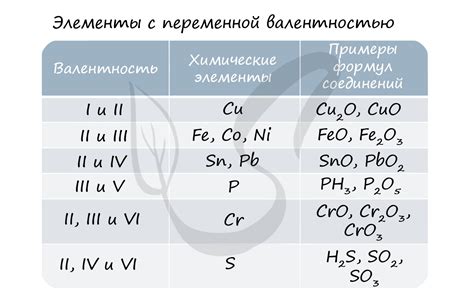
Степень окисления металла CuO указывает на количество электронов, которые металл отдал или принял при образовании оксида меди (II). Окисление представляет собой процесс потери электронов, а восстановление - приобретение электронов. Степень окисления позволяет определить, какие элементы в соединении являются окислителями или восстановителями.
Степень окисления металла CuO равна +2, так как медь (Cu) при образовании CuO теряет два электрона. Это означает, что медь окисляется на +2. Окисление металла может иметь различные степени, которые зависят от условий реакции и окружающей среды.
Вещества с положительной степенью окисления считаются окислами, так как способны принимать электроны от других веществ. В случае CuO, медь является окислителем. Окисление металла может происходить при контакте с кислородом воздуха или при реакции с другими веществами.
Знание степени окисления металла CuO позволяет понять его химические свойства и возможные реакции с другими веществами. Кроме того, степень окисления металла является важным показателем в химических уравнениях и расчетах реакций.
Определение и объяснение

Степень окисления металла CuO определяет, сколько электронов металл передал другому веществу или атому при химической реакции окисления. Степень окисления может быть положительной, отрицательной или равной нулю в зависимости от того, сколько электронов металл переходит или принимает.
Степень окисления металла CuO в окислительной реакции может быть положительной или отрицательной в зависимости от условий реакции и окислительного агента. Положительная степень окисления означает, что металл передает электроны другому веществу и окисляется, а отрицательная степень окисления указывает на то, что металл принимает электроны и восстанавливается.
Для металла CuO, степень окисления можно определить по правилам окислительной способности элементов. В этом случае CuO имеет степень окисления +2, так как медь обычно имеет степень окисления +2 в соединениях.
Знание степени окисления металла CuO важно для определения перехода электронов и понимания характера химических реакций, в которых участвует этот металл. Также степень окисления может помочь в расчетах количества веществ, участвующих в реакции и определении реакционных условий.
Как измерить степень окисления металла CuO?
Для измерения степени окисления металла CuO необходимо провести ряд экспериментов и использовать соответствующие химические методы анализа.
Один из способов измерения степени окисления металла CuO - определение его массы. Для этого можно взвешивать образец металла перед и после окисления и вычислить разницу массы. Таким образом, можно определить количество кислорода, участвующего в реакции окисления.
Другой метод измерения степени окисления металла CuO - использование реакции с красителем. Краситель, окрашенный в одной степени, взаимодействует с металлической поверхностью CuO, а затем изменяет свой цвет. Путем сравнения исходного и измененного цветов можно определить степень окисления металла.
Также можно использовать электрохимические методы для измерения степени окисления металла CuO. Например, можно провести эксперимент с использованием электролитической ячейки, где металл CuO будет служить анодом. Путем измерения тока, протекающего через ячейку, можно определить степень окисления металла.
Важно отметить, что результаты измерения степени окисления металла CuO могут зависеть от условий эксперимента, таких как температура, давление, концентрация реагентов и других факторов. Поэтому для получения более точных результатов следует проводить несколько повторных измерений и проводить контрольные эксперименты.
Реакции и свойства металла CuO

Металл CuO обладает рядом уникальных реакций и свойств, которые делают его важным компонентом в различных промышленных процессах и технологиях.
1. Окислительные свойства: CuO обладает высокой окислительной активностью. Он способен взаимодействовать с различными веществами, уступая свои электроны и переходя в более низкую степень окисления. Например, CuO может окисляться до более стабильной формы металла, такой как Cu.
2. Реакция с кислотами: Металл CuO реагирует с кислотами, образуя соли меди и воду. Например, при взаимодействии с соляной кислотой образуется хлорид меди и вода:
- CuO + 2HCl → CuCl2 + H2O
3. Реакция с основаниями: CuO также реагирует с основаниями, образуя соли меди и воду. Например, при взаимодействии с гидроксидом натрия образуется гидроксид меди и натрия:
- CuO + 2NaOH → Cu(OH)2 + Na2O
4. Реакция с кислородом: Под действием кислорода, металл CuO может взаимодействовать с органическими веществами, такими как алкоголи и алдегиды, образуя соответствующие карбонаты или карбоксилаты меди.
5. Физические свойства: Металл CuO обладает высокой температурой плавления, что делает его устойчивым к высоким температурам. Он также обладает хорошей электропроводностью и является хорошим проводником тепла.
Помимо вышеуказанных реакций и свойств, металл CuO также может использоваться в качестве катализатора для различных химических реакций, а также в производстве различных материалов, включая электроды, магнитные материалы и керамику.
Применение металла CuO

Металл CuO или оксид меди (II) используется в различных отраслях промышленности и науки благодаря своим уникальным свойствам и химическим реакциям.
Оксид меди часто применяется в области катализа. Благодаря своей высокой активности, CuO используется в процессах окисления, включая окисление органических соединений и аммиака. В каталитических реакциях CuO способствует образованию различных продуктов, играя важную роль в производстве пластмасс, лекарственных веществ и многих других химических соединений.
Металл CuO также находит применение в производстве красок и пигментов. Благодаря своему яркому зеленому цвету, CuO используется для окрашивания керамических изделий, стекла и косметических продуктов. Кроме того, металл CuO используется в производстве электронных компонентов, включая полупроводники и солнечные элементы.
Оксид меди также находит применение в биологии и медицине. Из-за своих антибактериальных и противогрибковых свойств, CuO используется в производстве антибактериальных покрытий для ран и поверхностей, а также для лечения различных инфекций и заболеваний кожи.
Помимо этого, металл CuO используется в производстве аккумуляторов, суперконденсаторов, противопожарных материалов, эмалей, шлифовальных материалов и многого другого. Благодаря своим уникальным свойствам и разнообразным применениям, CuO остается востребованным материалом современного промышленного производства.
Выводы о степени окисления металла CuO

Степень окисления металла CuO может быть определена с помощью различных экспериментальных методов и аналитических приборов.
Одним из таких методов является измерение электрохимического потенциала раствора CuO. По изменению потенциала можно судить о том, в каком состоянии находится металл CuO - окисленном или восстановленном состоянии.
Другим методом определения степени окисления CuO является спектральный анализ. По спектру поглощения или излучения можно определить, какие энергетические уровни заняты электронами в атомах металла CuO и, следовательно, установить степень окисления этого металла.
Также степень окисления металла CuO можно определить с помощью химических реакций. Например, при взаимодействии CuO с кислородом в результате окисления происходит образование Cu2O, что указывает на исходное состояние металла. Путем анализа процесса реакции и продуктов можно сделать выводы об исходной степени окисления металла CuO.
Таким образом, степень окисления металла CuO может быть определена с использованием различных методов и инструментов, таких как измерение электрохимического потенциала, спектральный анализ и химические реакции. Комбинированный подход позволяет получить более точные и надежные результаты.
Вопрос-ответ

Что такое степень окисления металла CuO?
Степень окисления металла CuO – это число, которое показывает, сколько электронов металл передаёт другому элементу, когда образуется соединение CuO. В данном случае, металлом является медь (Cu), а кислород (O) – другой элемент.
Какова степень окисления металла CuO и как она определяется?
Степень окисления металла CuO равна +2. Она определяется через заряд атома металла в соединении, то есть, в данном случае, через заряд меди (Cu). Так как кислород (O) обладает зарядом -2, а в молекуле есть два атома кислорода, то заряд меди должен быть равен +2, чтобы суммарный заряд соединения был равным нулю.
