Активные металлы являются основными элементами в химических реакциях благодаря способности активно взаимодействовать с различными веществами. Кислотные соли активных металлов, такие как хлориды, сульфаты и нитраты, обладают рядом уникальных свойств и химической активностью в растворах. В данной статье рассмотрим основные свойства и особенности среды растворов кислых солей активных металлов.
Первым свойством, на которое следует обратить внимание, является кислотность растворов кислых солей активных металлов. При растворении кислых солей в воде происходит диссоциация, т.е. разделение молекулы соли на ионы. Присутствие активных металлов позволяет образовывать ионы положительного заряда, которые обусловливают кислотность среды. Именно поэтому растворы кислых солей активных металлов проявляют кислотные свойства, например, образуют реакции с щелочами или показывают указания на высокую кислотность с помощью кислотометрических методов.
Кислотные соли активных металлов также обладают особенностями своей структуры и состава. Они часто представляют собой кристаллические соединения с определенными особенностями решетки, признаких упорядоченного строения. В зависимости от размеров и заряда ионов, кислотные соли активных металлов могут иметь различную степень солевого характера и координационных связей между ионами в кристаллической сетке.
Важным аспектом химической активности растворов кислых солей активных металлов является их способность окислять или восстанавливать другие вещества. Активные металлы, такие как натрий, калий или магний, могут активно отдавать свои электроны в процессе реакций окисления. Реакционная способность кислых солей активных металлов может быть использована в различных химических процессах, включая электрохимические реакции, гальваностегические процессы и синтез органических соединений.
Химическая активность среды растворов кислых солей активных металлов

Химическая активность среды растворов кислых солей активных металлов определяется их способностью образовывать гидроксиды при взаимодействии с водой. Эти растворы обладают выраженной щелочной реакцией, так как при соприкосновении с водой ионно-общей средой происходит гидролиз катионов металла.
Гидролиз кислых солей активных металлов приводит к образованию гидроксидов и оксидов металлов, которые обладают щелочными свойствами. Например, гидролиз сульфата натрия, соли активного металла натрия, приводит к образованию гидроксида натрия и сульфата натрия.
При растворении кислых солей активных металлов происходит их диссоциация на ионы металла и анионы кислоты. Это способствует образованию окислительно-восстановительных реакций, так как ионы металла могут участвовать в окислительной или восстановительной реакции.
Среды растворов кислых солей активных металлов также обладают высокой электропроводностью, так как ионы металла и анионы кислоты оказываются электролитами. Это связано с тем, что активные металлы в растворе образуют положительные ионы, которые передвигаются к аноду, а анионы кислоты передвигаются к катоду, что обеспечивает электропроводность раствора.
Таким образом, растворы кислых солей активных металлов проявляют химическую активность, связанную с образованием гидроксидов, оксидов и проведением электропроводности. Эти свойства определяют их роль в различных химических реакциях и процессах, как в природных, так и в промышленных условиях.
Свойства растворов кислых солей
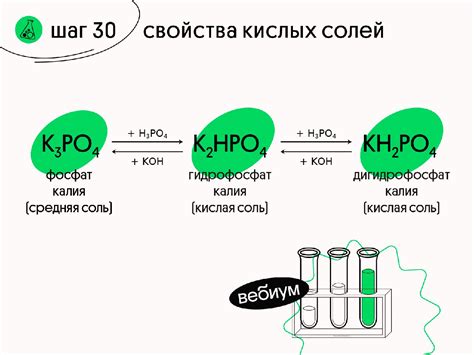
Растворы кислых солей активных металлов обладают рядом специфических свойств, которые определяются как их химическими особенностями, так и физическими параметрами. Важное свойство таких растворов - их кислотность, обусловленная наличием в них ионов водорода (Н+) и соответствующих кислотных групп. Такие растворы обычно обладают кислым вкусом и способностью вызывать раздражение слизистых оболочек.
Кроме того, растворы кислых солей являются электролитами, то есть они проводят электрический ток. Это обусловлено ионизацией солей в растворе, когда металлический катион отделяется анионом кислоты. Такое поведение растворов кислых солей позволяет им находить применение в электрохимических процессах и как электролиты в различных системах.
Также стоит отметить, что растворы кислых солей могут обладать коррозионной активностью, то есть вызывать разрушение материалов при контакте с ними. Это связано с химической активностью активных металлов, которые могут осуществлять окислительные реакции с органическими и неорганическими веществами, приводящие к повреждениям или разрушению материала.
Кроме того, растворы кислых солей могут проявлять свойства, связанные с осаждением солей, образованием осадка или отдельных фрагментов. Это может происходить при изменении условий температуры, концентрации соли или рН раствора. Образование осадка может приводить к изменению физических характеристик раствора и требовать специальных приемов для его удаления или предотвращения.
Активность металлов в растворах

Активность металлов в растворах зависит от их химических свойств и реакций с веществами, находящимися в растворах. Растворы кислых солей активных металлов обладают специфической химической активностью, которая определяется способностью металла образовывать ионы в растворе.
Активные металлы, такие как натрий, калий, магний и цинк, имеют высокую активность в растворах кислых солей. Они способны легко реагировать с водой и различными кислотами, образуя ионы металла и выделяя водород. Такие реакции приводят к образованию щелочных растворов или растворов, содержащих металлические ионы.
Активность металлов в растворах также может быть определена их способностью образовывать соединения с другими веществами в растворе. Например, активные металлы могут образовывать соли с кислотами, образуя ионы металла и ионы аниона кислоты.
Электрохимическая активность металлов в растворах зависит от их возможности активно участвовать в протекании электрохимических процессов. Например, активные металлы могут быть использованы в качестве электродов в электрохимических ячейках и батареях, где они окисляются и восстанавливаются в процессе обмена электронами с веществами в растворе.
Электронный перенос в растворах
В растворах кислых солей активных металлов происходит электронный перенос, который является важным аспектом химической активности и свойств среды. Электронный перенос представляет собой передачу электронов между различными веществами в растворе. Главную роль в этом процессе играют ионы металлов и их электронные оболочки.
При растворении кислых солей активных металлов в воде происходит диссоциация, то есть распад соли на ионы. Это позволяет электронам находиться в движении и образовывать ток в растворе. Ионы катиона металла, обладая положительным зарядом, могут взаимодействовать с электронами отрицательно заряженных ионов аниона в растворе.
Электронный перенос в растворах кислых солей активных металлов является основой для процессов окисления и восстановления. Катионы металлов способны передавать электроны анионам, что приводит к образованию ионных связей и стабилизации раствора. Это позволяет установить равновесие между различными формами существования ионов и электронов.
Электронный перенос в растворах кислых солей активных металлов имеет большое значение в химических реакциях и процессах, происходящих в электрохимических системах. Он определяет возможность реакций окисления-восстановления, регулирует активность ионов металлов и их способность вступать во взаимодействие с другими веществами. Понимание механизмов электронного переноса в растворах помогает объяснить множество физико-химических явлений и является основой для разработки новых технологий и материалов.
Влияние растворов кислых солей на окружающую среду

Растворы кислых солей активных металлов обладают высокой химической активностью и могут оказывать значительное влияние на окружающую среду. Как правило, они обладают ярко выраженной коррозионной активностью, что может привести к разрушению материалов и инфраструктуры вблизи мест их выпуска.
Кроме того, растворы кислых солей активных металлов могут оказывать негативное влияние на биоту водных экосистем. Кислотные соединения, образующиеся при диссоциации кислых солей, могут изменять pH воды и нарушать ее химическое равновесие. Это может привести к гибели водных организмов, таких как рыбы, микроорганизмы и водные растения.
Кроме того, кислые растворы активных металлов могут быть опасными для здоровья человека. При неправильном обращении с ними их испарения могут вызывать раздражение глаз, кожи и дыхательных путей. При попадании в организм могут возникать отравления, которые могут быть опасными для жизни и здоровья.
В целях минимизации негативного влияния растворов кислых солей на окружающую среду необходимо соблюдать правила безопасного обращения с ними и обеспечивать их надежное упаковывание и хранение. Также необходимо проводить контрольные мероприятия и мониторинг качества окружающей среды вблизи мест их использования и хранения, чтобы своевременно выявлять и предотвращать возможные загрязнения.
Коррозия металлов в растворах кислых солей
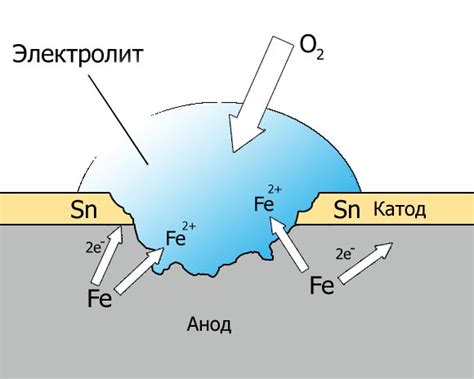
Коррозия металлов в растворах кислых солей является одной из наиболее распространенных форм химической разрушительной активности для металлических материалов. Кислые соли содержат в своей структуре положительные активные металлы, которые образуют с металлами электрохимические пары, вызывающие коррозию.
Процесс коррозии металлов в растворах кислых солей характеризуется активными реакциями электродных пар. Причинами коррозии являются окисление металла в анодной зоне и восстановление положительного активного металла в катодной зоне. Это приводит к проникновению металлического материала, образующего коррозионные явления, в раствор кислотного компонента среды раствора.
Коррозийная активность растворов кислых солей сильно зависит от их концентрации и pH. Кислотность среды способствует активированию электродных процессов и интенсификации коррозии. Кроме того, на скорость коррозии влияет также температура среды и содержание примесей.
Для предотвращения коррозии металлов в растворах кислых солей применяют различные защитные методы. Одним из них является покрытие металла защитными пленками, такими как эмали или лаки. Другим методом является установка анодной защиты, которая предусматривает подключение стального анода к металлическому оборудованию для предотвращения коррозии. Также важным фактором является контроль состояния среды растворов, в том числе поддержание оптимального значения pH и концентрации кислых солей. Мониторинг и регулировка данных параметров позволяет предотвратить разрушение металлических конструкций и увеличить их срок службы.
Применение растворов кислых солей активных металлов
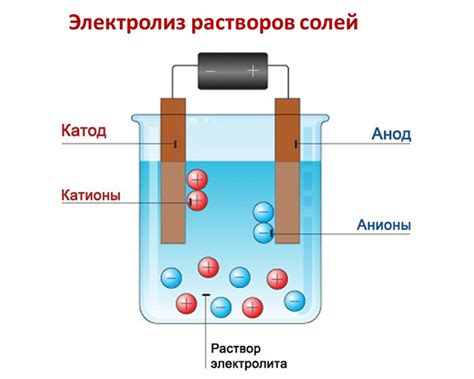
Растворы кислых солей активных металлов находят широкое применение в различных отраслях науки и промышленности. Одним из наиболее распространенных применений является использование этих растворов в гальванических процессах. Например, растворы кислых солей активных металлов, таких как железо, медь, цинк, используются в процессе электролитического осаждения металлических покрытий на различных поверхностях.
Кроме того, растворы кислых солей активных металлов используются как катализаторы в химической промышленности. Например, сульфаты железа и меди часто применяются в процессе производства серной кислоты. Каталитические свойства растворов кислых солей активных металлов позволяют ускорить химические реакции и повысить их выход продукта.
Еще одним важным применением растворов кислых солей активных металлов является использование их в медицине. Например, раствор сульфата магния применяется в качестве противосудорожного средства и для лечения гипомагниемии. Раствор сульфата цинка применяется для лечения гнойного воспаления кожи и слизистых оболочек.
Также стоит отметить, что растворы кислых солей активных металлов имеют широкое применение в аналитической химии. Они используются для определения содержания металлов в различных образцах, а также для подавления нежелательных реакций при анализе.
В целом, растворы кислых солей активных металлов являются важными компонентами в различных промышленных процессах, научных исследованиях и медицинской практике. Их уникальные свойства и химическая активность делают их неотъемлемой частью современного мира.
Факторы, влияющие на химическую активность растворов кислых солей

Химическая активность растворов кислых солей активных металлов зависит от нескольких факторов, которые определяют их свойства и реакционную способность.
Первым фактором является концентрация кислоты, которая влияет на уровень ионизации соли в растворе. Чем выше концентрация кислоты, тем больше ионов металла будет присутствовать в растворе, что способствует увеличению химической активности раствора.
Вторым фактором является величина заряда ионов металла. Чем больше заряд иона металла, тем больше энергии требуется для его ионизации и реакций с другими веществами. Это делает раствор более химически активным.
Третьим фактором влияющим на химическую активность является размер ионов металла. Если ионы металла имеют малый размер, они могут достигать более высоких концентраций, что усиливает их химическую активность. Кроме того, малые ионы имеют большую мобильность, что делает их более доступными для реакций со средой раствора.
И наконец, четвертый фактор, влияющий на химическую активность, - это реакционные свойства кислых солей активных металлов. Некоторые соли могут образовывать комплексные соединения с другими веществами или проявлять окислительные свойства, что усиливает их химическую активность и способность к реакциям.
Способы уменьшения химической активности растворов кислых солей активных металлов

1. Добавление кислородосодержащих препаратов. В целях уменьшения химической активности растворов кислых солей активных металлов можно применить кислородосодержащие препараты, такие как перекись водорода или кислород в газообразной форме. Эти вещества способны участвовать в окислительно-восстановительных реакциях и связывать активные ионы металлов.
2. Понижение концентрации. Другим способом уменьшения химической активности растворов кислых солей является понижение их концентрации. Это можно сделать путем разбавления раствора с помощью воды или добавления нейтральных растворов. Уменьшение концентрации солей может снизить их реакционную способность и химическую активность.
3. Добавление катионов с меньшей химической активностью. Еще одним способом уменьшения химической активности растворов кислых солей активных металлов является добавление катионов с меньшей химической активностью. Например, можно добавить катионы натрия или калия, которые обладают меньшей реакционной способностью по сравнению с активными металлами. Это может привести к уменьшению химических реакций и снижению активности раствора.
4. Регулирование pH. Регулирование pH раствора также может влиять на его химическую активность. Увеличение значения pH, делая раствор менее кислым, может снизить активность кислых солей активных металлов. И наоборот, уменьшение pH делает раствор более кислым и повышает его химическую активность.
Вопрос-ответ

Какие свойства имеют растворы кислых солей активных металлов?
Растворы кислых солей активных металлов обладают рядом характерных свойств. Они обычно обладают кислотно-щелочными свойствами, могут иметь высокую электропроводность, изменять окраску, их pH может быть ниже 7. Кроме того, они могут быть коррозионно активными и обладать интенсивным запахом.
Каковы основные явления, определяющие химическую активность среды растворов кислых солей активных металлов?
Химическая активность растворов кислых солей активных металлов определяется рядом явлений. Прежде всего, это отдача металла, при которой активный металл переходит в ионное состояние. Кроме того, имеет место образование комплексных ионообменных реакций, реакций гидролиза и окислительно-восстановительных процессов.
Что происходит с раствором кислых солей активных металлов при нагревании?
При нагревании растворов кислых солей активных металлов могут происходить различные процессы. Это может быть обезводнение соли, кристаллизация воды, аммиака и др., образование остатка в виде соли, оксида или гидроксида активного металла. Также при нагревании может происходить порошение соли, разложение с образованием газов, окисление или восстановление веществ.
Какие факторы влияют на растворимость кислых солей активных металлов?
Растворимость кислых солей активных металлов зависит от нескольких факторов. Одним из них является концентрация ионов в растворе. Чем выше концентрация ионов, тем выше растворимость. Также важную роль играют температура раствора, его pH и наличие других химических веществ, которые могут вступать в реакцию с кислыми солями активных металлов.
