Водород – самый легкий элемент в таблице Менделеева, однако его свойства обладают уникальностью и всегда вызывают большой интерес у исследователей. В то же время, металлы – это группа элементов, обладающих высокой проводимостью электричества и тепла, а также способностью приобретать металлический блеск. Несмотря на сильные различия в своих свойствах, водород и металлы также имеют некоторые сходства.
Прежде всего, следует отметить, что как водород, так и металлы являются химическими элементами и имеют сходную структуру атомов. Водород в своей наиболее распространенной форме состоит из одного атома, что делает его особенным по сравнению с другими элементами, которые обычно образуют кристаллическую решетку. В то же время, металлы также обладают кристаллической структурой и могут быть одно- или многокомпонентными.
Кроме того, и водород, и металлы являются хорошими проводниками электричества. Металлы имеют высокую электропроводность благодаря свободным электронам, которые могут свободно двигаться в металлической решетке. Водород также обладает неплохой электропроводимостью, особенно при повышенных температурах и давлении. Это делает его применимым в технологиях водородной энергии и в различных электрохимических процессах.
В целом, хотя водород и металлы имеют много различий в своих свойствах, они также имеют некоторые сходства. Оба являются химическими элементами, имеют кристаллическую структуру и могут быть хорошими проводниками электричества. Изучение и сравнение этих двух групп элементов позволяет нам лучше понять законы природы и создать новые технологии, основанные на их свойствах.
Водород и металлы: сходства и различия

Водород и металлы, несмотря на различные свойства и химические характеристики, имеют как сходства, так и различия.
Одно из сходств между водородом и металлами заключается в их способности образовывать ионы с положительным зарядом. Водород при наличии свободного электрона может образовывать положительный ион, обычно принимая форму H+. Точно так же металлы образуют положительные ионы, освобождая электроны и образуя ион с положительным зарядом.
Кроме того, и водород, и металлы обладают высокой теплопроводностью. Они оба могут легко передавать тепло через свою структуру, что делает их эффективными теплопроводниками. Это свойство широко используется при создании металлических конструкций и водородных сегментов в различных областях науки и промышленности.
Однако, существуют и различия между водородом и металлами. Водород является неметаллом и входит в периодическую систему химических элементов в группе неметаллов. В то время как металлы являются специфической группой элементов, характеризующихся высокой проводимостью электричества и тепла.
Кроме того, металлы имеют большую плотность и твердость по сравнению с водородом. Химически, металлы обычно образуют ионы, обладающие положительным зарядом, в то время как водород может образовывать и положительные, и отрицательные ионы, в зависимости от условий.
Таким образом, водород и металлы имеют как сходства, так и различия, которые определяют их химические и физические свойства. Понимание этих различий помогает углубить наше знание о строении и свойствах веществ и применить его в различных областях науки и технологий.
Физические свойства водорода и металлов

Водород - легкий и химически активный элемент, характеризующийся низким кипением и плотностью. Он является самым легким элементом в таблице Менделеева и находится в первой группе. Водород имеет газообразное состояние при обычных условиях, но при низких температурах и высоких давлениях может переходить в жидкое или твердое состояние. Его плотность составляет 0,0899 г/л, что делает его легким и подвижным веществом.
Металлы - элементы, обладающие хорошей электропроводностью и теплопроводностью. Они обычно имеют металлический блеск и являются твердыми при комнатной температуре, хотя некоторые металлы могут быть мягкими и пластичными. Металлы обладают высокой плотностью и тяжелой атомной массой, что делает их крепкими и прочными материалами. Они обладают высокой точкой плавления и кипения.
Основные физические свойства водорода и металлов можно сравнить в следующей таблице:
| Свойство | Водород | Металлы |
|---|---|---|
| Агрегатное состояние при обычных условиях | Газ | Твердое |
| Температура плавления | -259.16 °C | Различается для разных металлов |
| Температура кипения | -252.87 °C | Различается для разных металлов |
| Плотность | 0.0899 г/л | Различается для разных металлов |
| Электропроводность | Плохая | Хорошая |
| Теплопроводность | Плохая | Хорошая |
Таким образом, водород и металлы отличаются по своему агрегатному состоянию при обычных условиях, температуре плавления и кипения, а также по плотности, электропроводности и теплопроводности. Они имеют разные физические свойства и химическую активность, что делает их уникальными элементами таблицы Менделеева.
Химические свойства водорода и металлов

Водород и металлы обладают некоторыми сходными химическими свойствами, что обусловлено их общей строительной особенностью - наличием свободных электронов во внешней оболочке. Оба элемента способны образовывать ионные или ковалентные соединения с другими элементами. Кроме того, и водород, и металлы проявляют активность при вступлении в химические реакции, что позволяет им образовывать различные соединения.
Металлы, в отличие от водорода, обладают выраженной металлической проводимостью, что связано с перемещением свободных электронов внутри кристаллической решетки. При взаимодействии с другими веществами металлы способны образовывать ионы положительного заряда, что определяет их роль в химических реакциях и формирование соединений с отрицательно заряженными частицами.
Водород, в свою очередь, обладает уникальной способностью к образованию водородных связей, которые являются одними из наиболее прочных связей в химии. Водород образует соединения с многими не только металлами, но и неметаллами, такими как кислород, азот, сера и др. В результате образуется широкий спектр соединений с различными свойствами и применениями.
Таким образом, химические свойства водорода и металлов перекликаются и находятся взаимосвязи, однако каждый из них обладает и уникальными особенностями и способностями при вступлении в химические реакции.
Реактивность водорода и металлов

Водород и металлы обладают высокой реактивностью. Однако, хотя их реакции могут проявлять сходство, также существуют определенные отличия.
Водород обладает высокой активностью и способен реагировать с различными элементами в зависимости от условий. С металлами водород может образовывать металловодородные соединения, например, металлический гидрид. В реакциях с водородом металлы обычно выступают в качестве окислителя.
Реакции водорода с металлами могут протекать различными способами, включая образование солей или ионных соединений. В некоторых случаях, реакции водорода с металлами могут быть экзотермическими и высвобождать значительное количество энергии.
Однако, не все металлы равномерно реагируют с водородом. Некоторые металлы, такие как железо или алюминий, образуют слабые соединения с водородом и реагируют с ним только при высокой температуре или в присутствии катализаторов. Другие металлы, например, натрий или калий, активно реагируют с водородом уже при комнатной температуре.
Таким образом, реактивность водорода и металлов является важным фактором, который определяет возможность и характер процессов, в которых они участвуют. Понимание особенностей реакций водорода с металлами позволяет использовать эти процессы в различных областях, включая энергетику, каталитическую химию и материаловедение.
Использование водорода и металлов в промышленности

Водород и металлы играют важную роль в различных отраслях промышленности благодаря своим уникальным свойствам и широкому спектру применений.
Водород является ключевым сырьем для производства аммиака, который используется в производстве удобрений, например, аммиачной селитры. Также водород используется в процессах гидрогенизации, где он служит реагентом для превращения различных органических соединений, например, растительных масел, в топливо или добавку к топливу. Кроме того, водород используется в производстве стали, где он служит средством десульфурации и улучшения качества металла.
Металлы также являются неотъемлемой частью промышленности. Например, алюминий широко используется в авиационной и автомобильной промышленности из-за своей легкости, прочности и устойчивости к коррозии. Медь является ключевым материалом для производства электрических проводов и кабелей благодаря своей высокой электропроводности. Железо и его сплавы используются в строительстве и производстве механизмов.
Важно отметить, что водород и металлы также могут быть использованы в совместных процессах. Например, водород может быть использован для производства аммиака, который является основной сырьевой основой для производства удобрений, содержащих такие металлы как азот, фосфор и калий.
Выводящий водород и металлы вместе открывает новые возможности исследований и разработок в области промышленности, их применение в различных отраслях и постоянное развитие технологий позволяют создавать новые продукты с улучшенными характеристиками и снижением затрат.
Роль водорода и металлов в экологической сфере

Водород – один из ключевых игроков в экологической сфере, благодаря своим уникальным свойствам. Во-первых, водород является чистым источником энергии, поскольку его сгорание не ведет к выделению углекислого газа, который является одним из основных виновников парникового эффекта. Кроме того, водород может быть использован как сырье для производства и хранения электроэнергии, что делает его незаменимым в решении проблемы перехода на возобновляемые источники энергии.
Металлы, в свою очередь, также играют важную роль в экологической сфере. Многие металлы используются в процессах очистки воды и загрязненного воздуха. Например, железо может служить для удаления нитратов и фосфатов из воды, а активированный уголь – для поглощения различных загрязнителей из атмосферы. Кроме того, металлы широко применяются в процессах рециклинга и утилизации отходов, что помогает сократить объемы отходов и уменьшить негативное воздействие на окружающую среду.
Таким образом, как водород, так и металлы играют важную роль в экологической сфере. Они предоставляют новые возможности для создания чистых источников энергии, обеспечивают очистку воды и воздуха, а также способствуют улучшению систем утилизации отходов. Однако важно помнить, что эффективное использование водорода и металлов требует разработки и внедрения соответствующих технологий и инфраструктуры.
Валентность водорода и металлов
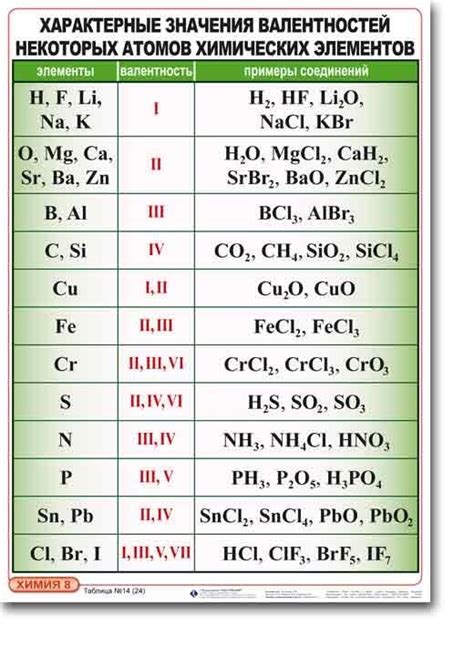
Водород и металлы имеют различную валентность, что определяет их способность к образованию химических соединений. Водород обладает валентностью +1, что означает, что в химических соединениях он может присоединиться к атомам других элементов, образуя положительный ион H+.
Металлы, в свою очередь, имеют валентность, равную своему заряду, и, как правило, положительную. Например, валентность железа (Fe) может быть +2 или +3, а валентность алюминия (Al) всегда равна +3. Это означает, что атомы этих металлов могут образовывать соединения, в которых они отдают два или три электрона соответственно.
Валентность элемента определяется его электронной конфигурацией. Водород имеет один электрон в своей внешней оболочке, поэтому его валентность равна +1. У металлов, обычно, внешней оболочкой является s- или p-подобная подоболочка. В зависимости от количества электронов в этой подоболочке, валентность металла определяется числом электронов, которое он может отдать при образовании соединений.
Физические свойства соединений водорода и металлов
Соединения водорода и металлов обладают рядом особых физических свойств, которые делают их уникальными в мире химии. Водород, будучи легким и газообразным элементом, образует различные соединения с металлами, обладающими металлическими свойствами.
Одной из основных особенностей соединений водорода с металлами является их высокая теплопроводность. Это связано с высокой подвижностью электронов в металлах и способностью водорода эффективно передавать тепловую энергию. Благодаря этому, соединения водорода с металлами широко используются в различных технологиях, включая производство металлических сплавов и электролиз воды.
Еще одной характеристикой соединений водорода с металлами является их высокая пластичность. Металлы, образующие соединения с водородом, обладают способностью к легкому превращению в различные формы без потери своих металлических свойств. Это делает возможным использование таких соединений для создания различных изделий и конструкций.
Кроме того, соединения водорода с металлами обладают высокой электропроводностью. Это объясняется наличием свободных электронов в металлах, которые способны эффективно перемещаться внутри соединения. Такая электропроводность может быть использована во множестве различных электротехнических приложений.
В заключение, соединения водорода с металлами обладают рядом уникальных физических свойств, включая высокую теплопроводность, пластичность и электропроводность. Эти свойства делают их очень ценными в различных отраслях промышленности и технологии.
Применение соединений водорода и металлов в науке и технологиях
Соединения водорода и металлов находят широкое применение в различных областях науки и технологий. Великая электроотрицательность водорода и его способность образовывать химические связи с металлами делают эти соединения особо интересными.
Одним из важных применений соединений водорода с металлами является производство металлов. Водород используется в процессе восстановления металлических руд, что позволяет получать металлы высокой чистоты. Кроме того, соединения водорода с металлами широко применяются в процессах электролиза для получения металлов из их солей.
Еще одной важной областью применения соединений водорода и металлов является производство водорода. Металлы могут служить в качестве катализаторов при генерации водорода путем разложения воды. Также соединения водорода с металлами активно используются в процессах синтеза аммиака, который является важным компонентом в производстве удобрений.
Соединения водорода и металлов обладают высокой проводимостью тепла и электричества. Это свойство находит применение в технологиях, связанных с передачей энергии. Например, соединения водорода с платиной используются в водородных паливных элементах, которые являются эффективными источниками энергии.
Соединения водорода и металлов также широко используются в области хранения и транспортировки водорода. Металлические сплавы с водородом обладают высокой плотностью водорода, что позволяет хранить и транспортировать его в удобном для использования состоянии.
В целом, соединения водорода и металлов имеют большое значение в науке и технологиях, обеспечивая эффективные способы получения металлов, производства водорода, передачи энергии и хранения водорода.
Вопрос-ответ

Какие особенности обладает водород?
Водород является уникальным элементом, так как он обладает свойствами и металлов и неметаллов. Он легче воздуха, обладает высокой энергетической плотностью и может гореть в присутствии кислорода. Также водород обладает возможностью формировать ковалентные и ионные связи.
Чем схожи водород и металлы?
Водород и металлы обладают рядом сходных свойств. Они оба могут проводить ток электричества и тепло, обладают высокой пластичностью и может образовывать ионные связи. Также водород, подобно металлам, обладает способностью образовывать сплавы с другими веществами.
Какие отличия между водородом и металлами можно выделить?
Водород и металлы имеют и ряд отличительных черт. В отличие от металлов, водород обладает газообразным состоянием при комнатной температуре и атмосферном давлении. Кроме того, водород имеет более низкую энергию ионизации и электроотрицательность. Также, хотя водород способен образовывать ионные связи, он обычно образует ковалентные связи в соединениях с другими элементами.
