Оксиды активных металлов являются основными соединениями, образующимися при взаимодействии металлов с кислородом. Они обладают широким спектром свойств и являются важными веществами в различных сферах промышленности и научных исследований.
Оксид калия (К2O) - один из наиболее распространенных оксидов активных металлов. Он образуется при сжигании калия в кислороде или при нагревании калия с кислородом содой, и является белым кристаллическим веществом. Оксид калия широко применяется в производстве стекла, мыла, щелочей и других продуктов.
Оксид натрия (Na2O) - еще один важный оксид активного металла. Он образуется при сжигании натрия в кислороде или при нагревании натрия с кислородом. Оксид натрия имеет вид белого порошка и широко используется в производстве стекла, моющих средств и щелочей. Он также применяется в процессе производства электролитического алюминия.
Оксид магния (MgO) - еще один из оксидов активных металлов. Он образуется при сжигании магния в кислороде или при нагревании магния с кислородом. Оксид магния является белым кристаллическим веществом и широко используется в производстве огнеупорных материалов, цемента, косметических средств и лекарственных препаратов.
Оксид лития
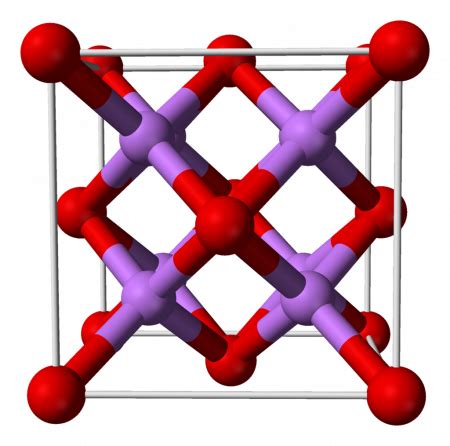
Оксид лития - это химическое соединение, образующееся при соединении активного металла - лития - с кислородом.
Оксид лития химически обозначается формулой Li2O и представляет собой сильный окислитель. Он обладает белым цветом и кристаллической структурой. Оксид лития является щелочным соединением и растворяется в воде с образованием щелочной реакции и образованием гидроксида лития.
Оксид лития широко применяется в различных областях. Он используется в производстве стекла и керамики, а также в электрохимических процессах. Благодаря своим свойствам оксид лития также применяется в качестве катализатора и добавки в различные химические реакции.
Оксид лития также используется в медицине. Его вещества широко применяют в качестве противорвотного и противоэпилептического средства. Они используются для лечения некоторых психических расстройств, таких как биполярное и маниакально-депрессивное расстройство.
Оксид натрия
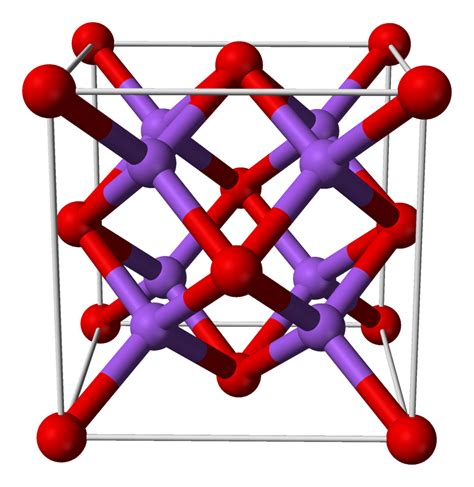
Оксид натрия - неорганическое соединение, состоящее из атомов натрия и кислорода. Химическая формула данного вещества - Na2O. Оксид натрия является амфотерным оксидом, что означает его способность взаимодействовать с кислотами и щелочами.
Это белая кристаллическая вещество образует гигроскопическую модификацию Na2O·10H2O, которая называется гидратированным оксидом натрия. Однако стабильна только в непрерывно влажной среде, в сухом виде он превращается в анионный диозид согласно реакции:
- 2Na2O·10H2O → Na2O + 9H2O
- Na2O → Na+ + O2-
- 2O2- + O2- → O2²-
Оксид натрия активно используется в различных отраслях промышленности. Он является одним из основных компонентов стекла, керамики и эмали. Также оксид натрия используется в процессе обработки руды при получении металла натрия и в производстве мыла, моющих средств и других химических препаратов.
Оксид калия
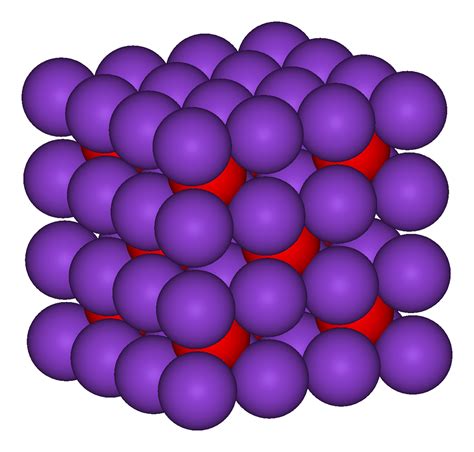
Оксид калия (K2O) - неорганическое соединение, состоящее из атомов калия и кислорода. Этот оксид является продуктом полного окисления калия. Он имеет белый кристаллический вид и молекулярную массу 94.2 г/моль.
Оксид калия широко используется в различных отраслях промышленности. Например, он применяется в качестве катализатора при производстве пластиков, смол, резиновых изделий и других органических соединений. Кроме того, оксид калия используется в стекольной промышленности для придания прозрачности стеклу и улучшения его химической стойкости.
Оксид калия обладает рядом свойств, которые делают его полезным в различных областях. Например, он хорошо растворяется в воде, образуя щелочную среду и способствуя проведению электрического тока. Кроме того, оксид калия является сильным окислителем и может служить источником кислорода в химических реакциях.
Стоит отметить, что оксид калия обладает высокой токсичностью и может вызывать серьезные ожоги при контакте с кожей или слизистыми оболочками. Поэтому при работе с этим веществом необходимо соблюдать меры предосторожности и использовать защитное снаряжение.
Оксид рубидия

Оксид рубидия – неорганическое соединение, образующееся при окислении металла рубидия воздухом. Химическая формула этого оксида – Rb2O. Он представляет собой белую кристаллическую или аморфную субстанцию.
Оксид рубидия обладает высокой растворимостью в воде и способен образовывать гидроксид рубидия (RbOH) путем взаимодействия с водой. Также этот оксид реагирует с кислородом и образует пероксид рубидия (Rb2O2).
Оксид рубидия широко используется в производстве стекла и керамики, так как вносит специфические свойства в эти материалы. Он также применяется в химической промышленности для получения рубидия и его соединений.
Физические свойства оксида рубидия включают высокую температуру плавления, низкую теплопроводность и устойчивость к агрессивным средам. Они делают его полезным в различных промышленных и научных областях, таких как электроника, оптика и плазменные технологии.
Оксид рубидия также обладает определенными медицинскими свойствами и может использоваться в фармацевтической промышленности для создания лекарственных препаратов и добавок к пище.
Оксид цезия

Оксид цезия (CeO2) представляет собой соединение активного металла цезия с кислородом. Это непрозрачное вещество, обладающее высокой твердостью и степенью кристалличности. Оксид цезия широко применяется в различных индустриальных процессах.
Оксид цезия может быть использован в качестве катализатора в химической промышленности. Он обладает превосходными катализаторными свойствами и может ускорять химические реакции, увеличивать их эффективность и снижать степень потери реакционного субстрата.
Оксид цезия также применяется в производстве керамики и стекла. Благодаря своим высоким теплопроводящим и электропроводящим свойствам, он может быть использован в качестве добавки для улучшения физических и химических свойств материалов.
Кроме того, оксид цезия играет важную роль в производстве солнечных элементов, таких как солнечные батареи и фотоэлементы. Он способствует повышению эффективности преобразования солнечной энергии в электрическую.
Оксид магния

Оксид магния - один из самых широко распространенных оксидов активных металлов. Химическая формула этого соединения MgO. Он получается при сгорании магния в присутствии кислорода или при нагревании магния воздухе.
Оксид магния обладает высокой температурной устойчивостью и используется в различных областях. Он является основным компонентом шлака, который получается при выплавке стали. Также оксид магния применяется в производстве огнеупорных материалов, таких как огнеупорные кирпичи, шамотные изделия и прочие.
В медицине оксид магния используется как лекарственное средство, известное под названием магния оксид. Оно имеет слабительное действие и применяется для лечения запоров. Также оксид магния используется в качестве антацидного средства при лечении заболеваний желудка.
Оксид магния также является неотъемлемой частью магниевых аккумуляторов. Он используется в этих устройствах в качестве одной из электродных пластин. Благодаря своим химическим и электрическим свойствам, оксид магния обеспечивает высокую энергоэффективность и надежную работу аккумуляторов.
Оксид кальция

Оксид кальция, также известный как известь, является химическим соединением, состоящим из ионов кальция и кислорода. Его химическая формула CaO. Оксид кальция является одним из наиболее распространенных оксидов активных металлов.
Оксид кальция имеет белый цвет и кристаллическую структуру. Он нерастворим в воде, но при соприкосновении с водой быстро превращается в гидроксид кальция, выделяя большое количество тепла. Это свойство оксида кальция делает его незаменимым компонентом в различных строительных материалах, таких как известь и цемент.
Оксид кальция обладает высокой степенью основности, поэтому он используется в производстве различных химических соединений, таких как карбид кальция и карбонат кальция. Кроме того, оксид кальция применяется в сельском хозяйстве как удобрение, так как он содержит в себе кальций, необходимый для роста растений.
В промышленности оксид кальция используется в процессе очистки сточных вод и дымовых газов, так как он способен связывать и удалять различные загрязнения. Кроме того, оксид кальция используется в производстве стекла, керамики и жидкой и твердой жаростойких материалов.
Вопрос-ответ

Какие металлы входят в список активных металлов?
В список активных металлов входят металлы, такие как натрий, калий, литий, магний, алюминий, цезий, рубидий и другие.
Какие оксиды входят в список оксидов активных металлов?
В список оксидов активных металлов входят оксиды таких металлов, как натрий (Na2O), калий (K2O), литий (Li2O), магний (MgO), алюминий (Al2O3) и других.
Какие свойства имеют оксиды активных металлов?
Оксиды активных металлов обладают такими свойствами, как щелочность, высокая теплоемкость, способность к растворению в воде, образование щелочных растворов, а также способность взаимодействовать с кислотами и образовывать соли.
Какие применения могут иметь оксиды активных металлов?
Оксиды активных металлов имеют различные применения, например, оксид натрия (Na2O) используется в производстве стекла и мыла, оксид калия (K2O) используется в сельском хозяйстве в качестве удобрения, оксид алюминия (Al2O3) используется в производстве керамики и абразивных материалов.
Какие свойства активных металлов обуславливают образование оксидов?
Свойства активных металлов, такие как высокая электроотрицательность, способность к диссоциации и реактивность, обуславливают образование оксидов при взаимодействии с кислородом.
