В химии реакция между серной кислотой и металлом является одной из наиболее распространенных химических реакций. Сульфатная кислота, или серная кислота (H2SO4), обладает сильной органической кислотностью и может реагировать с широким спектром металлов. Реакция серной кислоты с металлом протекает с образованием соли серной кислоты и выделением водорода.
Процесс реакции серной кислоты с металлом можно описать следующим образом: металл обесцвечивается и растворяется в серной кислоте, а на его месте образуется соль серной кислоты. Водород выделяется в виде пузырьков газа. Реакция сильно экзотермична, поэтому она сопровождается выделением большого количества тепла.
Примером реакции серной кислоты с металлом может служить реакция цинка с серной кислотой. Уравнение реакции можно записать следующим образом:
Zn + H2SO4 → ZnSO4 + H2
В данной реакции цинк (Zn) растворяется в серной кислоте (H2SO4), образуя соль серной кислоты (ZnSO4) и выделяя молекулы водорода (H2). Разность потенциалов между цинком и серной кислотой позволяет происходить реакции обмена электронами и образованию ионов. Эта реакция является типичным примером реакции металла с кислотой и часто используется в химических экспериментах и промышленных процессах.
Список металлов, которые могут реагировать с серной кислотой
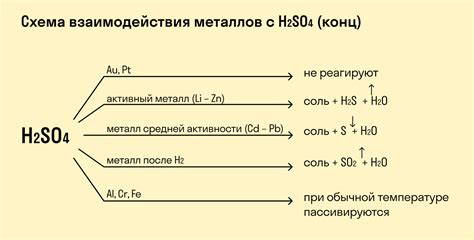
Серная кислота является одним из самых распространенных неорганических кислот и может реагировать с различными металлами. В результате таких реакций образуются соли серной кислоты и выделяется водород.
Ниже приведен список металлов, с которыми серная кислота может реагировать:
- Железо (Fe) - реакция с серной кислотой приводит к образованию соли FeSO4 и выделению водорода (H2).
- Цинк (Zn) - реакция с серной кислотой приводит к образованию соли ZnSO4 и выделению водорода (H2).
- Медь (Cu) - реакция с серной кислотой приводит к образованию соли CuSO4 и выделению водорода (H2).
- Свинец (Pb) - реакция с серной кислотой приводит к образованию соли PbSO4 и выделению водорода (H2).
- Цирконий (Zr) - реакция с серной кислотой приводит к образованию соли Zr(SO4)2 и выделению водорода (H2).
Таким образом, серная кислота может реагировать с различными металлами, образуя соли и выделяя водород. Эти реакции имеют важное применение в различных процессах и промышленности.
Общая информация о реакции

Серная кислота (H2SO4) - это одно из наиболее распространенных сильных минеральных кислот. Она обладает множеством применений в различных отраслях, включая химию, металлургию и производство удобрений.
Реакция серной кислоты с металлом происходит по типу щелочной реакции. При взаимодействии серной кислоты с металлом образуется соль и выделяется водородный газ.
Уравнение реакции между серной кислотой и металлом может быть общего вида:
H2SO4 + M → MSO4 + H2
Где M - металл, а MSO4 - соль металла.
Серная кислота является окислителем в данной реакции. При контакте с металлом, она принимает электроны и превращается из H2SO4 в SO42-. Водород выделяется в виде газа.
Эта реакция может происходить с различными металлами, такими как цинк, железо, медь и т. д. Реактивность металла и скорость реакции зависят от его электрохимического потенциала. Чем ниже потенциал, тем сильнее металл реагирует с серной кислотой.
Уравнение реакции может быть дополнено указанием состояний веществ. Например:
| H2SO4(концентрированная, жидкость) | + | Zn(твёрдое вещество) | → | ZnSO4(растворимая соль, вода) | + | H2(газ) |
Уравнение реакции серной кислоты с щелочными металлами
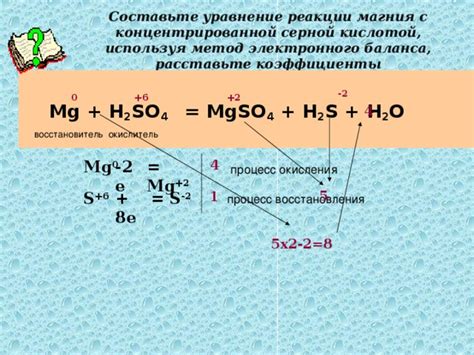
Серная кислота – одна из самых распространенных и важных кислот в химии. Она реагирует со многими веществами, включая металлы. Щелочные металлы, такие как натрий, калий и литий, не являются исключением.
Уравнение реакции серной кислоты с щелочными металлами можно записать следующим образом:
2Na + H2SO4 → Na2SO4 + 2H2
В данном случае, щелочный металл натрий (Na) реагирует с серной кислотой (H2SO4), образуя сульфат натрия (Na2SO4) и выделяя водород (H2).
Подобные реакции можно наблюдать и с другими щелочными металлами, например, с калием (K) или литием (Li). Уравнение реакции будет аналогичным:
- 2K + H2SO4 → K2SO4 + 2H2
- 2Li + H2SO4 → Li2SO4 + 2H2
Такие реакции являются классическими примерами взаимодействия металлов с кислотами и применяются в различных химических процессах и реакциях.
Уравнение реакции серной кислоты с щелочноземельными металлами
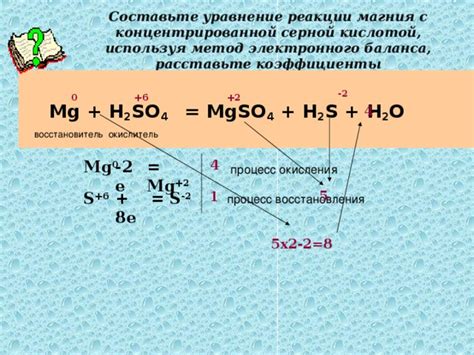
Серная кислота является одной из самых распространенных и химически активных кислот. Она образуется в результате окисления серосодержащих соединений и находит широкое применение в промышленности и научных исследованиях.
Серная кислота может реагировать с щелочноземельными металлами, такими как магний (Mg), кальций (Ca), стронций (Sr) и барий (Ba), образуя соответствующие соли и выделяяся водород. Эти реакции являются химическими окислительно-восстановительными процессами, в которых серная кислота окисляется, а металл восстанавливается.
Уравнение реакции серной кислоты с щелочноземельным металлом может быть представлено следующим образом:
- с серной кислотой (H2SO4) взаимодействует щелочноземельный металл (Mg, Ca, Sr, Ba);
- образуются соль металла (M2SO4) и водород (H2).
Например, уравнение реакции между серной кислотой и магнием выглядит следующим образом:
H2SO4 + Mg → MgSO4 + H2
Эта реакция является экзотермической, то есть сопровождается выделением тепла. При ее проведении необходимо соблюдать осторожность и работать в хорошо проветриваемом помещении, так как серная кислота является ядовитым и коррозионным веществом.
Уравнение реакции серной кислоты с активными металлами

Серная кислота - это одна из самых распространенных кислот, которая обладает сильной реактивностью. Когда она взаимодействует с активными металлами, происходит химическая реакция, которую можно описать уравнением. В результате этой реакции образуются соответствующие соли металлов и выделяется водородный газ.
Например, реакция серной кислоты с железом может быть представлена следующим уравнением:
Fe + H2SO4 = FeSO4 + H2
Здесь Fe обозначает металл железо, H2SO4 - серную кислоту, FeSO4 - соль железа(II) сернокислого, а H2 - водородный газ, который образуется в результате реакции.
Уравнение реакции серной кислоты с активными металлами можно записать обобщенно:
- Metal + H2SO4 = MetalSO4 + H2
Здесь Metal обозначает любой активный металл, который может вступать в реакцию с серной кислотой. MetalSO4 - соль металла и H2 - водородный газ.
Таким образом, уравнение реакции серной кислоты с активными металлами позволяет описать процесс и полученные продукты в результате этой химической реакции.
Вопрос-ответ

Что такое серная кислота?
Серная кислота (H2SO4) — это сильная дипротическая кислота, состоящая из двух атомов водорода, одного атома серы и четырех атомов кислорода. Она является одним из наиболее распространенных и широко используемых химических веществ в промышленности и лабораториях.
Как можно получить серную кислоту?
Серная кислота можно получить путем окисления серы или диоксида серы (SO2). Окисление серы происходит с помощью сильного окислителя, такого как кислород или водородный пероксид. При этом образуется сернистая (H2SO3) или сульфитная (SO3) кислота, которые затем окисляются до серной кислоты с помощью дополнительного кислорода или пероксида.
Что происходит при реакции серной кислоты с металлом?
При реакции серной кислоты с металлом происходит образование соответствующего сульфата металла и выделение водорода. Например, при реакции серной кислоты с железом образуется сульфат железа (FeSO4) и выделяется водород (H2). Это реакция окисления металла кислородом из серной кислоты и одновременно восстановления серной кислоты кислородом из металла.
