Генетический ряд кальция – это последовательность веществ, получаемых путем окисления металлического кальция в воздухе. Оксид кальция (CaO) представляет собой одно из наиболее распространенных оксидов в природе. Это белый кристаллический порошок, не имеющий запаха.
Данный ряд является примером генетической связи между веществами, иллюстрирующей образование и трансформацию различных соединений кальция. Следующее вещество в ряду получается путем окисления предыдущего соединения кальция, и так далее.
Схема металл-основный оксид представляет собой последовательное превращение металла в оксид и последующее реагирование оксида с водой или кислотным раствором, что приводит к образованию соответствующего основания или соли.
В генетическом ряду кальция по схеме металл-основный оксид можно выделить следующие соединения: CaO (оксид кальция), Ca(OH)2 (гидроксид кальция), CaCO3 (карбонат кальция), Ca(NO3)2 (нитрат кальция) и т.д. Каждое последующее соединение в ряду образуется из предыдущего путем взаимодействия с оксидами, кислотами или базами.
Генетический ряд кальция

Генетический ряд кальция представляет собой последовательность химических элементов, которые образуют основные оксиды и реагируют с водой с образованием оснований. Кальций является основным элементом этого ряда и самым распространенным металлом в земной коре.
Последующие элементы ряда – стронций и барий – обладают сходными свойствами с кальцием и также образуют основные оксиды. Они расположены в том же столбце таблицы Менделеева, что и кальций, что говорит о сходстве их свойств.
Генетический ряд кальция демонстрирует увеличение химической активности элементов по мере увеличения их атомных номеров. Также, увеличивается растворимость гидроксидов и сульфатов этих элементов при растворении в воде.
Данный ряд находит применение в химическом анализе для определения присутствия и количества кальция, стронция и бария в различных образцах. Он также помогает в понимании химических свойств и возможных реакций этих элементов.
Металл-основный оксид: значение и применение
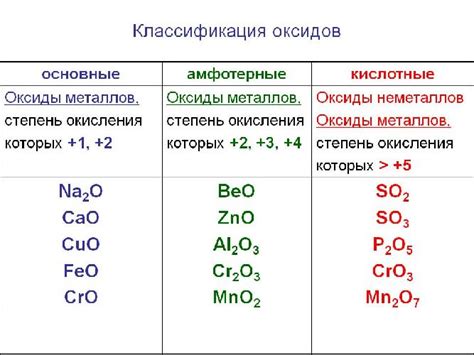
Металл-основный оксид – это химическое соединение, состоящее из металлического катиона и оксидионного аниона. Главной особенностью такого оксида является его щелочная или щелочно-земельная природа. Другими словами, металл-основный оксид способен образовывать щелочные или щелочно-земельные растворы с водой.
Значение металл-основных оксидов заключается в их широком применении в различных отраслях промышленности и науки. Такие оксиды используются в металлургии для получения металлических соединений и сплавов с определенными свойствами. Они также находят применение в производстве керамики и стекла, где используются в качестве важных компонентов.
Благодаря своим химическим и физическим свойствам, металл-основные оксиды применяются в процессе катализа, играя роль активных катализаторов в различных химических реакциях. Они также широко используются в электротехнике, где служат проводниками электричества или используются для создания электролитов в аккумуляторных батареях.
По своей природе металл-основные оксиды могут быть как нерастворимыми, так и растворимыми в воде. Это позволяет использовать их в качестве катализаторов или пигментов в производстве красок и покрытий. Благодаря своей способности давать окрашенный оттенок, металл-основные оксиды находят широкое применение в производстве косметики, текстиля и красителей.
Вопрос-ответ

Зачем нужен генетический ряд кальция по схеме металл-основный оксид?
Генетический ряд кальция по схеме металл-основный оксид нужен для определения реакционной способности кальция с различными оксидами металлов.
Какие сложности могут возникнуть при использовании генетического ряда кальция?
При использовании генетического ряда кальция могут возникнуть сложности с выбором соответствующих оксидов металлов и правильной интерпретацией результатов реакций.
Можно ли использовать генетический ряд кальция для определения реакционной способности других металлов?
Генетический ряд кальция был разработан специально для определения реакционной способности кальция, поэтому он не может быть использован для определения реакционной способности других металлов.
