Металлы - это элементы, которые обладают характерными свойствами, такими как блеск, проводимость тепла и электричества, пластичность и твердость. Они являются одними из основных строительных блоков материи и широко используются в промышленности.
Молекулы простых веществ металлов состоят из атомов, обладающих специфической структурой. В отличие от молекул органических соединений, которые имеют сложную и разнообразную структуру, молекулы металлов отличаются более простой и симметричной организацией.
Основной строительный блок молекулы металла - это атом металла. Атомы металлов имеют отличную от атомов неметаллов структуру, которая обуславливает их специфические свойства. Они характеризуются наличием свободных электронов, которые могут двигаться внутри металлической решетки и образовывать электронное облако вокруг атомов. Благодаря этому, молекулы металлов обладают отличной проводимостью электричества и тепла.
Кроме основного блока, в молекулах металлов могут присутствовать и другие элементы, такие как сплавы и примеси, которые изменяют их свойства и состав. Сплавы представляют собой смеси двух и более металлов, которые образуют новые соединения с особыми свойствами. Примеси могут влиять на структуру молекулы и создавать дополнительные силы взаимодействия между атомами.
В зависимости от состава молекулы и особенностей структуры, металлы могут образовывать различные соединения и структуры. Например, металлы могут образовывать ионные соединения, в которых атомы металла отдают электроны, образуя положительно заряженные ионы. Также металлы могут образовывать ковалентные соединения, в которых атомы металла обмениваются электронами с другими атомами. В результате, молекулы металлов могут обладать различными свойствами и химической активностью.
Молекулы металлов: основные сведения
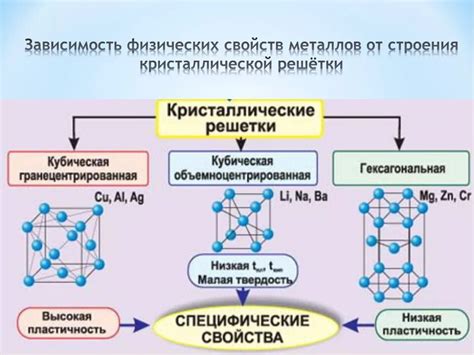
Молекулы металлов - это структурные единицы, составленные из атомов металлов. В отличие от молекул органических соединений, молекулы металлов не образуются путем совместного участия электронов в ковалентной связи. Вместо этого атомы металлов формируют кристаллическую решетку, в которой они образуют связи через общие электронные облака.
Металлы обладают высокой электропроводностью и теплопроводностью, что обусловлено специфическим строением и свойствами их молекул. Атомы металлов могут быть организованы в различные структуры, такие как кубическая решетка граней центрированная решетка и шестиугольная ближайшая упаковка. Различная структура молекулы металла определяет его свойства и способность к образованию сплавов.
Молекулы металлов обычно обладают металлическим блеском и характерным серебристым цветом. Они хорошо проводят ток и тепло благодаря особенностям связи в кристаллической решетке. В металлических молекулах электроны свободно двигаются по всему объему молекулы, что обеспечивает высокую электропроводность. Также, благодаря этому свойству, металлы могут подвергаться формированию и созданию различных структурных материалов.
Одной из характерных особенностей молекул металлов является способность образовывать сплавы. Сплавы представляют собой смеси молекул различных металлов, которые объединяются в однородную структуру. Это свойство обусловлено особенностями связи между атомами металлов и создает возможность для создания материалов с новыми свойствами, в том числе с повышенной прочностью и устойчивостью к коррозии.
Строение молекул металлов
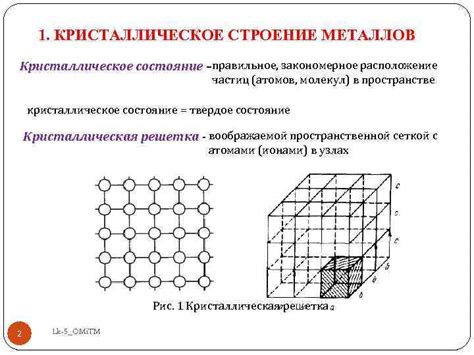
Металлы представляют собой вещества, обладающие высокой электропроводностью и способностью образовывать положительные ионы. Строение молекул металлов отличается от строения молекул других веществ, так как металлические связи обеспечивают особую структуру, называемую кристаллической решеткой.
Кристаллическая решетка состоит из положительных ионов металла, расположенных в упорядоченном и регулярном порядке. Между ионами расположены электроны, которые свободно передвигаются по кристаллической решетке, обеспечивая электропроводность металлов.
Металлические связи сильны и направлены во всех направлениях в кристаллической решетке, что придает металлам их характерные свойства, такие как пластичность и хорошая теплопроводность. Кристаллическая решетка позволяет металлам образовывать различные структуры, такие как слоистые, кубические или гексагональные решетки.
Изучение строения молекул металлов помогает понять их свойства и применение в различных областях. Кроме того, исследования в этой области могут привести к разработке новых материалов и технологий на основе металлов.
Влияние электронной структуры на свойства

Металлы обладают специфическими свойствами, такими как хорошая тепло- и электропроводность, пластичность, малые значения температуры плавления и кипения. Эти уникальные свойства объясняются особым строением электронной оболочки атомов металлов.
В электронной структуре атомов металлов на внешнем энергетическом уровне находятся свободные или легко подвижные электроны, называемые электронами проводимости. Они образуют облако электронов, которое простирается по всему объему металла. Именно благодаря наличию электронов проводимости металлы обладают высокой электропроводностью и теплопроводностью.
Свободные электроны не связаны с конкретными атомами и легко перемещаются под воздействием внешних сил. Это позволяет молекулам металлов двигаться друг относительно друга без значительных столкновений, что дает металлам пластичность и способность принимать определенную форму.
Также, наличие свободных электронов влияет на температуру плавления и кипения металлов. Когда металл нагревается, электроны проводимости поглощают энергию и начинают быстрее двигаться, что повышает температуру, необходимую для перехода вещества из твердого состояния в жидкое и далее в газообразное.
Механизмы образования молекул металлов
Образование молекул металлов осуществляется через образование химических связей между атомами металла. Механизмы образования молекул металлов варьируются в зависимости от свойств каждого конкретного металла, его электронной конфигурации и условий реакции.
Одним из механизмов образования молекул металлов является образование металлической связи. Металлическая связь образуется между атомами металла за счет обмена свободными электронами. Эти электроны перемещаются свободно по кристаллической решетке металла и образуют области отрицательного заряда, окруженные положительными ионами металла. Такой тип связи обеспечивает металлам высокую теплопроводность и электропроводность.
Другим механизмом образования молекул металлов является образование координационных соединений. В координационных соединениях атомы металла образуют с катионами или нейтральными молекулами лигандов структурные единицы, называемые комплексными ионами. Эти структурные единицы могут быть одно-, двух- или многокоординатными. Координационные соединения металлов обладают разнообразными свойствами и могут образовывать различные типы связей, такие как ионные, ковалентные или металлические связи.
Таким образом, образование молекул металлов может происходить через образование металлической связи или образование координационных соединений, в зависимости от свойств каждого конкретного металла и условий реакции. Эти механизмы образования молекул металлов определяют их структуру и свойства.
Возможные состояния молекул металлов
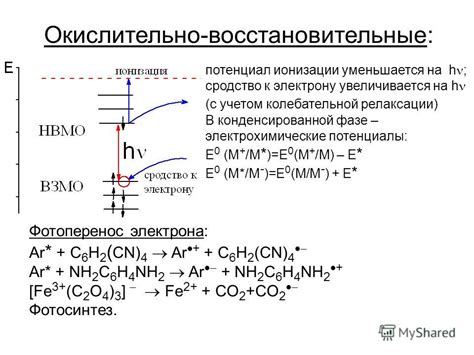
Молекулы металлов имеют специфическое строение и свойства, которые отличаются от молекул органических или неорганических соединений. В отличие от молекул не-металлов, молекулы металлов обычно имеют одну или несколько валентных связей, образованных между атомами металла и другими элементами.
Состояние молекул металлов может быть различным в зависимости от условий внешней среды. Один из возможных вариантов - состояние, при котором молекулы металлов находятся в газообразном состоянии. Это может происходить при высоких температурах, когда молекулы металла испаряются.
Другим возможным состоянием молекул металлов является жидкое состояние. При определенных условиях внешней среды, металлы могут существовать в виде жидких соединений, где молекулы металла находятся в состоянии подвижности и могут перемещаться.
Однако, самым распространенным и стабильным состоянием молекул металлов является твердое состояние. В твердой форме молекулы металлов образуют решетчатую структуру, где атомы металла располагаются в определенном порядке и могут быть связаны с другими элементами или молекулами.
Состав молекул металлов может быть разнообразным и зависит от типа металла и его химических свойств. Например, молекулы железа могут состоять из атомов железа и других элементов, таких как углерод или кислород.
Таким образом, состояние и состав молекул металлов определяют их химические и физические свойства, а также их способность взаимодействовать с другими элементами и соединениями.
Физические и химические свойства

Металлы обладают рядом характерных физических и химических свойств, которые определяют их уникальные свойства и способности. Физические свойства металлов включают высокую теплопроводность и электропроводность, что делает их ценными материалами для использования в проводах и электронных устройствах.
Металлы также обладают высокой пластичностью и прочностью, что позволяет им быть использованными в различных конструкциях и строительных материалах. Они также обладают высокой плотностью и твердостью, что делает их устойчивыми к физическим воздействиям и повышает их долговечность и устойчивость к разрушению.
Химические свойства металлов включают их способность образовывать ионы положительного заряда, что позволяет им образовывать химические соединения с другими веществами. Благодаря этой способности металлы могут образовывать соли и окислы, которые имеют широкий спектр применений в промышленности и химической промышленности.
Одной из важных химических свойств металлов является их реактивность. Металлы могут быть активными или инертными, в зависимости от их способности к реакциям с другими веществами. Некоторые металлы, такие как натрий и калий, очень реактивны и способны взрываться при контакте с водой или кислородом. Другие металлы, такие как золото и платина, более инертны и не вступают в химические реакции с обычными веществами.
Взаимодействие молекул металлов с другими веществами

Металлы, как химически активные элементы, имеют свойства взаимодействовать с различными веществами. Они способны образовывать соединения как с металлическими, так и с неметаллическими элементами. Взаимодействие молекул металлов с другими веществами основано на электронных переходах и обмене зарядами.
Когда металл вступает в реакцию с металлическими элементами, происходит образование сплавов. Сплавы обладают улучшенными механическими и физическими свойствами по сравнению с чистыми металлами. Например, добавление небольшого количества меди в железо приводит к образованию сплава стали, который обладает повышенной коррозионной стойкостью и прочностью.
При взаимодействии металлов с неметаллами происходит образование металлических оксидов или солей. Например, алюминий, реагируя с кислородом, образует оксид алюминия (Al2O3), который является основным компонентом глины. Кроме того, металлы могут реагировать с кислотами, образуя соли и выделяя водород. Например, железо реагирует с соляной кислотой, образуя соль железа(III) хлорида (FeCl3) и выделяя водород.
Взаимодействие металлов с водой также имеет место. Некоторые металлы, например калий или натрий, реагируют с водой, образуя гидроксиды металлов и выделяя водород. Реакции металлов с водой играют важную роль, например, в энергетике для получения водорода, который используется в качестве источника энергии.
Таким образом, взаимодействие молекул металлов с другими веществами является одной из основных характеристик этих элементов. Оно позволяет получать различные соединения металлов, которые имеют широкое применение в различных отраслях промышленности и науки.
Применение молекул металлов в промышленности

Молекулы металлов широко применяются в различных отраслях промышленности благодаря своим уникальным свойствам и химическим характеристикам. Они играют важную роль в процессах производства и используются для создания разнообразных материалов и изделий.
Одно из главных применений молекул металлов – это производство сплавов. Металлы образуют различные сплавы, которые обладают улучшенными свойствами по сравнению с чистыми металлами. Например, добавление небольшого количества другого металла может повысить прочность и твердость сплава, делая его идеальным для использования в машиностроении или строительстве.
Молекулы металлов также используются для создания катализаторов. Катализаторы – это вещества, которые ускоряют химические реакции, не изменяя при этом своей структуры. Металлические катализаторы широко применяются в различных процессах, таких как производство пластмасс, нефтепереработка и синтез полимеров.
Еще одним важным применением молекул металлов является их использование в электронной промышленности. Металлы используются для создания электродов, проводов и контактов. Они обладают отличной электропроводностью и стабильностью, что позволяет им быть надежными и эффективными элементами электронных устройств.
Кроме того, молекулы металлов применяются в процессах поверхностного покрытия. Например, гальваническое покрытие позволяет защитить металлические изделия от коррозии и придать им дополнительные свойства. Молекулы металлов могут быть нанесены на поверхность изделия в виде тонкого слоя, что улучшает его внешний вид, защищает от воздействия окружающей среды и увеличивает срок его службы.
Исследования молекул металлов в современной науке
Современная наука активно исследует молекулы металлов с целью понять их структуру и свойства. Изучение этих молекул важно для развития новых материалов с определенными характеристиками, а также для разработки методов и технологий их синтеза.
Одним из основных методов исследования молекул металлов является рентгеноструктурный анализ. Он позволяет определить точную структуру молекулы, расстояния между атомами и углы связи. Эта информация необходима для понимания механизмов химических реакций, происходящих с участием молекул металлов.
Исследования молекул металлов также проводятся с использованием спектроскопических методов. Например, масс-спектрометрия позволяет определить массу молекулы и идентифицировать атомы, из которых она соcтоит. Инфракрасная спектроскопия позволяет изучать колебательные и вращательные движения молекул, а ультрафиолетовая и видимая спектроскопия - электронные переходы.
Важным направлением исследований молекул металлов является изучение их реакций с другими веществами. Это позволяет выявить возможные реакционные механизмы и оптимизировать условия реакции. Исследование реактивности молекул металлов важно для создания новых катализаторов и прогнозирования их эффективности.
Результаты исследований молекул металлов находят широкое применение в различных областях, включая катализ, электронику, энергетику и медицину. Они позволяют создавать новые материалы с уникальными свойствами, а также улучшать существующие процессы и технологии. Благодаря продолжающимся исследованиям молекул металлов, наука продолжает совершенствовать свои знания о мире химии и расширять возможности применения металлов в различных сферах жизни.
Вопрос-ответ

Какие элементы входят в состав молекул простых веществ металлов?
Молекулы простых веществ металлов обычно состоят из атомов металла. Например, водород Х2, кислород О2.
Чем отличается состав молекул простых веществ металлов от состава других веществ?
В отличие от других веществ, молекулы простых веществ металлов обычно состоят только из атомов одного элемента.
Можно ли встретить молекулы простых веществ металлов, состоящие из нескольких элементов?
В природе очень редко встречаются молекулы простых веществ металлов, состоящие из нескольких элементов. Обычно молекулы простых веществ металлов состоят только из атомов металла.
