Атомные ядра щелочных металлов представляют собой особенную структуру, которая играет важную роль в химических реакциях и физических свойствах этих элементов. Щелочные металлы, такие как литий, натрий, калий и другие, обладают уникальным составом ядра и обуславливают их основные химические и физические свойства.
Атомные ядра щелочных металлов состоят из протонов и нейтронов. Протоны имеют положительный заряд, в то время как нейтроны не имеют заряда. Количество протонов в ядре определяет атомный номер элемента и его положение в периодической системе. Количество нейтронов может варьироваться для разных изотопов щелочных металлов, что приводит к различиям в их массовых числах.
Структура атомного ядра щелочных металлов также включает в себя электроны, которые движутся вокруг ядра на энергетических уровнях. Электроны имеют отрицательный заряд и обеспечивают образование и устойчивость атома. Количество электронов в атоме щелочных металлов также определяет их химические свойства и способность образовывать ионы.
Таким образом, состав атомного ядра щелочных металлов играет ключевую роль в определении их химических и физических свойств. Благодаря этой особенности, щелочные металлы обладают низким плавлением и кипением, хорошей электропроводностью и реактивностью с водой. Понимание структуры и состава атомного ядра щелочных металлов является важным для изучения и исследования их свойств и потенциального использования в различных областях науки и технологий.
Определение щелочных металлов

Щелочные металлы – это элементы химической группы I периодической системы, включающей литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются особыми химическими и физическими свойствами, что делает их уникальными в мире химии.
Наиболее характерной особенностью щелочных металлов является их высокая реактивность, особенно в контакте с водой и кислородом. Они способны заметно реагировать с водой, выделяя горючие газы и образуя щелочные гидроксиды. Кроме того, щелочные металлы обладают высокой электропроводностью и подвержены окислению воздухом.
Состав атомного ядра щелочных металлов представляет собой протоны и нейтроны. Протоны - положительно заряженные частицы, а нейтроны - не имеющие заряда. Отношение количества протонов к нейтронам определяет стабильность атомного ядра щелочных металлов. Например, в ядре лития содержится 3 протона и разное количество нейтронов, в зависимости от изотопа.
В общем, щелочные металлы представляют собой важную группу элементов, которые находят широкое применение в различных областях, включая промышленность, медицину и научные исследования. Их особенности и структура атомного ядра делают их уникальными и интересными для исследования.
Значимость атомного ядра

Атомное ядро является одной из основных составляющих атома и имеет огромную значимость для его структуры и свойств. Оно содержит положительно заряженные протоны и нейтроны, которые обеспечивают оставшуюся массу атома после вычета массы электронов.
Первая и главная значимость атомного ядра заключается в том, что именно заряд ядра определяет химические свойства элементов и их взаимодействие. Заряд ядра определяет электростатическую привлекательную силу, которая держит электроны на определенных орбиталях и обеспечивает формирование химических связей между атомами.
Вторая значимость атомного ядра состоит в том, что именно ядро определяет массу атома. Протоны и нейтроны имеют существенно большую массу, чем электроны, и вносят основной вклад в массу атома. Масса атома влияет на его физические свойства, такие как плотность, температура плавления и кипения, а также на его поведение в химических реакциях.
Кроме того, атомное ядро играет ключевую роль в ядерных реакциях, которые происходят при делении и слиянии ядер. В результате этих реакций высвобождается огромное количество энергии, которая используется в ядерной энергетике, а также в процессе образования звезд и взрыве ядерных бомб.
Состав атомного ядра щелочных металлов

Атомное ядро щелочных металлов состоит из протонов и нейтронов. Протоны - это заряженные частицы, имеющие положительный заряд. Нейтроны не имеют заряда, они нейтральны. Обычно атомное ядро щелочного металла содержит один или два электрона в внешней оболочке.
Количество протонов в атомном ядре определяет химические свойства элемента. Например, атомы лития содержат 3 протона, натрия - 11, калия - 19. Количество нейтронов в ядре может варьироваться для одного и того же элемента, образуя изотопы. Изотопы щелочных металлов обладают различными физическими свойствами, такими как масса и радиоактивность.
Структура атомного ядра щелочных металлов имеет следующие особенности:
- Протоны и нейтроны расположены внутри ядра вблизи друг друга.
- Протоны образуют плотное ядро, которое занимает небольшой объем внутри атома.
- Нейтроны помогают удерживать протоны вместе благодаря силе ядерного взаимодействия.
Состав и структура атомного ядра щелочных металлов играют важную роль в их физических и химических свойствах. Исследование атомного ядра позволяет понять особенности поведения щелочных металлов и применять их в различных областях, таких как энергетика и материаловедение.
Атомы и их составляющие
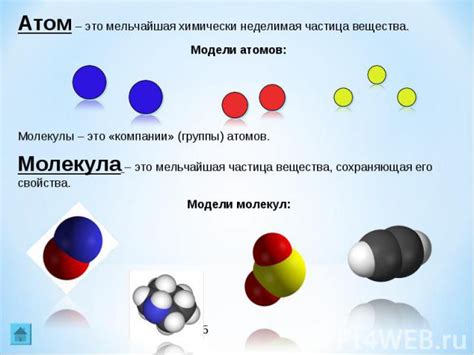
Атом является основной структурной единицей всех веществ. Он состоит из ядра и электронной оболочки.
Ядро атома представляет собой его центральную часть, в которой сосредоточена большая часть его массы. Ядро состоит из протонов и нейтронов, которые называются нуклонами.
Протоны имеют положительный заряд и определяют химические свойства атома. Количество протонов в ядре определяет химический элемент и называется атомным номером.
Нейтроны не имеют заряда и служат для увеличения массы ядра. Они также способствуют стабильности ядра, так как электрический отталкивающий заряд протонов компенсируется.
Электронная оболочка представляет собой область вокруг ядра, где находятся электроны. Электроны обладают отрицательным зарядом и участвуют в химических реакциях между атомами.
Количество электронов в оболочке определяет энергетический уровень атома. На каждом уровне может находиться ограниченное количество электронов:
- На первом уровне может находиться не более 2 электронов.
- На втором и последующих уровнях может находиться не более 8 электронов.
Таким образом, атомы щелочных металлов имеют один электрон во внешней оболочке, что делает их химически активными и склонными к образованию ионов.
Протоны и нейтроны
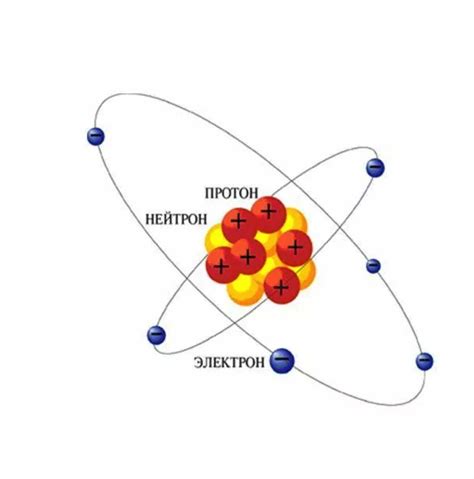
Атомное ядро щелочных металлов состоит из протонов и нейтронов. Протоны - это положительно заряженные частицы, которые находятся в ядре атома. Они имеют массу примерно равную массе нейтрона и образуют основу ядра. Количество протонов в ядре определяет химические и физические свойства элемента. Например, у калия в ядре находится 19 протонов.
Вместе с протонами в ядре находятся нейтроны. Нейтроны - это нейтральные частицы, не имеющие заряда. Они также имеют массу примерно равную массе протона и способствуют стабильности ядра. Количество нейтронов в ядре может быть разным и определяет изотопы элемента. Например, у калия существуют изотопы с разным количеством нейтронов - 39K и 41K.
Протоны и нейтроны в ядре взаимодействуют друг с другом с помощью сильного ядерного взаимодействия. Это взаимодействие помогает объединить и удерживать эти частицы вместе в ядре. Кроме того, оба типа частиц являются фермионами, что означает, что они подчиняются принципам квантовой механики, таким как принцип Паули.
Изотопы щелочных металлов
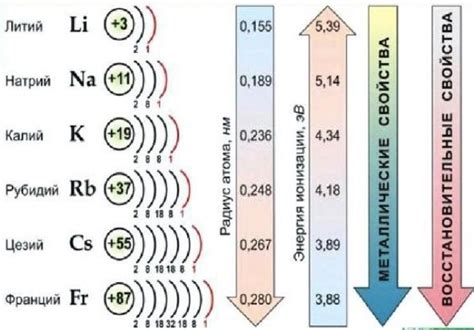
Щелочные металлы - это элементы первой группы периодической системы, которые включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). В атомах щелочных металлов обычно преобладает один стабильный изотоп, наиболее распространенный из которых - литий-7 (7Li), натрий-23 (23Na) и калий-39 (39K).
Однако, помимо стабильных изотопов, у щелочных металлов существуют и радиоактивные изотопы. Например, у лития имеются два радиоактивных изотопа: литий-6 (6Li) и литий-8 (8Li), оба из которых нестабильны и распадаются со временем.
У натрия также есть два радиоактивных изотопа: натрий-22 (22Na) и натрий-24 (24Na). Радиоактивные изотопы щелочных металлов чаще всего используются в медицинских и научных исследованиях, так как они обладают свойством излучать радиацию, что позволяет использовать их для различных исследовательских целей.
Радиоактивные изотопы щелочных металлов имеют свои характеристики и особенности. Они имеют короткий период полураспада, что означает, что они быстро распадаются и превращаются в другие элементы. Это делает их нестабильными и опасными для использования в бытовых условиях. Однако, благодаря своим свойствам они играют важную роль в медицине, промышленности и научных исследованиях.
Структура атомного ядра щелочных металлов
Атомные ядра щелочных металлов, таких как литий, натрий, калий и др., имеют свою особенную структуру. Они состоят из протонов и нейтронов, которые называются нуклонами. Протоны являются положительно заряженными частицами, в то время как нейтроны не имеют заряда.
В атомном ядре каждый щелочный металл имеет определенное количество протонов, которое определяет его атомный номер. Например, литий имеет атомный номер 3, а натрий - 11. Количество нейтронов в атомном ядре может отличаться, и это определяет изотопы щелочных металлов.
Структура атомного ядра щелочных металлов также может быть представлена в виде ядерной модели. В этой модели протоны и нейтроны образуют атомное ядро, которое находится в центре атома. Вокруг ядра находятся электроны, движущиеся по энергетическим уровням или оболочкам.
Важно отметить, что структура атомного ядра щелочных металлов имеет влияние на их физические и химические свойства. Например, щелочные металлы хорошо растворяются в воде, потому что их атомы имеют низкую энергию и высокий радиус, что облегчает взаимодействие с водными молекулами.
Внутренняя структура ядра
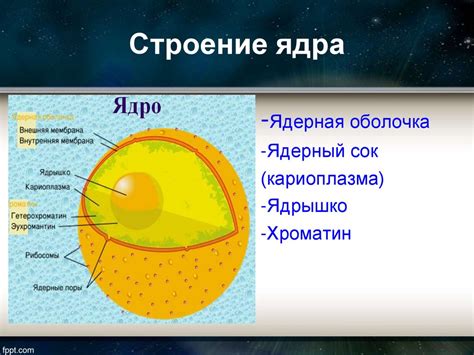
Атомное ядро щелочных металлов состоит из протонов и нейтронов. Протоны - это элементарные частицы, имеющие положительный электрический заряд. Нейтроны же не имеют заряда и являются нейтральными.
У щелочных металлов в ядре обычно преобладает число протонов над числом нейтронов, что обуславливает положительный заряд атомного ядра. Этот положительный заряд компенсируется наличием отрицательно заряженных электронов в атомной оболочке, что, в конечном счете, делает атом электрически нейтральным.
Структура ядра щелочных металлов также характеризуется его размерами и массой. Масса атомного ядра определяется суммой масс протонов и нейтронов, а его размеры составляют порядка нескольких фемтосекунд (10^-15 метров).
Важно отметить, что внутри ядра происходят сложные взаимодействия между протонами и нейтронами, атомное ядро щелочных металлов может испытывать различные изменения. Некоторые изотопы щелочных металлов могут быть нестабильными и подвергаться радиоактивному распаду.
- Структурные особенности ядра:
- Состоит из протонов и нейтронов;
- Происходят сложные взаимодействия;
- Изменения и радиоактивный распад.
- Масса определяется суммой масс протонов и нейтронов;
- Размеры составляют несколько фемтосекунд.
Сложность структуры ядра
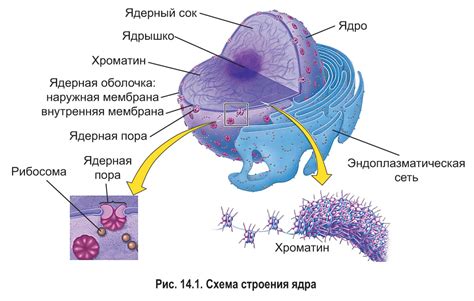
Ядра атомов щелочных металлов, таких как литий, натрий, калий и др., характеризуются сложной структурой, которая обусловлена особенностями их состава.
Основными составляющими ядра являются протоны и нейтроны. Протоны, обладая положительным зарядом, определяют атомный номер и химические свойства элемента. Нейтроны не имеют заряда и служат стабилизирующим импульсом для ядра.
Структура ядра щелочных металлов может быть представлена в виде таблицы, где указывается количество протонов, нейтронов и электронов для каждого элемента. Также можно использовать визуальные модели и схемы, иллюстрирующие расположение и взаимодействие частиц внутри ядра.
Стоит отметить, что сложность структуры ядра щелочных металлов обусловлена не только количеством его составляющих частиц, но и их взаимодействием и организацией внутри ядра. Такая сложность требует тщательного исследования и анализа для полного понимания физических и химических свойств данных элементов.
Взаимодействие частиц внутри ядра
Атомное ядро щелочных металлов состоит из протонов и нейтронов. Внутри ядра происходят различные взаимодействия между этими частицами, определяющие его устойчивость и свойства.
Основным взаимодействием, определяющим структуру ядра, является притяжение между протонами и нейтронами - ядерная сила. Она обеспечивает сцепление этих частиц внутри ядра и позволяет ему существовать в устойчивом состоянии.
Протоны обладают положительным зарядом и отталкиваются друг от друга электростатическим взаимодействием, но их удерживает ядерная сила. Нейтроны не имеют заряда, поэтому их взаимодействие с другими нейтронами и с протонами также осуществляется через ядерную силу.
Внутри ядра также происходят процессы ядерного распада, при которых происходит изменение состава ядра. Эти процессы могут быть спонтанными или вызванными, и они часто сопровождаются выбросом альфа- и бета-частиц.
Взаимодействие частиц внутри ядра обусловливает его свойства, такие как масса, заряд, спин и изотопический состав. Понимание этих взаимодействий позволяет исследовать ядра щелочных металлов и использовать их в различных приложениях, включая ядерную энергетику и промышленность.
Вопрос-ответ

Какова структура атомного ядра щелочных металлов?
Атомное ядро щелочных металлов состоит из протонов и нейтронов. Все щелочные металлы имеют одно электронное облако, полностью заполняющее внешнюю энергетическую оболочку.
Что представляют собой протоны и нейтроны в составе атомного ядра щелочных металлов?
Протоны - это положительно заряженные элементарные частицы, которые находятся в ядре атома. Они определяют химические свойства элемента. Нейтроны - это нейтральные элементарные частицы, они также находятся в ядре атома и не имеют электрического заряда.
Почему атомное ядро щелочных металлов состоит из протонов и нейтронов?
Протоны и нейтроны необходимы для стабилизации атомного ядра щелочных металлов. Протоны, имеющие положительный заряд, удерживают нейтроны, обеспечивая ядру достаточную силу притяжения. Нейтроны же помогают снизить отталкивающее воздействие между протонами и обеспечивают стабильность атомного ядра.
