Соли щелочных металлов: особенности и свойства Na2CO3
Na2CO3, известная также как карбонат натрия или сода, является одной из наиболее распространенных солей щелочных металлов. Она применяется во множестве отраслей промышленности и быта, благодаря своим уникальным свойствам и особенностям.
Сода является белым кристаллическим веществом, хорошо растворимым в воде. Она имеет щелочную реакцию и широко используется в качестве основного компонента многих моющих средств и средств для борьбы с запахами. Карбонат натрия также используется в производстве стекла, бумаги, мыла и других промышленных продуктов.
Одним из самых интересных свойств Na2CO3 является ее способность к превращению насыщенных растворов в щелочную или кислотную среду. Например, при нагревании соды она разлагается на два компонента: карбонат натрия и оксид углерода. Это свойство делает Na2CO3 очень полезным в промышленности и быту.
Щелочные металлы и их соли
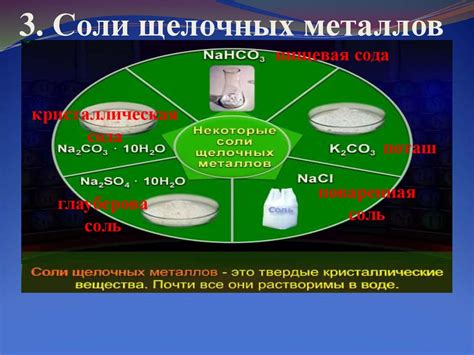
Щелочные металлы являются элементами первой группы периодической таблицы химических элементов. В эту группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются высокой реактивностью, низкой плотностью и низкой температурой плавления и кипения.
Щелочным металлам свойственно образование солей с кислотами. Соли щелочных металлов обладают определенными свойствами и особенностями. Например, натриевая соль, называемая также пищевой содой (Na2CO3), широко используется в пищевой промышленности в качестве пищевой добавки E500. Она используется для придания пищевым продуктам щелочной реакции, регулирования кислотности и улучшения технологических свойств продуктов.
Соли щелочных металлов широко применяются в промышленности и научных исследованиях. Например, калиевые соли используются в удобрениях для повышения урожайности сельскохозяйственных культур. Кроме того, соли щелочных металлов используются в производстве стекла, мыла, моющих средств, лекарственных препаратов и других продуктах. Они также играют важную роль в биологических процессах организма, в том числе в регуляции водно-солевого баланса и функционировании нервной системы.
Онлайн автоматизированная система помощника может предоставить больше сведений о соли щелочных металлов, особенностях и свойствах, таких как растворимость, кристаллическая структура и реактивность. Она также может помочь в определении применения их солей в различных сферах промышленности и научных исследованиях.
Химическая формула и свойства Na2CO3
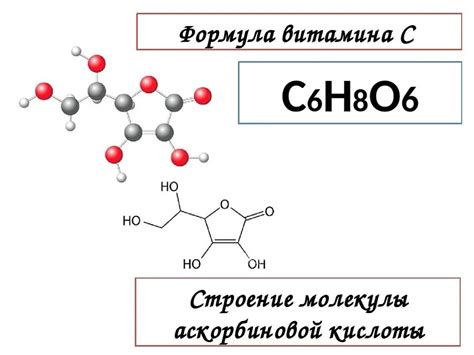
Химическая формула Na2CO3 обозначает химическое соединение натрия с углекислым ангидридом. Также известное как сода Нера или кристаллическая сода, это белые кристаллы или порошок с щелочным вкусом.
Na2CO3 обладает несколькими химическими свойствами, которые делают его полезным в различных областях. Одно из основных свойств - это его щелочность. Оно может реагировать с кислотами, образуя соль и выделяя углекислый газ.
Na2CO3 также обладает амфотерными свойствами, то есть может проявлять как щелочные, так и кислотные свойства в разных условиях. В щелочных условиях оно реагирует с кислотами, а в кислотных условиях оно может быть ионизировано и выделять гидроксид натрия.
Это соединение также хорошо растворимо в воде и может притягивать влагу из воздуха. Оно также способно абсорбировать углекислый газ. Кроме того, Na2CO3 может быть использовано в процессе выработки стекла, производства моющих средств и при очистке воды от жесткости.
В целом, Na2CO3 имеет разнообразные свойства, которые делают его важным соединением во многих промышленных и хозяйственных процессах.
Применение и использование Na2CO3

Na2CO3, более известное как пищевая или техническая сода, широко применяется в различных отраслях и областях. Ее многочисленные свойства делают ее полезным и востребованным веществом.
Одним из важных применений Na2CO3 является его использование в пищевой промышленности. Сода используется в качестве пищевой добавки – регулятора кислотности, стабилизатора и загустителя в разработке различных продуктов. Она может использоваться для регулирования кислотности в приготовлении кондитерских изделий, напитков, сыров и многих других продуктов.
В технической сфере Na2CO3 также широко применяется. Его использование связано с его свойствами как щелочного вещества. Сода может использоваться в качестве очистителя поверхностей, размораживателя, регулятора pH и дезинфектанта. Она может быть использована для удаления жиров, загрязнений и накипи с различных поверхностей.
Еще одно применение Na2CO3 включает его использование в процессе производства стекла и стекловолокна. Сода используется для стабилизации, обезопасивания и улучшения качества стекла. Стекловолокно, полученное при использовании Na2CO3, обладает высокими механическими и химическими свойствами, что позволяет его использовать в различных отраслях, включая строительство и автомобильную промышленность.
В окружающей среде Na2CO3 может быть использована в качестве нейтрализатора кислотных веществ и даже как компонент в процессе очистки воды. Она может быть также использована для контроля уровня pH в воде и снижения содержания хлора и других загрязнений.
Вопрос-ответ

Какие особенности и свойства имеют соли щелочных металлов, в частности Na2CO3?
Соли щелочных металлов, такие как Na2CO3 (натрий карбонат), обладают рядом особенностей и свойств. Они обычно растворяются в воде и образуют щелочные растворы. Натрий карбонат является белым кристаллическим веществом, которое образует моноклинные кристаллы. Он довольно хорошо растворяется в воде и способен реагировать с кислотами, образуя соли и выделяя углекислый газ.
Какие применения имеет Na2CO3?
Na2CO3 (натрий карбонат) имеет широкое применение в различных отраслях. Он используется в стекольной промышленности, для производства мыла и моющих средств, а также в производстве бумаги и текстиля. Также натрий карбонат применяется в пищевой промышленности как регулятор кислотности, и его используют в качестве отбеливателя и очистителя в бытовых условиях.
Какое влияние оказывает Na2CO3 на окружающую среду?
Na2CO3 (натрий карбонат) не является сильным загрязнителем окружающей среды. Он не является токсичным и его можно безопасно использовать, однако его концентрация в воде или почве может повлиять на ее химическое состояние и pH. Поэтому при использовании натрия карбоната в больших количествах необходимо учитывать его влияние на окружающую среду и принимать соответствующие меры для минимизации негативного воздействия.
Какие побочные эффекты может вызвать Na2CO3?
Использование Na2CO3 (натрий карбоната) может вызвать некоторые побочные эффекты. Внешнее воздействие карбоната натрия на кожу или слизистые может вызвать раздражение или аллергическую реакцию. При прямом попадании в глаза он может вызвать ожоги или раздражение. Поэтому при работе с карбонатом натрия необходимо соблюдать меры предосторожности и использовать защитные средства.
