Соль является одним из важнейших классов соединений в химии металлов. Она имеет широкий спектр связей с металлами и играет ключевую роль в множестве реакций. Благодаря своим уникальным свойствам, соль находит применение во многих сферах жизни, начиная от промышленности и заканчивая медициной и пищевой промышленностью.
В химии металлов соль образуется при реакции металла с кислотой или основанием. Обычно соль состоит из положительного и отрицательного ионов, где положительным ионом является металл, а отрицательным - анион от кислоты или основания. Эти ионы образуют кристаллическую решетку, которая обладает определенными свойствами, такими как растворимость, температура плавления, проводимость электричества и другие химические и физические свойства.
Важно отметить, что ионы соли обладают определенной полярностью, что влияет на их способность реагировать с другими веществами. Металлы имеют большой интерес в связи с их электропроводностью и реакционной способностью. Ионы металлов в соли могут образовывать комплексные соединения с другими реагентами, что позволяет использовать соли для получения различных продуктов, таких как лекарства, пигменты для красок, катализаторы и другие вещества.
Значение соли в химии металлов: связи, реакции и применение
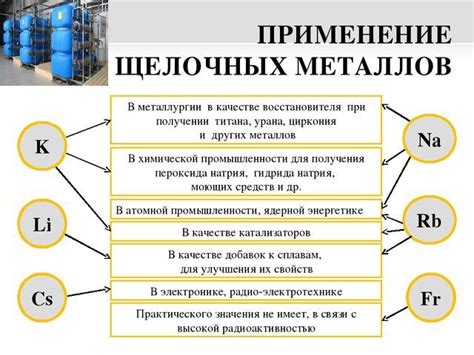
Соль является важным компонентом в химии металлов. Она играет роль связующего элемента, образуя ионные связи между металлами и не металлами. Ионы металлов обладают положительным зарядом, в то время как ионы не металлов имеют отрицательный заряд. Эта электростатическая связь между ионами обеспечивает стабильность соединений металлов и их реактивность в различных химических процессах.
Реакция солей с металлами происходит путем обмена ионов. Соли, распадаясь на ионы, могут реагировать с металлами, образуя новое соединение. Эти реакции могут быть экзотермическими или эндотермическими процессами, которые могут протекать с выделением или поглощением энергии соответственно.
Применение солей в химии металлов включает их использование в качестве катализаторов, жидкостей охлаждения и смазок. Например, соли металлов, такие как хлориды, используются как катализаторы в различных процессах, таких как производство пластмасс и фармацевтических препаратов.
Благодаря своим физическим и химическим свойствам, соли металлов также находят широкое применение в промышленности. Они используются в гальванических процессах, при производстве металлов и сплавов, а также в производстве стекла и керамики. Соли металлов также применяются в медицине и косметологии, где они используются в процессе изготовления лекарственных препаратов и косметических средств.
В заключение, соль играет существенную роль в химии металлов. Она участвует в образовании ионных связей и обеспечивает стабильность соединений металлов. Реакции солей с металлами позволяют получать новые соединения, а применение солей металлов в различных отраслях промышленности обеспечивает их широкое использование и важность в современном обществе.
Роль соли в образовании и разрушении связей между металлами

Соли играют важную роль в образовании и разрушении связей между металлами. Одним из механизмов, при котором соли участвуют в формировании связей между металлами, является образование комплексных соединений. Комплексные соединения являются структурными единицами, в которых металлы связаны с другими атомами или молекулами через ковалентные или ионные связи.
Соли также могут быть использованы для разрушения связей между металлами в процессе химических реакций. Например, некоторые соли могут обладать сильными окислительными свойствами и быть способными окислять металлы до ионов. Это приводит к разрушению связи между атомами металла и образованию ионов металла в растворе соли.
Соли также могут служить в качестве катализаторов для разрушения связей между металлами. Катализаторы - это вещества, которые ускоряют химические реакции, не расходуясь при этом. Некоторые соли могут быть эффективными катализаторами для реакций, в которых происходит разрушение связей между металлами.
В конечном счете, роль соли в образовании и разрушении связей между металлами зависит от их химического состава и структуры. Соли могут быть использованы в различных процессах и реакциях, имеющих практическое значение в различных областях, таких как металлургия, электрохимия и катализ.
Взаимодействие соли с металлами: реакции и образование комплексов

Соли играют важную роль в химии металлов, так как они могут вступать в реакции с металлами и образовывать комплексы. Комплексы – это химические соединения, состоящие из центрального ионного металлического комплекса, который связан с одним или несколькими лигандами.
В результате взаимодействия соли с металлом возможно образование различных типов комплексов, таких как октаэдрические, квадратно-плоскостные или тетраэдрические комплексы. Эти комплексы обладают уникальными свойствами и могут использоваться в различных областях, например в катализе, нанотехнологиях или в медицине.
В процессе образования комплекса соль вступает в реакцию с металлом, где одни из ее ионов координируются к металлическому иону, образуя так называемую координационную сферу. Часто в состав комплексов входят различные лиганды – молекулы или ионы, которые образуют координационные связи с металлом.
Существует множество реакций, которые могут привести к образованию комплексов с металлами. Некоторые из таких реакций включают замещение или обмен лигандов, координационную полимеризацию или комплексообразование с образованием ионных связей. Эти реакции могут быть использованы для синтеза новых соединений с желаемыми свойствами.
Применение солей в металлургии и металлообработке

Соли играют важную роль в металлургии и металлообработке, применяясь для различных процессов и реакций.
Одним из основных способов использования солей в металлургии является процесс флотации. Соли, такие как сульфаты меди и свинца, добавляются в руду для ее обогащения и разделения на полезные компоненты. Они способствуют образованию пенообразного слоя на поверхности рудных частиц, что облегчает их отделение от нежелательных примесей.
Кроме того, соли широко используются в процессе гальванизации, которая позволяет покрыть металлические изделия тонким слоем другого металла. В этом процессе соль выборочно разлагается в электрохимической ячейке, образуя металлическое покрытие на поверхности изделия.
Соли также применяются в качестве флюсов, которые снижают температуру плавления металлов и способствуют равномерному распределению тепла. Флуокалиевая соль, например, используется при сварке и пайке, чтобы обозначить и защитить сварочный шов.
Для удаления загрязнений с металлических поверхностей также используются соли. Ацетат натрия, аммиак и некоторые другие соли применяются для очистки металлов от ржавчины, окислов и прочих загрязнений.
Таким образом, применение солей в металлургии и металлообработке является незаменимым для проведения различных процессов и обработки металлических материалов.
Соль в качестве катализатора реакций металлов
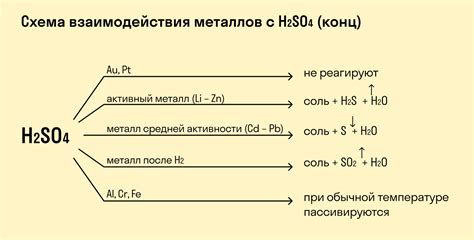
Соль играет важную роль в химических реакциях металлов в качестве катализатора. Катализаторы - это вещества, которые ускоряют химические реакции, не расходуясь при этом. Соль способна влиять на скорость реакции, образование промежуточных соединений, а также на выборочность реакций.
Каталитическое действие соли может проявляться в различных реакциях металлов. Например, соль может ускорять окисление металла, увеличивая скорость образования соответствующего окиси. Также соль может способствовать процессам диспергирования металлических частиц, что приводит к увеличению поверхности реакции и, соответственно, ускорению процесса.
Кроме того, соль может помочь в выборочных реакциях металлов, когда необходимо получить определенное соединение из смеси различных металлических компонентов. Соль может способствовать образованию определенных межметаллических соединений или оказывать влияние на разделение компонентов.
В промышленности соль также широко используется в качестве катализатора реакций металлов. Например, в процессе гидрогенирования соли никеля и палладия часто применяются в качестве катализаторов для образования сырья для производства пластиков и лекарственных препаратов.
Роль соли в качестве электролита для электролиза и гальванических процессов
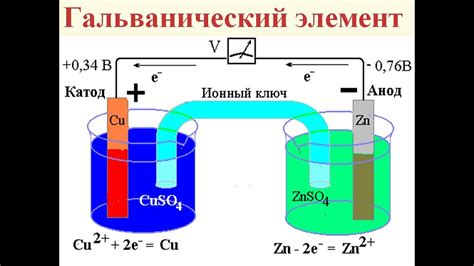
Соли играют важную роль в химии металлов, так как они способны выступать в качестве электролитов при электролизе и гальванических процессах. Электролиты – это вещества, способные проводить электрический ток. При электролизе соли распадаются на ионы и переносят ток через раствор. Этот процесс является основой для получения различных металлов и проведения химических реакций.
Электролиты на основе солей широко используются в промышленности. Например, при производстве алюминия применяется электролиз раствора глиноземного фторида в криолите – соли алюминия и кальция. В результате электролиза получают чистый алюминий и фтор. Также соли используются для проведения гальванических (батарейных) процессов, например, в аккумуляторах, где происходит преобразование химической энергии в электрическую.
Важно отметить, что для эффективного электролиза и гальванических процессов необходимо правильно подобрать электролит. Зависимость эффективности электролиза от свойств соли могут использовать при разработке новых методов получения металлов или улучшении эффективности батарейных систем.
Соль в качестве консерванта и добавки в металлические сплавы

Соль является важным консервантом и добавкой в металлических сплавах. Ее применение обусловлено ее физико-химическими свойствами, которые обеспечивают стабильность и защиту металлов от окисления и коррозии.
Одно из основных свойств соли - ее способность вступать в реакцию с кислородом воздуха и воды. Благодаря этому, соль препятствует окислению и коррозии металлов, сохраняя их в исходном состоянии на протяжении длительного времени.
Кроме того, соль также способствует укреплению металлических сплавов, повышая их прочность и устойчивость к воздействию различных внешних факторов. Она может использоваться как добавка для изменения микроструктуры сплава и повышения его термической стабильности.
Одним из часто используемых методов применения соли в металлургии является использование соляных растворов для обработки поверхностей металлических изделий перед их покрытием. Это позволяет очистить поверхность металла от загрязнений и окисленных слоев, а также создать оптимальные условия для нанесения покрытия.
Таким образом, соль играет важную роль в обработке и защите металлических сплавов. Ее использование позволяет сохранить металлы в исходном состоянии, повысить их прочность и стабильность, а также обеспечить качественное нанесение покрытий.
Вопрос-ответ

Что такое соль в химии металлов?
Соль в химии металлов представляет собой химическое соединение, состоящее из катиона металла и аниона, обычно неметалла или группы неметаллов. Соли играют важную роль в химии металлов, так как они являются основными продуктами окисления металлов, а также могут использоваться в различных реакциях и применениях.
Какие связи образуются в соли металлов?
В соли металлов образуются ионные связи. Катион металла и анион неметалла или группы неметаллов притягиваются друг к другу с помощью электростатических сил. Катион обычно является положительно заряженным, так как он теряет один или несколько электронов, а анион - отрицательно заряженным, так как он получает один или несколько электронов. Эти связи являются крепкими и характерными для солей.
