Натрий — щелочной металл, который является одним из основных элементов в периодической системе. Он обладает атомным номером 11 и химическим символом Na. Натрий является очень реактивным элементом и прочно входит в состав многих соединений, которые играют важную роль в различных отраслях промышленности и научных исследованиях.
Соединения натрия имеют широкий спектр применений. Например, натрий образует соль, которая является важным пищевым продуктом и используется в кулинарии для добавления вкуса и сохранения пищевых продуктов. Натрий также является необходимым компонентом многих стеклостекольных материалов, таких как окна и посуда. Кроме того, соединения натрия используются в производстве щелочных батарей, моющих средств, и средств для очистки воды и сточных вод.
Одним из наиболее известных соединений натрия является гидроксид натрия, или щелочь. Это очень сильная щелочь, которая широко используется в производстве мыла, бумаги, стекла и других продуктов. Также гидроксид натрия используется для регулирования pH-уровня в бассейнах и аквариумах.
Натрий является неотъемлемым элементом живых организмов, и его наличие в организме человека имеет большое значение для нормального функционирования органов и систем. Однако, избыток натрия в организме может привести к различным заболеваниям, включая гипертонию и заболевания сердечно-сосудистой системы. Поэтому важно следить за уровнем потребления натрия и обеспечивать его достаточное количество для поддержания здоровья.
Физические свойства натрия

Натрий - мягкий металл серебристо-белого цвета, характеризующийся хорошей пластичностью и проводимостью электричества.
Точка плавления натрия составляет около 98 градусов Цельсия, а точка кипения - около 883 градусов Цельсия.
Натрий имеет плотность примерно равную 0,97 г/см³ и малую твердость, что делает его достаточно мягким для резки ножом.
При комнатной температуре натрий сохраняет металлический блеск, однако, при длительном контакте с воздухом, на его поверхности образуется оксидный слой.
Одной из интересных особенностей натрия является его способность активно взаимодействовать с водой, в результате чего образуется водород и образуется раствор щелочи – гидроксида натрия.
Натрий является важным минералом в питании человека, играет значимую роль в водно-солевом обмене организма и участвует в регуляции кислотно-щелочного баланса.
Химические свойства натрия

Натрий (Na) – алкалийный металл, имеющий химическую природу, отличающуюся от других элементов периодической системы. Его химические свойства делают его очень реакционноспособным элементом.
На воздухе натрий быстро окисляется, покрываясь белой пленкой оксида, что делает его легко горючим материалом, вызывая яркий оранжевый пламя. При этом образуется оксид натрия (Na2O), который растворяется в воде, образуя щелочное растворение.
Щелочные свойства натрия делают его одним из ключевых элементов в производстве щелочей и щелочных металлов. Натрий способен реагировать с водой, образуя гидроксид натрия (NaOH), являющийся основой широко используемого щелочного раствора.
Соли натрия являются основными считывающими элементами в ряде аналитических методов и тестов. Они имеют широкое применение в пищевой промышленности, фармацевтике и других отраслях.
Взаимодействие с другими элементами основано на способности натрия передавать свой электрон. Большинство соединений натрия являются ионными и имеют высокую растворимость в воде.
Комплексообразующие свойства натрий проявляет в соединениях с положительно заряженными металлами, формируя стабильные комплексы. Важными примерами являются натрий-калиевая и натрий-серебряная пары, используемые в лазерной технологии.
Реакция натрия с кислотами приводит к выделению водорода и образованию солей натрия. Эта реакция является классическим примером нейтрализации. Натрий широко используется в промышленности для производства различных солей, таких как хлорид натрия (NaCl) и серной кислоты (Na2SO4).
Важные соединения натрия

Гидроксид натрия (NaOH) – это одно из важнейших соединений натрия. Оно известно также под названием щелочь и шишковатка. Гидроксид натрия представляет собой белый кристаллический порошок, хорошо растворимый в воде. Он используется в различных областях, включая производство бумаги, текстиля и мыла, очистку пищевых продуктов, а также в химической промышленности.
Карбонат натрия (Na2CO3) – еще одно важное соединение натрия. Оно представляет собой белые кристаллы или порошок, растворимый в воде. Карбонат натрия широко используется в различных отраслях промышленности, таких как стекольная, химическая и металлургическая. Он также применяется в бытовых целях, например, для мягкой очистки посуды и стирки.
Хлорид натрия (NaCl) – наиболее известное соединение натрия. Оно представляет собой белую кристаллическую соль, хорошо растворимую в воде. Хлорид натрия используется в качестве пищевой добавки и консерванта, а также в промышленности для производства хлора, соды и других химических веществ.
Нитрат натрия (NaNO3) – еще одно важное соединение натрия. Оно представляет собой белые кристаллы или порошок, растворимый в воде. Нитрат натрия используется в сельском хозяйстве в качестве удобрения, а также в производстве взрывчатых веществ и стекла.
Фосфат натрия (Na3PO4) – важное соединение натрия, которое представляет собой белый порошок или кристаллы, хорошо растворимые в воде. Фосфат натрия используется в медицине, пищевой промышленности и производстве моющих средств.
Кроме перечисленных соединений, натрий может образовывать и другие важные составные части различных материалов и продуктов, играя значительную роль в химической и промышленной сферах.
Применение натрия и его соединений
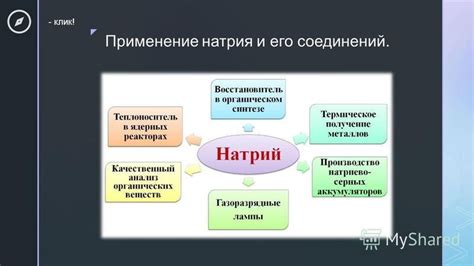
Натрий широко применяется в различных отраслях промышленности и науки благодаря своим уникальным свойствам. В первую очередь натрий используется в производстве химических соединений и сплавов. Он является важным компонентом при производстве стекла, мыла, моющих средств и лекарственных препаратов.
Натрий также применяется в электроэнергетике и батарейной промышленности. Он используется в качестве одной из составляющих аккумуляторных батарей, а также в процессе создания ионных проводников и электролитов для электролитических источников энергии.
В пищевой промышленности натрий играет важную роль в качестве консерванта и регулятора кислотности. Он используется для усиления вкусовых качеств и продления срока годности продуктов. Однако, употребление больших количеств натрия может быть вредным для здоровья, поэтому важно следить за его потреблением.
Кроме того, натрий находит применение в металлургии и производстве алюминия. В виде сплавов с другими металлами, такими как калий, литий и магний, натрий используется для улучшения свойств материалов, повышения их пластичности и прочности.
В заключение, натрий и его соединения являются важными компонентами в различных сферах промышленности и науки. Благодаря своим химическим и физическим свойствам, натрий играет важную роль в производстве химических соединений, стекла, моющих средств, аккумуляторов и продуктов питания. Необходимо учесть, что правильное использование натрия и его соединений является важным аспектом для обеспечения безопасности и качества получаемых продуктов.
Последствия использования натрия
1. Повышенное кровяное давление: Высокое содержание натрия в рационе может способствовать повышению кровяного давления. Это может повлечь за собой различные сердечно-сосудистые заболевания, такие как инсульт и сердечный приступ.
2. Ухудшение функции почек: Натрий может вызывать задержку воды в организме, что может приводить к проблемам с почками. Постоянное потребление жидкостей с высоким содержанием натрия может увеличить риск развития заболеваний почек и способствовать образованию камней в них.
3. Остеопороз: Избыточное потребление натрия может вызвать потерю кальция из костей, что приводит к развитию остеопороза. Это может привести к ухудшению костной массы и повышению риска различных переломов.
4. Желудочно-кишечные нарушения: Избыточное потребление натрия может спровоцировать различные проблемы со здоровьем ЖКТ. Это может включать в себя запоры, изжоги, вздутие живота и необычные стулы.
5. Риск развития диабета: Потребление натрия в больших количествах может увеличить риск развития диабета. Некоторые исследования связывают повышение уровня натрия в организме с ухудшением чувствительности к инсулину и повышенным уровнем сахара в крови.
Итак, хотя натрий является неотъемлемым элементом для нормальной работы организма, излишнее потребление этого элемента может привести к серьезным последствиям для здоровья. Рекомендуется соблюдать балансированную диету и ограничивать потребление продуктов, богатых натрием, чтобы минимизировать риск развития различных заболеваний и нарушений в организме.
Вопрос-ответ

Какие соединения образует натрий?
Натрий образует различные соединения, такие как натриевый хлорид (NaCl), натриевый карбонат (Na2CO3), натриевая гидроксид (NaOH) и другие. Все они имеют различные свойства и применения.
Для чего используется натрий?
Натрий имеет множество применений. Например, натриевый хлорид (обычная кухонная соль) используется в кулинарии для улучшения вкуса пищи. Натриевый карбонат (пищевая сода) используется в выпечке и в качестве моющего средства. Натриевая гидроксид используется в производстве мыла и бумаги. Кроме того, натрий используется в производстве стекла, лекарств и других продуктов.
Какие опасности связаны с использованием натрия?
Натрий является реактивным металлом и может быть опасен при неправильном использовании. Контакт с натрием может вызывать ожоги на коже и раздражение глаз. Кроме того, натрий реагирует с водой, выделяя взрывоопасный водород. Поэтому необходимо соблюдать осторожность при работе с натрием и его соединениями.
Какие свойства имеет натрий?
Натрий является щелочным металлом и имеет низкую плотность. Он имеет серебристо-белый цвет и мягкую консистенцию. Натрий легко реагирует с водой и кислородом, образуя соответствующие соединения. Он также хорошо проводит тепло и электричество.
