При взаимодействии металла с неметаллом происходит особый химический процесс, который имеет свое название. Такое взаимодействие может происходить под воздействием различных факторов, таких как температура, давление, наличие катализаторов и других веществ. В результате этого процесса происходит образование нового вещества, имеющего уникальные свойства и химическую формулу.
Одним из таких процессов является окисление металла неметаллом. При этом взаимодействии воздуха с поверхностью металла происходит образование оксидов металла, которые могут иметь различные цвета и структуру. Например, при взаимодействии железа с кислородом образуется ржавчина, которая является оксидом железа.
Взаимодействие металла с неметаллом может также приводить к образованию солей. Например, при взаимодействии железа с хлором образуется хлорид железа, который применяется в производстве различных веществ, таких как красители, проводящие материалы и прочие химические соединения.
Важно отметить, что взаимодействие металла с неметаллом способно изменять физические и химические свойства исходных веществ. Это означает, что процесс взаимодействия металла с неметаллом играет важную роль в химической промышленности и научных исследованиях, а также имеет практическое применение в различных отраслях народного хозяйства.
Взаимодействие металла с неметаллом: химический процесс

Взаимодействие металла с неметаллом представляет собой химический процесс, при котором происходят изменения состава и свойств веществ. Этот процесс происходит при контакте двух различных веществ, где одно из них является металлом, а другое - неметаллом.
Химическое взаимодействие между металлом и неметаллом основано на обмене электронами. Металлы обладают свободными электронами, поэтому в процессе взаимодействия они отдают свои электроны неметаллу, который, в свою очередь, становится отрицательно заряженным и образует ионы.
Реакция между металлом и неметаллом может протекать различными способами, в зависимости от их химических свойств. Например, при взаимодействии металла с кислородом происходит окисление металла, образуются оксиды металла, которые могут иметь различные степени окисления.
Также взаимодействие металла с неметаллом может приводить к образованию солей или кислот. Например, при взаимодействии натрия (металла) с хлором (неметаллом) образуется хлорид натрия, который является солью.
Взаимодействие металла с неметаллом может происходить при разных условиях, включая температуру, давление, концентрацию реагентов и наличие катализаторов. Этот процесс является основой для многих важных химических реакций и играет важную роль в различных областях, таких как металлургия, электрохимия и промышленная химия.
Реакция между металлами и неметаллами: основные принципы

Реакции между металлами и неметаллами являются основой многих химических процессов, которые важны для нашей повседневной жизни. В этих реакциях металлы и неметаллы обмениваются электронами, что приводит к образованию ионов и образованию новых химических веществ.
Одной из основных причин, по которой металлы и неметаллы вступают в реакцию, является разность электроотрицательности. Неметаллы имеют высокую электроотрицательность, что означает, что они сильно притягивают электроны. Металлы, напротив, имеют низкую электроотрицательность и готовы отдать свои электроны.
При взаимодействии металла и неметалла происходит передача электрона из металла к неметаллу. Металл окисляется, теряя электрон, и становится положительно заряженным ионом - катионом, а неметал получает электрон и становится отрицательно заряженным ионом - анионом.
Реакции между металлами и неметаллами могут протекать с выделением или поглощением энергии. Например, реакция горения металлов в кислороде является экзотермической, то есть при этой реакции выделяется тепло и свет. С другой стороны, реакция между неметаллами и металлами, такая как реакция между кислородом и металлом натрием, может протекать с поглощением энергии.
Реакции между металлами и неметаллами являются основой для получения многих важных веществ и материалов. Например, реакция между металлом и неметаллом может привести к образованию соли - химического соединения, состоящего из ионов металла и неметалла. Также эти реакции могут быть использованы для создания различных сплавов, полимеров и керамических материалов.
Взаимодействие металла и неметалла в природе: примеры из окружающей среды

Кислород и железо: Один из наиболее известных примеров взаимодействия металла и неметалла в природе - это окисление железа. Когда железо взаимодействует с кислородом в присутствии влаги или влажного воздуха, происходит образование ржавчины. Ржавые поверхности железа имеют характерный красно-коричневый цвет, который свидетельствует о наличии окиси железа.
Углерод и железо: Другой пример взаимодействия металла и неметалла - это образование стали. Сталь - это сплав железа с углеродом. Когда углерод добавляется к железу в определенных пропорциях и проходит специальную обработку, образуется сталь, обладающая высокой прочностью и твердостью. Сталь широко используется в строительстве, автомобильной и судостроительной промышленности.
Кремний и алюминий: В природе также встречается взаимодействие металла и неметалла, например, в алюминиевых сплавах. Алюминий может быть сплавлен с различными металлами, такими как медь, магний и силикон. Добавление кремния в алюминий повышает его прочность и устойчивость к коррозии, что делает его идеальным материалом для производства авиационных и автомобильных деталей, а также в строительной отрасли.
Сера и свинец: Взаимодействие металла и неметалла также происходит при производстве аккумуляторных батарей. Свинцовые аккумуляторы широко используются в автомобилях и различных электронных устройствах. В этих аккумуляторах свинец соединяется с серой, образуя активные материалы, которые обеспечивают электрохимическую реакцию и снабжение электроэнергией.
Флуор и алюминий: Флуор и алюминий также образуют сплавы, которые обычно используются в производстве авиационных и космических аппаратов для уменьшения веса и увеличения прочности конструкций. Сплавы флюора и алюминия имеют низкую плотность и обладают хорошими механическими свойствами, что делает их ценными материалами в инженерии и технологии.
Химические свойства металлов и их влияние на взаимодействие с неметаллами

Металлы обладают рядом характерных химических свойств, которые влияют на их взаимодействие с неметаллами. Одной из основных характеристик металлов является их способность к окислению. Металлы легко отдают электроны, образуя положительно заряженные ионы, называемые катионами. Таким образом, металлы обладают хорошей электропроводностью и часто используются в электротехнике и электролитических процессах.
Окислительные свойства металлов приводят к их реакционной способности с неметаллами. Неметаллы, наоборот, имеют высокую электроотрицательность и предпочитают приобретать электроны, образуя отрицательно заряженные ионы, или анионы. Поэтому взаимодействие металлов с неметаллами часто сопровождается образованием солей, представляющих собой химические соединения, состоящие из положительно и отрицательно заряженных частиц.
Реактивность металлов с неметаллами зависит от разных факторов, включая их положение в химической активности серии. Например, металлы, находящиеся выше в серии активности, имеют большую склонность к окислительным реакциям и более легко взаимодействуют с неметаллами. Некоторые металлы, такие как натрий или магний, реагируют с кислородом даже при обычных условиях, образуя оксиды.
Взаимодействие металлов с неметаллами может также протекать в виде реакции замещения, когда один металл замещает другой в химическом соединении. Например, при контакте алюминия с раствором соли меди происходит реакция, в результате которой алюминий замещает медь в соединении, образуя алюминиевую соль, а медь выпадает в свободной форме.
Влияние условий на химическую реакцию металла с неметаллом: температура и давление

Химическая реакция, происходящая между металлом и неметаллом, зависит от различных факторов, включая температуру и давление. Эти условия могут оказать значительное влияние на характер и скорость реакции.
Температура играет важную роль в химическом взаимодействии металла с неметаллом. При повышении температуры, скорость реакции обычно увеличивается. Это происходит из-за того, что при более высокой температуре, молекулы обладают большей энергией и движутся быстрее, что приводит к большей вероятности столкновения между металлическими и неметаллическими атомами.
Однако, в зависимости от конкретных условий, повышение температуры также может привести к изменению химической реакции между металлом и неметаллом. Например, в некоторых случаях, повышение температуры может способствовать возникновению окислительных реакций, при которых металл окисляется, а неметалл выступает в качестве окислителя.
Давление также может оказать воздействие на химическую реакцию между металлом и неметаллом. При повышении давления, межатомные расстояния сокращаются, что увеличивает вероятность столкновения и взаимодействия между металлическими и неметаллическими частицами. В результате, скорость реакции может увеличиться.
В то же время, некоторые химические реакции могут быть зависимы от давления в обратной стороне. Это значит, что повышение давления может сдвинуть равновесие реакции в обратную сторону. Это может быть связано с образованием более стабильных соединений или изменением концентраций реагентов и продуктов.
Таким образом, температура и давление играют важную роль в химической реакции металла с неметаллом. Изменение этих параметров может изменить характер и скорость реакции, что может быть полезным при разработке новых материалов или оптимизации процессов производства.
Применение реакции металла с неметаллом в промышленности
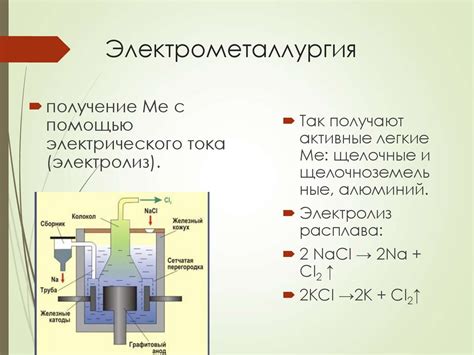
Реакции металлов с неметаллами – это важный процесс, который широко применяется в промышленности. Одной из наиболее распространенных реакций является образование соединений металл-неметалл, они используются в производстве различных материалов, изделий и химических веществ.
Одним из ключевых применений этой реакции является получение металлических сплавов. Сплавы – это материалы, состоящие из двух или более металлов, которые объединяют свои свойства и придают сплаву новые качества. Например, сплав железа с углеродом – сталь – обладает высокой прочностью и твердостью.
Также реакция металла с неметаллом применяется в процессе гальванизации. Гальванизация – это метод нанесения металлического покрытия на поверхность деталей и изделий для защиты от коррозии и придания им декоративного вида. Например, цинковое покрытие на стали защищает ее от оксидации и повышает ее стойкость к воздействию внешних факторов.
Реакция металла с неметаллом также находит применение в производстве различных химических веществ. Например, важную роль играет реакция металла с кислородом при получении оксидов металлов. Оксиды металлов применяются в качестве катализаторов, сырья для производства стекла, керамики, электронной техники и других материалов.
Таким образом, реакция металла с неметаллом имеет широкое применение в промышленности и играет важную роль в процессе создания различных материалов и веществ. Взаимодействие этих двух классов элементов позволяет получить новые соединения с улучшенными свойствами и расширить сферу их применения.
Биологическое значение взаимодействия металла с неметаллом: роль в организме

Взаимодействие металла с неметаллом имеет важное биологическое значение и играет роль в организме. Один из наиболее известных примеров такого взаимодействия – связь железа с кислородом в гемоглобине красных кровяных клеток. Железо является металлом, а кислород – неметаллом. Это взаимодействие позволяет транспортировать кислород к клеткам организма, обеспечивая их жизнедеятельность.
Кроме того, взаимодействие металла с неметаллом проявляется в работе ферментов, которые катализируют химические реакции в организме. Например, цинк играет важную роль в работе фермента цинковых пальцев, который участвует в регуляции генной экспрессии. Это означает, что без присутствия цинка в организме невозможно правильное функционирование генов и, следовательно, нормальный рост и развитие.
Взаимодействие металла с неметаллом также имеет место в иммунной системе. Например, медь играет важную роль в работе фермента церулоплазмина, который участвует в обороне организма от инфекций. Церулоплазмин активирует нейтрофилы – белые кровяные клетки, которые уничтожают бактерии и вирусы.
Таким образом, взаимодействие металла с неметаллом играет важную роль в организме, обеспечивая многочисленные биологические процессы. Без этого взаимодействия организм не смог бы функционировать нормально, поэтому поддержание баланса металлов и неметаллов в организме является одним из важных аспектов здорового образа жизни.
Вопрос-ответ

Что происходит при взаимодействии металла с неметаллом?
При взаимодействии металла с неметаллом происходит процесс, называемый окислительно-восстановительной реакцией. В результате этого процесса металл отдает электроны, образуя положительно заряженные ионы, а неметалл принимает эти электроны, образуя отрицательно заряженные ионы.
Каким образом происходит передача электронов между металлом и неметаллом?
Передача электронов между металлом и неметаллом происходит через электронный перенос, который осуществляется посредством электрического контакта между веществами. Металл отдает электроны, которые перемещаются на неметалл и заполняют его электронные орбитали.
Какие факторы влияют на скорость взаимодействия металла с неметаллом?
Скорость взаимодействия металла с неметаллом зависит от нескольких факторов. Важную роль играют электрохимические свойства веществ, такие как электронная проводимость металла и электроотрицательность неметалла. Также влияние на скорость реакции оказывают температура, концентрация веществ, наличие катализаторов и других факторов.
Какое значение имеет взаимодействие металла с неметаллом на практике?
Взаимодействие металла с неметаллом имеет большое значение на практике. Это основа для получения металлических соединений и материалов, а также для проведения различных химических реакций и процессов, таких как электролиз, гальваническая коррозия, создание электрических цепей и других.
