Металлогалогениды - это класс химических соединений, представляющий собой соединения металла с галогенами: фтором, хлором, бромом и иодом. Эти соединения обладают рядом особенностей, которые определяют их структуру, свойства и применение в различных областях науки и промышленности.
В металлогалогенидах, металл играет роль положительно заряженного иона, а галоген - отрицательно заряженного иона. Именно такое сочетание зарядов обеспечивает их устойчивость и электрохимическую активность, делая их важными реагентами в химических реакциях.
Одной из особенностей металлогалогенидов является их кристаллическая структура. В большинстве случаев, эти соединения образуют кристаллы с определенной регулярностью атомного строения. Такая структура обуславливает их механические, оптические и электронные свойства, которые могут быть использованы в различных технических и научных областях.
Металлогалогениды также обладают химической активностью, позволяющей проводить различные химические реакции. Они могут быть использованы в качестве катализаторов, веществ, позволяющих ускорить скорость химической реакции без участия в ней, или стабилизаторов, обеспечивающих стабильность и сохранение молекулярной структуры соединений. Такие свойства металлогалогенидов могут быть использованы в различных областях науки, промышленности и медицины.
Металлогалогениды: химические соединения металлов и галогенов
Металлогалогениды – это класс химических соединений, образующихся при взаимодействии металлов с галогенами. Галогены, такие как фтор, хлор, бром и йод, обладают высокой реакционной способностью и образуют стабильные соединения с металлами.
Одним из наиболее известных примеров металлогалогенидов является хлорид натрия (NaCl) – стандартный пример соли. При взаимодействии натрия и хлора образуется кристаллическое соединение, где металл и галоген образуют кристаллическую решетку, в которой ионы натрия и хлора расположены в определенном порядке.
Металлогалогениды широко используются в различных областях, включая промышленность, фармацевтику, электронику и катализ. Например, хлорид железа (FeCl3) используется в качестве катализатора в различных химических реакциях, а йодид свинца (PbI2) является одним из основных компонентов перовскитовых солнечных элементов.
Благодаря уникальным свойствам металлогалогениды находят применение и в изучении электронных и оптических свойств веществ. Например, металлогалогениды билиридия (BiI3) и свинца (PbI2) отличаются значительной оптической поглощающей способностью и используются в разработке фоточувствительных материалов и оптоэлектроники.
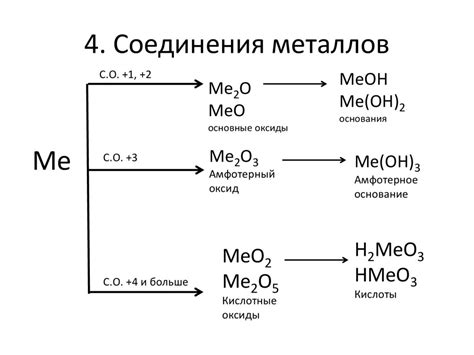
Строение металлогалогенидов

Металлогалогениды представляют собой соединения, в которых металлы связаны с атомами галогенов. Они обладают характерным строением, которое определяется взаимодействием металла и галогена.
Основной строительный блок металлогалогенидов - анионный комплекс, состоящий из металла и галогена. Металл может находиться в различных степенях окисления, что влияет на его свойства и взаимодействие с галогеном. Галогены, в свою очередь, могут образовывать одноатомные или многомерные структуры.
В металлогалогенидах встречается разнообразие структур, которые зависят от типа металла, галогена, стехиометрического соотношения компонентов и условий синтеза. Одноатомные галогены обычно связаны с металлом через ковалентную связь, что обуславливает их высокую химическую реактивность и возможность образования сложных многоатомных структур.
Многомерные структуры металлогалогенидов могут образовываться при комплексировании нескольких атомов галогена с одним или несколькими атомами металла. Такие структуры часто обладают высокой степенью организации и регулярности, что делает их интересными для использования в различных областях науки и техники.
Свойства металлогалогенидов
Металлогалогениды представляют собой класс соединений, образующихся при взаимодействии металлов с галогенами. Они обладают рядом характерных свойств, которые делают их важными в различных областях науки и технологии.
Одним из основных свойств металлогалогенидов является их высокая химическая реактивность. Благодаря этому свойству они широко используются в синтезе различных комплексных соединений и катализаторов. Кроме того, металлогалогениды могут быть использованы в качестве ионных жидкостей, имеющих хорошую электропроводность и термическую стабильность.
Еще одним важным свойством металлогалогенидов является их возможность образования трехмерных структур и полимерных цепей. Это позволяет использовать данные соединения в качестве материалов для создания полупроводников, светодиодов, солнечных батарей и других электронных устройств с широким спектром применения.
На основе металлогалогенидов также создаются материалы с ферроэлектрическими, пьезоэлектрическими и магнитооптическими свойствами. Это позволяет использовать их в производстве сенсоров и активных электронных компонентов.
Также следует отметить, что металлогалогениды обладают низкой токсичностью и могут быть использованы в медицине как лекарственные препараты. Они также широко применяются в производстве красителей, пигментов и катализаторов для химической промышленности.
Виды металлогалогенидов
Металлогалогениды представляют собой класс химических соединений, состоящих из металла и галогена. В зависимости от соотношения между металлом и галогеном, металлогалогениды делятся на различные виды.
Бинарные металлогалогениды содержат только один металл и один галоген. Они могут быть простыми соединениями, такими как NaCl или KBr, или относиться к более сложным структурам, например, к кубической перовскитной структуре, где галогенные и металлические ионы альтернируются в кристаллической решетке.
Тернарные металлогалогениды содержат помимо металла и галогена еще один элемент. Этот третий элемент может быть атомом другого металла или неметалла, и его добавление может изменить свойства соединения. Примерами тернарных металлогалогенидов являются AlCl3 или FeCl3O.
Полимерные металлогалогениды образуются в результате повторяющихся структурных блоков металлогалогенидов. Они состоят из длинных цепочек, древовидных структур или трехмерных сетей. Полимерные металлогалогениды могут обладать различными свойствами и находить применение в разных областях, таких как катализ или оптика.
Комплексные металлогалогениды состоят из металла, галогена и органического или неорганического лиганда. Лиганды могут координировать катионы металла и образовывать стабильные соединения с металлом и галогеном. Данный класс соединений может обладать интересными каталитическими или магнитными свойствами.
Все эти виды металлогалогенидов имеют свои уникальные свойства и находят применение в различных областях науки и технологий. Изучение этих соединений помогает раскрыть их потенциал и применять их в разных сферах человеческой деятельности.
Применение металлогалогенидов в различных отраслях

Металлогалогениды, соединения металла с галогенами, играют важную роль в различных отраслях науки и промышленности. Их уникальные свойства открывают широкие перспективы использования данных соединений.
В химической промышленности металлогалогениды находят применение в качестве катализаторов в химических реакциях. Например, они используются для синтеза органических соединений, полимеров и фармацевтических препаратов. Катализаторы на основе металлогалогенидов обладают высокой активностью и селективностью, что делает их востребованными в промышленности.
В электронной промышленности металлогалогениды широко используются в качестве полупроводников и переходных металлооксидных систем. Они обладают уникальными электрофизическими свойствами, такими как высокая проводимость и оптическая прозрачность. Благодаря этим свойствам металлогалогениды нашли применение в производстве полупроводниковых компонентов, оптических устройств и солнечных батарей.
В сфере энергетики металлогалогениды используются в качестве катализаторов в процессах хранения и преобразования энергии. Например, они применяются в производстве топливных элементов, а также в процессах электролиза воды для получения водорода. Металлогалогениды обладают высокой электрохимической активностью и стабильностью, что делает их эффективными катализаторами в энергетических системах.
Металлогалогениды также находят применение в медицине и фармацевтической промышленности. Они используются для создания различных лекарственных препаратов и рентгеноконтрастных веществ. Металлогалогениды обладают специфическими свойствами, которые позволяют им взаимодействовать с биологическими системами, что делает их ценными инструментами в медицинских исследованиях и разработке новых препаратов.
Синтез металлогалогенидов

Синтез металлогалогенидов – это процесс получения соединений, в которых металл связан с галогенами. Металлогалогениды широко используются в различных областях науки и техники, включая химию, фармацевтику, электронику и т.д.
Один из наиболее распространенных методов синтеза металлогалогенидов – это реакция металла с соответствующим галогеном. Для этого часто используют термические методы, при которых металл и галоген нагреваются до высоких температур, что позволяет активировать химические связи и произвести реакцию синтеза.
Кроме того, для синтеза металлогалогенидов также применяют методы реакции в растворе. В этом случае металл и галоген растворяются в подходящем растворителе, который обеспечивает необходимые условия для проведения реакции. В результате образуются металлогалогениды, которые могут быть получены в различных формах, включая кристаллические соединения, порошки или пленки.
При синтезе металлогалогенидов важно учитывать различные факторы, такие как температура, давление, соотношение компонентов и длительность реакции. Эти параметры могут существенно влиять на характер получаемых соединений, и поэтому требуют тщательного контроля и оптимизации.
В заключение, синтез металлогалогенидов является важным исследовательским направлением, которое позволяет получать новые соединения с интересными свойствами и широким спектром применения. Это позволяет углубить наши знания о взаимодействии металлов и галогенов и использовать их потенциал в различных областях развития науки и техники.
Перспективы исследования металлогалогенидов

Металлогалогениды представляют собой класс соединений, в которых металл связан с атомами галогенов, такими как хлор, бром, йод и фтор. Исследование этих соединений открывает широкий спектр возможностей для разработки новых материалов и получения ценных знаний о свойствах металлогалогенидов.
Одной из перспектив исследования металлогалогенидов является изучение их структуры и свойств. Это позволяет понять, как взаимодействие между металлом и галогеном влияет на физические и химические свойства соединения. Полученные данные могут быть использованы для создания новых материалов с уникальными свойствами, такими как высокая проводимость или оптическая активность.
Другой перспективой исследования металлогалогенидов является их применение в различных областях науки и техники. Например, металлогалогениды могут использоваться в солнечных батареях для преобразования солнечной энергии в электричество. Изучение их свойств позволяет улучшить эффективность солнечных батарей и сделать их более доступными для повседневного использования.
Также исследование металлогалогенидов может иметь значительное значение в области каталитических процессов. Галогениды металлов, например, могут использоваться в качестве катализаторов при различных химических реакциях. Изучение их экспериментальных и теоретических свойств помогает оптимизировать процессы и разработать более эффективные катализаторы для различных промышленных процессов.
В целом, исследование металлогалогенидов имеет большой потенциал для научных открытий и практических применений. Дальнейшие исследования в этой области помогут расширить наши знания о структуре и свойствах этих соединений, а также приведут к созданию новых материалов и технологий с широким спектром применений.
Вопрос-ответ

Какие металлогалогениды существуют и какие они имеют свойства?
Металлогалогениды — это соединения металла с галогенами, такими как хлор, бром, йод и фтор. Существует большое количество металлогалогенидов, каждый из которых имеет свои уникальные свойства. Например, хлорид натрия (NaCl) — это белый кристаллический порошок, который растворяется в воде и обладает соленым вкусом. Бромид железа (FeBr2) — это красный кристаллический порошок, который используется в качестве катализатора в органической синтезе. Металлогалогениды имеют широкий спектр применений в различных отраслях науки и техники.
Как происходит образование металлогалогенидов и какие факторы влияют на их стабильность?
Металлогалогениды образуются путем реакции металла с соответствующим галогеном. Обычно, это происходит путем нагревания металла в присутствии галогена, но также могут быть использованы другие методы, например, электрохимическое осаждение. Стабильность металлогалогенидов зависит от разных факторов, включая энергию связи между металлом и галогеном, концентрацию реагентов, температуру и давление. Эти факторы могут влиять на скорость реакции образования металлогалогенида и его обратную реакцию.
Какие возможности имеют металлогалогениды в сфере электроники и фотоники?
Металлогалогениды имеют широкий спектр возможностей в сфере электроники и фотоники. Например, галогенид свинца (PbX2), такой как хлорид свинца (PbCl2) или бромид свинца (PbBr2), может использоваться в качестве полупроводникового материала для создания светодиодов и солнечных батарей. Металлогалогениды также обладают интересными оптическими свойствами, такими как фотолюминесценция и возможность регулирования их цвета путем изменения размеров частиц. Это делает их перспективными для применения в оптических материалах и устройствах, таких как лазеры и дисплеи.
