Щелочные металлы - это элементы, которые относятся к первой группе периодической системы элементов. В данной статье мы рассмотрим соединение щелочных металлов, такие как литий, натрий, калий, рубидий и цезий.
Соединение щелочных металлов являются самыми распространенными и хорошо изученными соединениями. Щелочные металлы обладают высокими химическими активностями и реагируют с большинством элементов. Одним из наиболее известных соединений является хлорид лития, LiCl, который имеет широкое применение в производстве литий-ионных аккумуляторов и фармацевтической промышленности.
Соединение щелочных металлов обладают особыми свойствами, такими как высокая электропроводность и низкая плотность. Они также обладают высокими температурными свойствами и используются в производстве огнетушителей и теплоносителей в ядерной энергетике.
Важно отметить, что соединение щелочных металлов являются ядерными отходами и требуют особого внимания при их использовании и утилизации.
Что такое щелочные металлы?
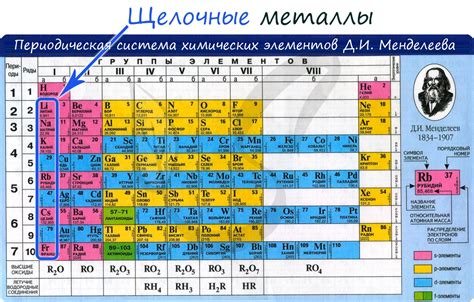
Щелочные металлы - это группа элементов периодической таблицы, состоящая из лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Они относятся к первой группе элементов и характеризуются высокой реактивностью, мягкостью, низкой плотностью и низкой температурой плавления.
Щелочные металлы обладают ярко выраженными металлическими свойствами, такими как блеск, проводимость тепла и электричества. Они легко окисляются воздухом и реагируют с водой, образуя щелочные растворы и выделяя водород. Это свойство позволяет использовать щелочные металлы в батареях и аккумуляторах.
Щелочные металлы широко используются в различных отраслях промышленности и науки. Например, натрий используется для производства стекла, калий - для производства удобрений, а литий - для производства легких и прочных материалов, аккумуляторов и лекарственных препаратов.
Однако, несмотря на полезные свойства, щелочные металлы очень реактивны и могут быть опасными при неправильном обращении с ними. Они могут воспламеняться при контакте с водой или воздухом, а их соединения могут вызывать ожоги и отравления. Поэтому необходимо соблюдать особые меры предосторожности при работе с этими элементами.
Соединение щелочных металлов
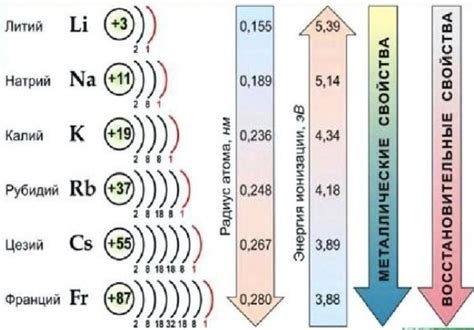
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, являются самыми реактивными элементами в периодической таблице. Из-за своей высокой активности, они легко реагируют с другими элементами и образуют различные соединения.
Соединение щелочных металлов происходит путем образования ионов. Щелочные металлы имеют один валентный электрон в своей внешней оболочке, который они готовы отдать. Они образуют положительно заряженные ионы, которые могут образовывать ионные соединения с отрицательно заряженными атомами других элементов.
Когда щелочные металлы реагируют с кислородом, они образуют оксиды. Например, реакция натрия с кислородом приводит к образованию натриевого оксида (Na2O). Когда соединение щелочного металла и кислорода растворяется в воде, оно образует гидроксиды. Например, реакция натрия с водой приводит к образованию гидроксида натрия (NaOH).
Соединение щелочных металлов также может происходить с халкогенами, такими как фтор, хлор, бром и йод. Реакция щелочного металла с халкогеном приводит к образованию соли. Например, реакция натрия с хлором приводит к образованию хлорида натрия (NaCl).
Одной из особенностей соединений щелочных металлов является их растворимость в воде. Гидроксиды щелочных металлов, такие как гидроксид натрия (NaOH) и гидроксид калия (KOH), обладают высокой растворимостью в воде и образуют щелочные растворы с щелочной реакцией.
Таким образом, соединение щелочных металлов происходит путем образования ионов и образования растворимых солей, оксидов и гидроксидов. Эти соединения обладают различными свойствами и являются важными в промышленности и научных исследованиях.
Применение соединений щелочных металлов в повседневной жизни

Соединения щелочных металлов - это химические соединения, состоящие из атомов щелочных металлов - лития, натрия, калия, рубидия, цезия и франция. Благодаря своим уникальным физическим и химическим свойствам, эти соединения широко используются в повседневной жизни человека.
Одним из наиболее распространенных применений соединений щелочных металлов является их использование в производстве щелочных батарей. Щелочные батареи широко применяются в различных электронных устройствах, таких как пульты ДУ, мобильные телефоны, фотокамеры и других устройствах, требующих постоянного питания.
Соединения щелочных металлов также используются в производстве стекла и керамики. Литий, например, входит в состав стекла, которое используется в изготовлении линз для очков и светофильтров для фотокамер. Калий и натрий используются для производства различных видов стекла, включая стеклянные посуду и окна.
Кроме того, соединения щелочных металлов играют важную роль в медицине. Натриевая и калиевая соли используются для гидратации организма и восстановления водно-солевого баланса. Литийевые препараты применяются для лечения психических расстройств, таких как биполярное расстройство и депрессия.
Кроме того, соединения щелочных металлов используются в производстве удобрений. Калийные соли, такие как калиевая соль, широко применяются в сельском хозяйстве для повышения плодородия почвы и усиления роста растений.
В заключение, соединения щелочных металлов играют важную роль в нашей повседневной жизни. Они находят применение в производстве щелочных батарей, стекла и керамики, медицине и сельском хозяйстве, их уникальные свойства делают эти соединения неотъемлемой частью различных сфер и областей нашей жизни.
Вопрос-ответ

Какие вещества могут образовываться при соединении щелочных металлов?
При соединении щелочных металлов, таких как литий, натрий, калий, образуются основные оксиды и гидроксиды. Например, образование гидроксида натрия - NaOH.
Какое значение имеют щелочные металлы в химии?
Щелочные металлы являются самыми активными металлами в группе. Они хорошо реагируют с водой и кислородом, образуя основные оксиды и гидроксиды, а также обладают низкой электроотрицательностью.
Какие особенности имеют соединения щелочных металлов?
Соединения щелочных металлов имеют ряд особенностей. Они растворимы в воде и способны образовывать кристаллы. Большинство из них являются твердыми веществами при комнатной температуре, обладают высокой теплопроводностью и электропроводностью. Они также могут иметь характерный запах и цвет.
Как получают соединения щелочных металлов?
Соединения щелочных металлов могут быть получены различными способами. Например, гидроксиды можно получить путем реакции щелочного металла с водой. Оксиды щелочных металлов могут быть получены путем нагревания металлов в кислороде или путем реакции металла с кислородом.
Какие свойства имеют щелочные металлы?
Щелочные металлы, такие как литий, натрий, калий и др., обладают рядом характерных свойств. Они имеют низкую плотность и низкую температуру плавления, очень мягкие и легко режутся ножом. Также они хорошо проводят тепло и электричество и реактивны в отношении воды и кислорода.
