Щелочные металлы, также известные как первая группа периодической системы химических элементов, обладают уникальными свойствами и играют важную роль в различных отраслях науки и промышленности. В настоящее время в щелочных металлах обозначаются только два элемента: литей (Li) и калий (K). Однако исторически эта группа включала в себя еще несколько элементов, а также сливающиеся, изменяемые вещества.
История открытия щелочных металлов начинается с открытия самого первого из них - лития. Этот элемент был обнаружен шведским химиком Иоганном Арфедсоном в 1817 году. Несколько лет спустя немецкий химик Вильгельм Генрих Вихерт изолировал другой щелочной металл - калий. Впоследствии исследования позволили установить, что ионные радиусы ионов щелочных металлов растут с увеличением атомного номера.
Остальные щелочные металлы: натрий (Na), рубидий (Rb), цезий (Cs) и франций (Fr), уже не рассматриваются как самостоятельные элементы, так как они реагируют с другими веществами и не могут существовать в свободном состоянии в природе. Открытие каждого следующего элемента щелочных металлов было важным шагом в развитии науки и позволило углубить наши знания о строении и свойствах атомов.
Сколько металлов входит в группу щелочных?
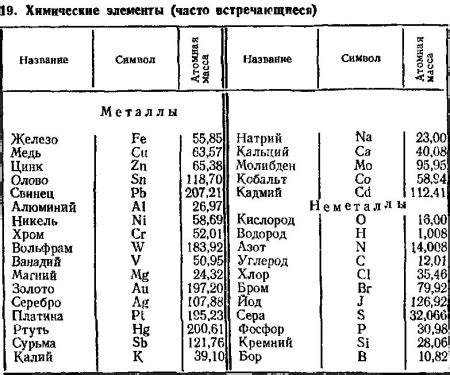
Щелочные металлы – это элементы, которые располагаются в первой группе периодической системы химических элементов. В данную группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Таким образом, всего в группе щелочных металлов насчитывается шесть элементов.
Щелочные металлы обладают общими химическими свойствами, такими как мягкость, низкая плотность, низкая температура плавления, активность при реакциях с водой и восстановительные свойства. Эти элементы хорошо растворяются в воде, образуя щелочные растворы, что было источником их названия.
Щелочные металлы широко применяются в различных областях. Например, литий используется в производстве аккумуляторных батарей и лекарственных препаратов, натрий – в производстве стекла и щелочи для очистки поверхностей, а калий – в производстве удобрений для сельского хозяйства.
Какие элементы относят к щелочным металлам?
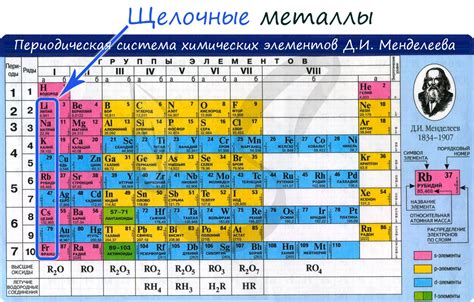
Щелочные металлы - это элементы с первой группой периодической таблицы, которые характеризуются высокой реактивностью и способностью образовывать ионы с положительным зарядом. К этой группе относятся следующие элементы:
- Литий (Li) - легкий металл, используется в производстве аккумуляторов, лекарственных препаратов и стекол.
- Натрий (Na) - серебристый металл, широко применяемый в пищевой промышленности и производстве щелочных металлических галогенидов.
- Калий (K) - мягкий металл, используется как удобрение, в производстве щелочных солей и в фармацевтической промышленности.
- Рубидий (Rb) - серебристый металл, применяется в исследовательских целях, в производстве фотокатодов и лекарственных препаратов.
- Цезий (Cs) - золотистый металл, используется в научных исследованиях, в производстве специального стекла и атомных часов.
- Франций (Fr) - радиоактивный металл, встречается в следовом количестве в природе и имеет ограниченное промышленное применение.
Все щелочные металлы имеют низкую плотность и низкую температуру плавления, а также образуют стабильные соединения с кислородом, хлором и другими химическими элементами.
Названия и свойства щелочных металлов
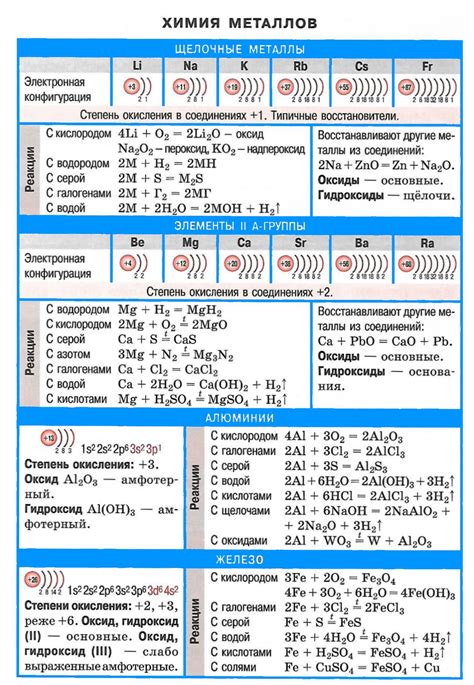
Щелочные металлы - это элементы периодической системы, которые относятся к I группе. Включая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr), эти металлы имеют ряд схожих свойств и являются элементами активной группы.
Каждый из щелочных металлов характеризуется низкой плотностью, низкой температурой плавления и реактивностью. Они обладают высокой электроотрицательностью и способны образовывать катионы с положительным зарядом, что делает их металлами-электролитами. Их ионные радиусы увеличиваются при движении по группе.
Щелочные металлы обладают сильно щелочными свойствами: они растворяются в воде, образуя гидроксиды, и их гидроксиды обладают щелочными свойствами. В реакциях с кислородом они образуют оксиды.
Кроме того, щелочные металлы хорошо проводят электричество и тепло. Они применяются в различных областях, включая производство батарей, стекла, а также в лабораторных и медицинских исследованиях. Благодаря своей высокой реактивности и активности, они часто используются в изучении химических реакций и структуры веществ.
Суммируя, названия щелочных металлов - литий, натрий, калий, рубидий, цезий и франций - сопровождаются уникальными свойствами, определяющими их группу в периодической системе элементов. Эти металлы являются важными в научных и промышленных отраслях, и их свойства продолжают открывать новые возможности и применения.
Как использовать щелочные металлы?
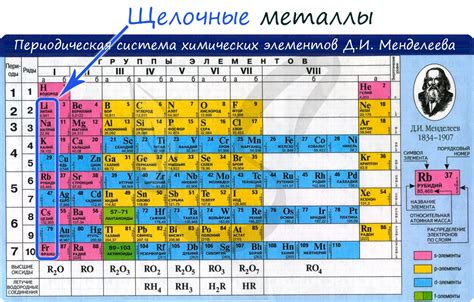
Щелочные металлы - это элементы dпериодической системы, которые характеризуются высокой реактивностью и электроотрицательностью. Известно пять щелочных металлов: литий, натрий, калий, рубидий и цезий. Каждый из них можно использовать в различных областях и сферах деятельности.
Первое и наиболее известное применение щелочных металлов - это использование их в производстве легких и высокопрочных сплавов. Литий широко используется в производстве аккумуляторов, так как обладает высокой электропроводностью и низким весом. Натрий используется в процессе получения алюминия, а также в производстве стекла и щелочей. Калий является необходимым элементом в растениеводстве и используется в удобрениях для повышения плодородия почвы.
Помимо этого, щелочные металлы применяются в фармацевтической промышленности. Например, рубидий добавляется в лекарства для лечения сердечных заболеваний. Цезий используется в медицинских аппаратах для диагностики и лечения раковых заболеваний. Также щелочные металлы находят применение в изготовлении специальной оптики и при создании солнечных батарей.
Щелочные металлы также находят применение в ядерной энергетике. Литий используется в производстве топлива для ядерных реакторов и имеет высокую способность удерживать нейтроны. Рубидий и цезий используются в вакуумных трубках для генерации электрических сигналов и в космической технике для создания стабилизирующих систем.
Как можно видеть, щелочные металлы имеют широкий спектр применения и играют важную роль в нашей повседневной жизни. Они используются в различных индустриях и сферах, таких как энергетика, фармацевтика, производство сплавов и материалов, в космической технике и многих других. Знание и использование свойств щелочных металлов позволяет создавать новые технологии и развивать науку.
Вопрос-ответ

Какие щелочные металлы существуют?
Существует шесть щелочных металлов: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Каковы свойства щелочных металлов?
Щелочные металлы обладают рядом общих свойств: они имеют низкую плотность, мягкие и легко режутся ножом, обладают низким температурным плавлением и кипением. Они очень реактивны и быстро окисляются на воздухе, образуя окисные пленки. Они также имеют низкую электроотрицательность и способны образовывать ионы положительного заряда.
