Металлы - это класс химических элементов, обладающих особыми физическими и химическими свойствами. Одной из важных характеристик металлических элементов является количество электронов на их наружном энергетическом уровне. Этот параметр определяет не только физические свойства металла, но и его способность реагировать с другими элементами и составлять соединения.
Количество электронов на наружном уровне у металлов может варьироваться от одного до шести. Это количество определяет химическую активность металла: чем больше электронов на наружном уровне, тем более активным будет металл. Например, металлы с одним электроном на наружном уровне, такие как литий и натрий, очень реакционны и легко образуют соединения с другими элементами.
Количество электронов на наружном энергетическом уровне также влияет на электропроводность металлов. Для металлов, у которых наружный уровень содержит всего один или два электрона, перенос электрического тока происходит без препятствий, и эти металлы обладают высокой электропроводностью. Напротив, металлы с большим количеством электронов на наружном уровне имеют более слабую электропроводность.
Свойства металлов и особенности электронной структуры
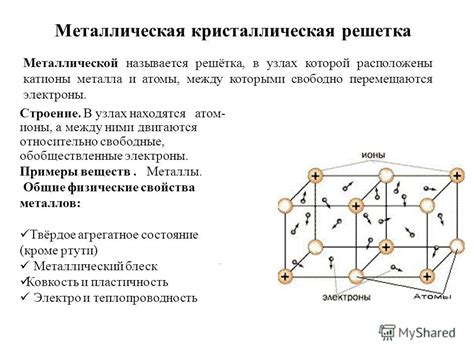
Металлы являются одной из основных групп веществ, имеющих множество уникальных свойств. Одной из ключевых особенностей металлов является их способность проводить электрический ток. Это свойство обусловлено особенностями их электронной структуры.
Электронная структура металлов отличается от электронной структуры других групп веществ, таких как неметаллы или полуметаллы. Внешний энергетический уровень металлов обычно содержит малое количество электронов, что является одной из причин их хорошей проводимости электрического тока. Эти электроны, называемые свободными электронами, могут свободно перемещаться по кристаллической решетке металла и создавать электрический ток.
Особенности электронной структуры металлов также обуславливают их другие характеристики, такие как высокая теплопроводность и хорошая пластичность. Свободные электроны обладают высокой подвижностью и способностью передавать энергию от одной точки к другой. Это позволяет металлам эффективно передавать тепло и электричество.
Также стоит отметить, что электронная структура металлов может определять их химическую активность. Благодаря низкому количеству электронов на внешнем энергетическом уровне, металлы обычно проявляют металлические свойства, такие как реакция с кислородом или образование ионов положительного заряда при химических реакциях.
Связь между электронной структурой и свойствами металлов
Электронная структура металлов играет важную роль в их свойствах. Она определяет такие вещественные характеристики, как электропроводность, теплопроводность, блеск, пластичность и т.д.
Металлы обладают высокой электропроводностью благодаря наличию свободных электронов в их энергетическом спектре. Эти электроны свободно двигаются по кристаллической решетке, создавая ток. Количество электронов на наружном энергетическом уровне металлов определяет их электропроводность. Чем больше свободных электронов, тем лучше проводимость.
Также электронная структура металлов влияет на их теплопроводность. Подобно электропроводности, теплопроводность металлов зависит от количества свободных электронов. Свободные электроны передают энергию в виде тепла внутри металлической решетки, обеспечивая высокую проводимость тепла.
Электронная структура металлов также определяет их блеск и пластичность. Блеск металлов обусловлен отражением света свободными электронами на поверхности металла. Пластичность же связана с возможностью электронов легко перемещаться в решетке металла, позволяя ему быть деформированным без разрушения.
Влияние числа электронов на наружном энергетическом уровне на химическую активность

Число электронов на наружном энергетическом уровне, также известное как валентные электроны, играет важную роль в определении химической активности металлов. Валентные электроны находятся на самом высоком энергетическом уровне и определяют способность атома металла образовывать химические связи с другими атомами и ионами.
Металлы с малым числом валентных электронов обычно обладают малой химической активностью. Это связано с тем, что у них относительно небольшая кинетическая энергия электронов, что затрудняет образование и разрыв химических связей. Такие металлы обычно считают инертными и имеют низкую реактивность.
Однако, металлы с большим числом валентных электронов обычно обладают высокой химической активностью. Большие электронные облака на наружном энергетическом уровне обеспечивают высокую кинетическую энергию электронов и легче образуют и разрывают химические связи. Такие металлы часто реагируют с другими веществами и образуют химические соединения.
Число валентных электронов также связано с электропроводностью металлов. Металлы с большим числом валентных электронов обладают лучшей электропроводностью, так как электроны на наружном энергетическом уровне легко могут двигаться вдоль кристаллической решетки и передавать электрический ток.
Итак, число электронов на наружном энергетическом уровне является важным фактором, определяющим химическую активность металлов. Большое количество валентных электронов обеспечивает высокую химическую активность и электропроводность, в то время как малое число валентных электронов приводит к низкой реактивности и инертности металлов.
Примеры металлов с разным числом электронов на наружном энергетическом уровне
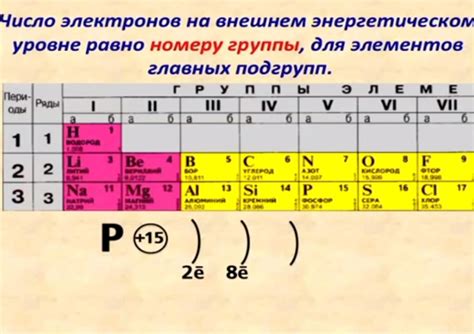
Некоторые металлы имеют разное количество электронов на своем наружном энергетическом уровне, что влияет на их свойства и химические реакции. Рассмотрим несколько примеров металлов с разным числом электронов на наружном энергетическом уровне:
1. Алюминий (Al) – 3 электрона на наружном энергетическом уровне:
- Алюминий является легким и прочным металлом, имеющим низкую плотность. Это позволяет использовать его в различных областях, включая авиацию, строительство и упаковку.
- Алюминий обладает хорошей коррозионной стойкостью благодаря образованию защитной пленки оксида алюминия на его поверхности.
- Электронная конфигурация алюминия (1s2 2s2 2p6 3s2 3p1) позволяет ему легко отдавать один электрон и образовывать положительные ионы Al^3+, что делает его полезным в процессе окисления-восстановления.
2. Железо (Fe) – 2 электрона на наружном энергетическом уровне:
- Железо является одним из самых распространенных и полезных металлов на Земле.
- Оно имеет высокую тепло- и электропроводность, что делает его неотъемлемым материалом для многих промышленных процессов и конструкций.
- Железо может образовывать соединения с различными оксидными степенями, например, Fe^2+ и Fe^3+, что позволяет ему участвовать в различных химических реакциях.
3. Золото (Au) – 1 электрон на наружном энергетическом уровне:
- Золото известно человечеству уже много тысячелетий и ценилось в различных культурах за свой блеск и драгоценность.
- Электронный наружный энергетический уровень золота делает его устойчивым и мало реакционным металлом.
- Золото обладает высокой электропроводностью и химической инертностью, что позволяет его использовать в электронике, ювелирном искусстве и других областях.
Вопрос-ответ

Какое количество электронов находится на наружном энергетическом уровне у металлов?
Количество электронов на наружном энергетическом уровне у металлов может варьироваться, но в большинстве случаев оно равно одному или двум электронам.
Какое значение имеет количество электронов на наружном энергетическом уровне у металлов?
Количество электронов на наружном энергетическом уровне у металлов определяет их химические и физические свойства, так как именно эти электроны участвуют в химических реакциях и формировании связей с другими атомами.
Как изменяются свойства металлов в зависимости от количества электронов на наружном энергетическом уровне?
Свойства металлов могут меняться в зависимости от количества электронов на наружном энергетическом уровне. Например, металлы с одним электроном на наружном уровне могут быть более реактивными и легко образовывать ионы, в то время как металлы с двумя электронами на наружном уровне могут образовывать более стабильные связи и обладать большей структурной прочностью.
Какие элементы относятся к металлам с одним электроном на наружном энергетическом уровне?
К металлам с одним электроном на наружном энергетическом уровне относятся, например, натрий (Na), калий (K), литий (Li) и цезий (Cs). Эти металлы обладают высокой реактивностью и хорошей проводимостью электричества и тепла.
Какие металлы имеют два электрона на наружном энергетическом уровне?
Металлами с двумя электронами на наружном энергетическом уровне являются, например, кальций (Ca), барий (Ba) и магний (Mg). Они обладают более стабильными связями и хорошей проводимостью электричества и тепла, но реактивностью могут быть менее высокими в сравнении с металлами с одним электроном на наружном уровне.
