Электроны - основные компоненты атомных структур, играющие ключевую роль в свойствах и характеристиках металлов. Вся химия металлов связана с поведением электронов на их внешнем энергетическом уровне. Количество электронов на внешнем энергетическом уровне металлов определяет их химическую активность, связанную с их способностью вступать в химические реакции и образовывать связи с другими атомами.
У каждого металла количество электронов на внешнем энергетическом уровне может быть различным. Оно зависит от расположения металла в периодической системе элементов. Все металлы находятся в периодах 1-12 и имеют от одного до двенадцати электронов на внешнем энергетическом уровне. Это обуславливает их способность образовывать ионные связи и обмен электронами с другими элементами.
Например, металлы в I группе периодической таблицы, такие как литий, натрий и калий, имеют только один электрон на внешнем энергетическом уровне, что делает их очень реакционноспособными. Ионы этих металлов легко образуют положительный заряд, чтобы стать стабильными. С другой стороны, металлы в VIII группе, такие как железо, никель и медь, имеют восемь электронов на внешнем энергетическом уровне, что делает их менее реакционноспособными и более стабильными.
Внешний энергетический уровень металлов: количество электронов
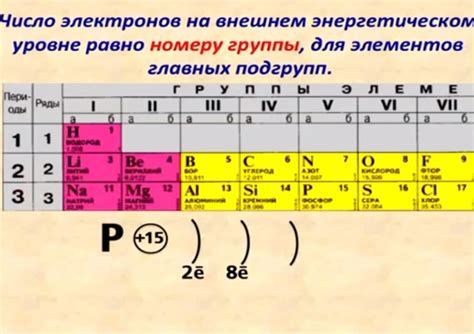
Внешний энергетический уровень металлов определяет количество электронов, находящихся на самом удаленном от ядра уровне. Он играет важную роль в химических свойствах металлов и определяет их реактивность и способность к образованию соединений.
Количество электронов на внешнем энергетическом уровне металлов может быть различным и зависит от их положения в периодической системе. Однако в большинстве случаев, металлы имеют небольшое количество электронов на внешнем уровне, что делает их хорошими проводниками электричества и тепла.
Например, у щелочных металлов, таких как литий, натрий и калий, на внешнем уровне находится 1 электрон, у щелочноземельных металлов, таких как магний и кальций, на внешнем уровне находятся 2 электрона. У переходных металлов, таких как железо и медь, количество электронов на внешнем уровне может быть различным и зависит от их положения в периодической системе.
Количество электронов на внешнем энергетическом уровне металлов влияет на их химические свойства. Большинство металлов имеют тенденцию терять электроны на внешнем уровне, образуя положительные ионы. Это объясняет их способность к образованию солей и металлических соединений. Однако некоторые металлы, такие как цинк и алюминий, могут образовывать соединения с отрицательно заряженными ионами.
Роль внешнего энергетического уровня в химических свойствах металлов

Внешний энергетический уровень является одной из ключевых характеристик атома металла, определяющей его химические свойства. Количество электронов на внешнем энергетическом уровне влияет на связывающие способности металла, его реакционную способность и температуру плавления.
У металлов на внешнем энергетическом уровне находится от 1 до 4 электронов. Чем больше электронов на внешнем уровне, тем выше связывающая способность металла. Они легко отдают свои электроны, образуя положительно заряженные ионы, и могут образовывать ионные соединения с атомами других элементов.
Например, металлы с одним электроном на внешнем уровне, такие как натрий и калий, образуют ионные соединения с элементами группы галогенов, такие как хлор и бром. Они образуют стабильные ионные связи, сильно притягивая электроны от галогенов и образуя соли.
С другой стороны, металлы с 3 или 4 электронами на внешнем уровне, такие как алюминий и железо, проявляют большую реакционную способность и смешанную связь. Они могут образовывать как ионные, так и ковалентные связи с другими элементами, что делает их химически универсальными и позволяет им формировать разнообразное количество соединений.
Кроме того, количество электронов на внешнем энергетическом уровне также влияет на температуру плавления металлов. Чем больше электронов на внешнем уровне, тем выше температура плавления металла. Это объясняется тем, что электроны на внешнем уровне создают сильные связи между атомами металла, требуя большего количества энергии для разрушения этих связей и перехода в жидкое состояние.
Таким образом, внешний энергетический уровень играет важную роль в химических свойствах металлов, определяя их связывающие способности, реакционную способность и температуру плавления. Это делает металлы одними из наиболее важных элементов в химии и промышленности.
Вопрос-ответ

Что такое внешний энергетический уровень металлов?
Внешний энергетический уровень металлов - это энергетический уровень, на котором находятся электроны на внешней оболочке атома металла. Он отвечает за химические свойства и реактивность металлов.
Какое количество электронов на внешнем энергетическом уровне имеют большинство металлов?
Большинство металлов имеют 1, 2 или 3 электрона на внешнем энергетическом уровне.
Почему количество электронов на внешнем энергетическом уровне металлов влияет на их химические свойства?
Количество электронов на внешнем энергетическом уровне металлов определяет их способность вступать в химические реакции и образовывать ионы. Это связано с тем, что в химических реакциях металлы обычно отдают электроны, и количество электронов на внешнем энергетическом уровне определяет, сколько электронов может быть отдано. Это также влияет на свойства металлов, связанные с электропроводностью и теплопроводностью.
