Щелочные металлы - это химическая группа элементов, которые находятся в первой группе периодической таблицы. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы имеют сходные свойства и химическую реактивность.
Литий является наименее реактивным из всех щелочных металлов. Он имеет низкую плотность и используется в батареях и лекарствах. Натрий - очень популярный элемент, используемый в пищевой промышленности и в производстве стекла. Калий встречается в некоторых продуктах питания и необходим для нормального функционирования организма.
Щелочные металлы имеют одну валентную электронную оболочку, что делает их очень реактивными. Они легко реагируют с водой и образуют щелочи, поэтому их называют "щелочными металлами". Они также обладают низкой температурой плавления и высокой теплопроводностью.
Рубидий и цезий являются наиболее реактивными из всех щелочных металлов. Они используются в научных исследованиях и в некоторых электронных устройствах. Франций - очень редкий и радиоактивный элемент, который рассматривается только в научных исследованиях.
Изучение щелочных металлов важно для понимания химических соединений и реакций. Они играют важную роль в жизни человека и применяются в различных областях науки и технологии.
Что такое щелочные металлы и их химические свойства
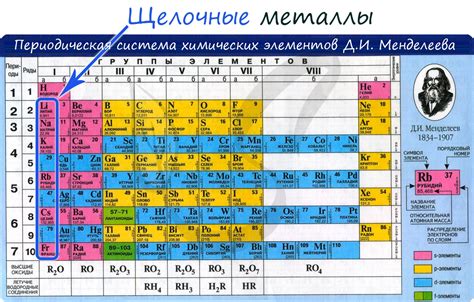
Щелочные металлы являются элементами периодической системы химических элементов, которые относятся к первой группе. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Химические свойства щелочных металлов определяются их уникальной электронной структурой и наличием одного электрона в валентной оболочке. Они являются очень активными элементами, так как стремятся отдать этот один электрон и образовать ион положительного заряда.
Щелочные металлы реагируют с водой, выделяя водородный газ и образуя щелочной раствор. Они также обладают высокой реактивностью с кислородом, азотом и серой. Кроме того, щелочные металлы обладают свойством образовывать сплавы с другими металлами и соединения с неметаллами.
Электроотрицательность щелочных металлов уменьшается с увеличением атомного номера группы, что влияет на их химические свойства. Например, литий является самым электроотрицательным щелочным металлом и обладает самой низкой плотностью, а калий является наиболее реактивным, образуя самые слабые ионы.
Для чего и в каких областях используются щелочные металлы

Щелочные металлы широко применяются в разных сферах и областях нашей жизни благодаря своим особенностям и химическим свойствам. Они являются мягкими и легкоплавкими, обладают высокой электропроводностью и часто используются в разных отраслях науки и промышленности.
Главным областями применения щелочных металлов являются электротехника и химическая промышленность. В электротехнике они используются как электроды, а также для изготовления аккумуляторов и батарей. Их высокая электропроводность позволяет использовать их в производстве проводников для передачи электричества.
Химическая промышленность использует щелочные металлы в качестве катализаторов при производстве различных химических веществ, таких как мыла, щелочные растворы, карбиды и другие продукты. Калий, например, используется для производства удобрений в сельском хозяйстве.
Щелочные металлы также находят свое применение в фармацевтической и медицинской отраслях. Натрий, калий и литий используются в составе различных препаратов для лечения сердечно-сосудистых и нервных заболеваний. Они также широко используются для создания медицинской аппаратуры, такой как батарейки для различных медицинских приборов.
В промышленности щелочные металлы применяются при производстве стекла, особенно оконного стекла, и керамики, а также в производстве огнеупорных материалов. Кроме того, они могут использоваться в процессе закалки стали и при изготовлении сплавов.
Научные исследования также тесно связаны с использованием щелочных металлов. Они используются в качестве источника ионов при создании исследовательских установок и при проведении экспериментов в рамках различных научных областей.
Таким образом, щелочные металлы являются важным и необходимым материалом в разных областях нашей жизни: от электротехники и промышленности до медицины и науки.
Важные предостережения при работе с щелочными металлами

Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, являются весьма реактивными веществами, и поэтому требуют специальных предосторожностей при работе с ними.
1. При работе с щелочными металлами необходимо надевать защитные очки, резиновые перчатки и фартук. Щелочные металлы могут реагировать с влагой и выделять воспламеняющиеся газы, поэтому важно защитить себя.
2. Перед началом работы с щелочными металлами необходимо убедиться в наличии огнетушителя и научиться им пользоваться. В случае возгорания или несчастного случая, следует немедленно принимать меры по тушению пожара.
3. Щелочные металлы должны храниться в хорошо закрытых емкостях, избегая контакта с влагой и воздухом. При хранении необходимо соблюдать указанные условия и регулярно проверять состояние упаковок.
4. При обработке или хранении щелочных металлов не следует использовать оборудование из золота, серебра и алюминия, так как эти металлы могут образовывать сплавы с щелочными металлами и вызывать взрывы.
5. При приготовлении растворов щелочных металлов необходимо добавлять их постепенно в воду, а не наоборот. Это позволяет избежать сильного нагревания и выбросов паров, которые могут быть опасными для здоровья и безопасности.
6. Важно помнить, что щелочные металлы могут быть токсичными и вызывать раздражение кожи и слизистых оболочек. Поэтому после работы с ними необходимо тщательно вымыть руки с мылом и водой.
Вопрос-ответ

Какие элементы входят в группу щелочных металлов?
В группу щелочных металлов входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Каковы свойства щелочных металлов?
Щелочные металлы обладают следующими свойствами: мягкость, низкую плотность, низкую температуру плавления и кипения, отдают электроны и образуют положительные ионы, реакционность воздушного кислорода, реакционность с водой, высокую электропроводность.
Какие вещества могут образовывать щелочные металлы?
Щелочные металлы могут образовывать щелочные оксиды, гидроксиды и соли.
Какие применения имеют щелочные металлы?
Щелочные металлы имеют различные применения. Например, натрий используется в производстве стекла и мыла, калий - в производстве удобрений, рубидий - в лазерной технологии, литий - в производстве аккумуляторов и лекарств.
Какие физические свойства характерны для щелочных металлов?
Щелочные металлы обладают низкими температурами плавления и кипения, низкой плотностью, хорошей электропроводимостью и мягкостью.
