Щелочные металлы – это химические элементы первой группы периодической системы. Они вступают во взаимодействие с водородом, образуя различные соединения. Однако, при этом происходят не только простые химические реакции, но и более сложные процессы, которые исследуются учеными.
В результате взаимодействия щелочных металлов с водородом образуется газ, который может быть использован в различных сферах человеческой деятельности. В первую очередь, образование газа происходит при реакции щелочного металла с водой, где водород выделяется в виде пузырей. Но не менее интересно, как образуется водород при взаимодействии щелочных металлов с аммиаком – это процесс, который приводит к образованию сложных координационных соединений.
Исследования в области взаимодействия щелочных металлов с водородом важны для понимания фундаментальных принципов химии и разработки новых технологий производства водорода, который является перспективным источником энергии для будущего.
Таким образом, изучение взаимодействия щелочных металлов с водородом имеет не только академическую, но и практическую значимость для развития науки и техники. Научные исследования в этой области позволяют не только расширить наши знания об химических реакциях, но и найти новые способы получения и использования водорода в различных отраслях промышленности.
Влияние щелочных металлов на образование водорода
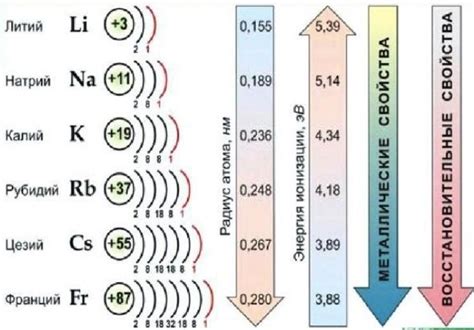
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, проявляют сильное влияние на образование водорода. Это связано с их химическими свойствами и особенностями взаимодействия с другими элементами.
Взаимодействие щелочных металлов с водородом приводит к образованию гидридов, соединений, содержащих атомы водорода. Гидриды щелочных металлов обладают высокой реактивностью и могут быть использованы в различных химических процессах.
Физические и химические свойства гидридов щелочных металлов определяются их структурой. Например, гидриды лития, натрия и калия образуются в виде кристаллических решеток, в которых атомы металла окружены атомами водорода. Это обуславливает их высокую реактивность при взаимодействии с веществами, содержащими активный водород.
Водород, образующийся при реакции щелочных металлов с водой или другими веществами, может быть использован в различных областях науки и техники. Например, он является важным компонентом в процессе генерации электроэнергии через водородные топливные элементы. Также водород широко применяется в химической промышленности и может быть использован в качестве чистого источника энергии.
Образование водорода в результате взаимодействия щелочных металлов с водой

Взаимодействие щелочных металлов с водой является одним из хорошо известных процессов химии. Когда щелочные металлы, такие как литий (Li), натрий (Na), калий (K), встречаются с водой, возникает реакция, в результате которой образуется водород (H2).
Вода (H2O) состоит из двух атомов водорода и одного атома кислорода. При взаимодействии щелочных металлов с водой, атомы металла вступают в контакт с молекулами воды. Процесс взаимодействия происходит за счет либо окисления металла, либо образования гидрида металла. При образовании гидрида металла, металловодородные соединения становятся основными продуктами реакции.
При взаимодействии щелочных металлов с водой, энергия реакции освобождается в виде тепла и возникают пузырьки водорода в результате газообразования. Взаимодействие щелочных металлов с водой является экзотермическим процессом, то есть сопровождается выделением тепла. Реакция длится до тех пор, пока металл не будет полностью расплавлен или потребованное количество воды не будет использовано.
Образование водорода в результате взаимодействия щелочных металлов с водой является важным явлением в химии. Процесс синтеза водорода, особенно изобретение методов получения водорода из воды, является одной из актуальных задач, с применением которых можно обеспечить устойчивое и экологически чистое производство энергии. Поэтому, изучение реакций взаимодействия щелочных металлов с водой является важной областью фундаментальных и прикладных исследований.
Химический процесс образования водорода при взаимодействии щелочных металлов и воды

Щелочные металлы, такие как литий, натрий и калий, обладают особой реакционной способностью при контакте с водой. Этот процесс называется водородное образование.
Водородное образование начинается с того, что щелочный металл реагирует с молекулой воды, разрушая ее на атомы водорода и гидроксидный ион. В данной реакции образуется щелочный гидроксид и выделяется водородный газ.
Уравнение реакции взаимодействия лития с водой выглядит следующим образом:
- 2Li + 2H2O → 2LiOH + H2
Целесообразно заметить, что уранение реакций взаимодействия натрия и калия с водой имеют аналогичное устройство, но отличается коэффициентами.
Этот процесс имеет значительную энергетическую выгоду и является реакцией экзотермического характера. Вследствие этого щелочные металлы могут постепенно растворяться в воде с образованием соответствующих гидроксидов и выделением водорода.
Факторы, влияющие на скорость реакции между щелочными металлами и водой
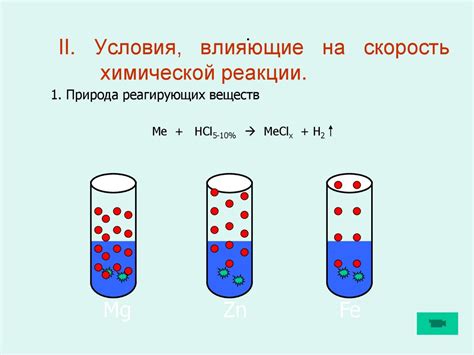
Скорость реакции между щелочными металлами и водой может быть значительно влияна различными факторами. Один из самых важных факторов – тип щелочного металла. Например, натрий и калий реагируют с водой более интенсивно, чем литий или рубидий. Это объясняется различием в их электрохимических свойствах и степени активности.
Другой фактор, влияющий на скорость реакции, – температура воды. Повышение температуры ускоряет реакцию, так как это приводит к увеличению количества молекул, обладающих достаточной энергией для преодоления энергетического барьера. При более высокой температуре осуществляются более активные столкновения между металлом и водой, что приводит к ускорению реакции.
Еще одним фактором, который влияет на скорость реакции, является поверхностная площадь щелочного металла. Большая поверхность обеспечивает большее количество активных мест для взаимодействия с водой. Например, щелочный металл в виде порошка будет реагировать с водой быстрее, чем в виде одного куска. Повышение поверхностной площади помогает увеличить активность реагентов и тем самым ускорить реакцию.
Также необходимо учитывать концентрацию щелочного металла. Повышение концентрации может привести к ускорению реакции, поскольку это увеличивает количество частиц, способных участвовать в реакции. Но слишком высокая концентрация может привести к образованию стабильной защитной пленки оксида на металлической поверхности и замедлить скорость реакции.
Роль щелочных металлов в процессе образования водорода

Щелочные металлы играют важную роль в процессе образования водорода, так как они являются активными катализаторами данной реакции.
Первый этап этого процесса - реакция щелочного металла с водой. В результате этой реакции образуется гидроксид щелочного металла и водород. Процесс происходит очень интенсивно, поскольку металлы из группы щелочных металлов имеют высокую активность в реакциях с водой.
Далее, образовавшийся гидроксид щелочного металла подвергается электролизу. В результате этой электролитической реакции водород выделяется на катоде, а окислительные и ионы гидроксида перемещаются к аноду. Однако, следует отметить, что электролиз щелочных гидроксидов требует высоких температур и специальных условий для эффективного получения водорода.
Использование щелочных металлов в процессе образования водорода имеет не только научное и промышленное значение, но и использование в повседневной жизни. Например, натрий широко используется в процессе получения водорода для различных радиотехнических, водопроводных и других промышленных целей.
Практическое применение образования водорода при взаимодействии щелочных металлов

Образование водорода при взаимодействии щелочных металлов может быть использовано в различных практических целях. Во-первых, водород является одним из важных компонентов в производстве аммиака, который в свою очередь используется в производстве удобрений. Аммиак получают путем каталитического сочетания водорода с азотом из воздуха. Щелочные металлы, такие как натрий или калий, могут служить в качестве катализатора для этой реакции. Благодаря этому применению образования водорода, щелочные металлы находят широкое применение в сельском хозяйстве и растениеводстве, способствуя увеличению урожайности и повышению плодородия почвы.
Во-вторых, водород является важным топливом для водородных энергетических технологий, таких как водородные топливные элементы. Водородные топливные элементы работают на основе реакции окисления водорода и позволяют получить электрическую энергию без выделения вредных выбросов. Щелочные металлы, например литий, используются как компоненты электролита в таких топливных элементах, где они обеспечивают электропроводимость и стабильность работы системы. Практическое применение щелочных металлов в водородных энергетических технологиях способствует созданию экологически чистых и энергоэффективных источников энергии.
Третье практическое применение образования водорода при взаимодействии щелочных металлов связано с использованием его в процессах восстановления и хранения энергии. Водород может служить как универсальное восстанавливающее агент, способное принимать или отдавать электроны во время различных химических реакций. Это позволяет использовать водородные системы для хранения энергии, например, в виде водородных батарей или водородных газовых аккумуляторов. Возможность хранения энергии в водородной форме с помощью щелочных металлов способствует развитию устойчивых источников энергии и решению проблемы энергетической независимости.
Вопрос-ответ

Какие соединения образуют щелочные металлы с водородом?
Щелочные металлы образуют гидриды с водородом. Например, натрий образует гидрид NaH, калий - KH, рубидий - RbH и цезий - CsH.
Почему щелочные металлы образуют соединения с водородом?
Щелочные металлы образуют соединения с водородом из-за их высокой активности и низкой ионизационной энергии. Эти свойства позволяют щелочным металлам легко передавать электроны водороду и образовывать соединения.
Чему равна общая формула гидридов щелочных металлов?
Общая формула гидридов щелочных металлов - MH, где M обозначает щелочный металл.
Какая реакция происходит при образовании гидридов щелочных металлов?
При образовании гидридов щелочных металлов происходит реакция щелочного металла с водородом. Например, натрий реагирует с водородом по следующему уравнению: 2 Na + H2 -> 2 NaH.
Для чего используют гидриды щелочных металлов?
Гидриды щелочных металлов используются в различных областях, таких как производство чистого водорода, хранение водорода, в качестве катализаторов и в процессах синтеза органических соединений.
