Калий - один из самых известных и широко используемых химических элементов. Он относится к группе щелочных металлов, которые обладают рядом уникальных свойств и особенностей. Превращение щелочных металлов, включая калий, является одной из наиболее интересных исследовательских областей, которая до сих пор вызывает оживленный интерес среди ученых и химиков по всему миру.
Щелочные металлы, включая калий, имеют очень низкую энергию ионизации. Это означает, что для отделения электрона от атома калия требуется минимальное количество энергии. Это делает калий очень реактивным и легко превращаемым элементом. Благодаря этим свойствам калий образует различные соединения и реагирует с другими веществами при комнатной температуре.
Процесс превращения калия и других щелочных металлов характеризуется образованием ионов с положительным зарядом, так называемых катионов. Калий, оказавшись в реакции с другими веществами, может легко передать свой электрон другому атому или молекуле, что позволяет формировать новые соединения и образования.
Влияние калия на превращение щелочных металлов
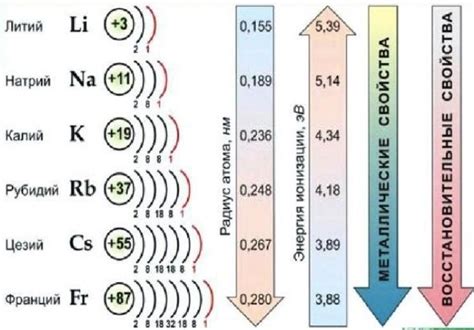
Калий является одним из щелочных металлов, и его присутствие может оказать значительное влияние на превращение других щелочных металлов. Для понимания этого влияния необходимо обратиться к химическим свойствам калия и других щелочных металлов.
Калий обладает высокой реакционной способностью и может образовывать стабильные и нестабильные соединения с различными элементами. Его наличие может привести к образованию новых фаз или изменению фазового состава при превращении других щелочных металлов. Например, в реакции с натрием или литием калий может образовывать сплавы или формировать новые кристаллические структуры.
Одно из важных свойств калия, которые оказывают влияние на превращение щелочных металлов, - его способность растворяться в различных растворителях. Калий может быть растворен в разных органических и неорганических соединениях, образуя специфические реакционные среды с определенными свойствами. Присутствие калия в таких реакционных средах может изменить химическую реакцию и привести к образованию новых соединений или изменению характеристик исходных металлов.
Таким образом, влияние калия на превращение щелочных металлов является существенным. Взаимодействие калия и других щелочных металлов может привести к образованию новых фаз, изменению фазового состава или химической реакции с образованием новых соединений. Это является важным фактором при исследовании и использовании щелочных металлов в различных областях науки и промышленности.
Свойства и значения калия

Калий является щелочным металлом и химическим элементом с атомным номером 19 в периодической таблице.
У калия имеется мягкий серебристо-белый металлический блеск и низкая плотность, что делает его легким в обработке.
Калий является очень реактивным элементом и быстро окисляется на воздухе, поэтому он обычно хранится в инертной среде, такой как минеральное масло или керосин.
Калий обладает хорошей электропроводностью и используется в производстве различных электронных устройств, таких как транзисторы и солнечные батареи.
Калий играет важную роль в растениях и животных, так как он является необходимым элементом для нормального функционирования клеток и регулирования водного баланса.
Значение калия в организмах людей и животных заключается в его важной роли в работе сердечно-сосудистой системы и нервной системы, а также в поддержании нормального уровня давления крови и устойчивости мышц.
Первые открытия щелочных металлов

История открытия щелочных металлов начинается в конце XVIII века. Первым из них был открыт калий. Открытие этого элемента произошло в 1807 году французским химиком Шарлем-Луи Талландье, который независимо от него работал над этими металлами.
Талландье получил калий путем электролиза его гидроксида, известного также как пижмонат калия. Эксперименты с проведением электрического тока через различные растворы стали важной частью исследований в то время, что позволило ученым обнаружить и изолировать новые элементы.
Калий был назван в честь слова "калия", которое на латыни означает "калиевые соли". Эта название было выбрано из-за наличия значительного количества калия в различных минералах, таких как пижма и селитра. Калий был первым щелочным металлом, открытым человеком, и новость о его открытии вызвала большой интерес в научном сообществе.
Химические переходы калия
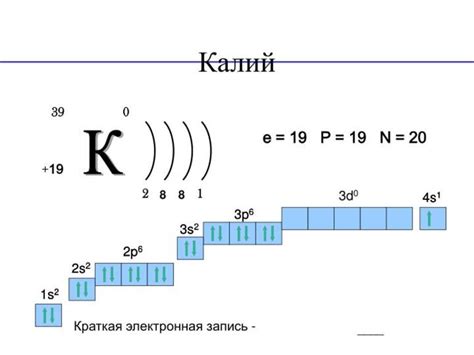
Калий – щелочной металл, который обладает активностью в химических реакциях. При взаимодействии калия с кислородом происходит образование оксида калия (K2O), который является алкалием. Это реакция химического окисления, при которой калий отдает электроны и образует положительный ион.
Взаимодействие калия с водой приводит к образованию гидроксида калия (KOH), который является щелочью. Это реакция окисления калия, при которой он отдает электроны и образует положительный ион. Гидроксид калия широко используется в промышленности и научных исследованиях.
Калий может также реагировать с галогенами, образуя соли. Например, при взаимодействии с хлором образуется хлорид калия (KCl). Эта реакция представляет собой пример образования ионной связи, при которой калий отдает электроны и образует положительный ион, а галоген принимает электроны и образует отрицательный ион.
Калий также может вступать в реакцию с некоторыми кислотами, образуя соли. Например, взаимодействие с серной кислотой приводит к образованию сульфата калия (K2SO4). Это реакция, при которой калий отдает электроны и образует положительный ион, а кислота принимает электроны и образует отрицательный ион.
Особенности превращения калия

Превращение калия – это химическая реакция, в результате которой калий превращается из одного состояния в другое. Калий является щелочным металлом, и его превращение происходит с сильным выбросом энергии.
При превращении калия происходит реакция с кислородом из воздуха, что приводит к окислению металла. В результате образуется окись калия, которая имеет ярко-желтый цвет. При этом выбросится большое количество тепла и света.
Поверхность окиси калия тонкая и ломкая, что обеспечивает доступ кислорода к металлу и ускоряет процесс превращения. Кроме того, влияние кислорода приводит к формированию кристаллической структуры оксида, что делает его более устойчивым.
Превращение калия может быть использовано в различных химических реакциях и экспериментах. Например, при горении калия в атмосфере кислорода образуется яркая пламя с фиолетовым оттенком. Также калий используется в производстве удобрений и как компонент при получении различных химических соединений.
Негативное влияние калия на окружающую среду

Калий, превращаясь из щелочного металла в соединения, может оказывать негативное влияние на окружающую среду. Во-первых, высокая концентрация калия в почве может вызывать ее засоление, что негативно сказывается на качестве и плодородии почвы. Это может привести к уменьшению урожая и снижению качества сельскохозяйственных культур.
Во-вторых, калий содержится в многих удобрениях, которые часто применяются в сельском хозяйстве. Использование больших количеств удобрений с высоким содержанием калия может привести к его перегрузке в почве и водных ресурсах. Это может негативно сказаться на водной экосистеме, вызывая понижение кислорода в воде и смерть рыб и других водных организмов.
Кроме того, калий может быть втянут в атмосферу при сжигании растительной массы. Выпуск калия в атмосферу может привести к загрязнению воздуха и образованию смога. Постоянное присутствие калия в воздухе может представлять опасность для здоровья человека, особенно для людей с заболеваниями дыхательной системы и астмой.
В целом, необходимо контролировать концентрацию калия в почве и водных ресурсах, чтобы минимизировать его негативное влияние на окружающую среду. Для этого можно применять сбалансированное использование удобрений, контролировать сжигание растительной массы и внедрять технологии очистки и рециклирования для уменьшения выбросов калия в атмосферу и водные ресурсы.
Использование калия в промышленности

Калий – это щелочной химический элемент, который обладает рядом уникальных свойств и находит широкое применение в промышленности.
1. Производство удобрений: Калий является одним из основных компонентов для производства удобрений. Он играет важнейшую роль в обеспечении нормального роста и развития растений. Калийные удобрения способствуют повышению урожайности, улучшению качества плодов и устойчивости растений к стрессовым условиям.
2. Металлургия: Калий используется в металлургической промышленности для получения сплавов с другими металлами. Такие сплавы обладают повышенной прочностью и устойчивостью к окислению, что делает их идеальными материалами для производства авиационных и космических конструкций.
3. Химическая промышленность: Калий и его соединения находят применение в различных отраслях химической промышленности. Например, калий используется в производстве стекла для придания ему прочности и прозрачности, а также в производстве мыла и моющих средств.
4. Электроника: Калийные соединения применяются в электронике для создания электролитов, которые используются в различных электролитических процессах. Калийные электролиты являются надежными и эффективными растворами, которые обеспечивают стабильность и безопасность работы электронных устройств.
5. Производство взрывчатых веществ: Калийные соединения используются в производстве взрывчатых веществ, таких как пиротехнические и взрывные материалы. Калийные соли обладают способностью интенсивно гореть при взаимодействии с кислородом, что делает их незаменимыми компонентами во многих пиротехнических и взрывных смесях.
Значение калия в лечебных целях

Калий – важный химический элемент, часто используемый в лечебных целях. Он является одним из основных постоянных компонентов организма человека и выполняет множество функций, влияющих на здоровье и работу различных систем организма.
Калий играет важную роль в поддержании нормальной работы сердечно-сосудистой системы. Он регулирует сердечный ритм и силу сокращения сердца, участвует в передаче нервных импульсов и контролирует сокращение мышц. Недостаток калия может привести к нарушениям ритма сердца, повышению артериального давления и развитию сердечной недостаточности.
Калий также влияет на работу почек и образование мочи. Он помогает поддерживать нормальный баланс воды и солей в организме, а также улучшает фильтрацию и выведение токсинов. Недостаток калия может привести к образованию камней в почках и развитию хронической почечной недостаточности.
В дополнение к этому, калий играет важную роль в поддержании здоровья нервной системы. Он участвует в передаче нервных импульсов и помогает поддерживать нормальное функционирование мозга. Недостаток калия может привести к раздражительности, нарушению сна и концентрации, а также проблемам с памятью.
Итак, калий имеет большое значение для организма человека, особенно в лечебных целях. Регулярное потребление продуктов, богатых калием, таких как бананы, картофель, орехи и сушеные фрукты, поможет поддерживать нормальный уровень калия в организме и сохранять здоровье сердца, почек и нервной системы.
Вопрос-ответ

Зачем нужен калий организму человека?
Калий является необходимым микроэлементом для нормального функционирования организма человека. Он участвует в регуляции водного баланса, поддержании нормального кровяного давления, сокращении мышц, передачи нервных импульсов и других метаболических процессах.
Какие продукты содержат большое количество калия?
Большое количество калия содержат бананы, картофель, сушеные фрукты, шпинат, абрикосы, семена тыквы, фасоль и гречка. Также калий присутствует в рыбе, молочных продуктах и мясе.
Какие проблемы могут возникнуть при недостатке калия?
Недостаток калия в организме может привести к нарушению нервной системы, мышечным судорогам, нарушению сердечного ритма, повышенному артериальному давлению и другим проблемам. Также недостаток калия может вызвать ослабление иммунной системы и ухудшение общего состояния организма.
Может ли избыток калия быть опасным для здоровья?
Да, избыток калия в организме также может быть опасным. Он может привести к сердечным проблемам, нарушению работы почек, а также вызвать снижение уровня сахара в крови. Поэтому важно не превышать установленную норму потребления калия и консультироваться с врачом, особенно при наличии заболеваний почек или сердечно-сосудистой системы.
