Щелочные металлы - это группа элементов, которые находятся в первой группе периодической системы химических элементов. Эти элементы обладают рядом схожих характеристик и свойств, которые делают их необычными и важными в химической и физической науке.
Как правило, щелочные металлы имеют низкую плотность, низкую температуру плавления и кипения, а также высокую реактивность. Они обычно мягкие и можно резать ножом. Кроме того, они хорошо проводят электричество и тепло.
Если говорить о конкретных элементах, относящихся к группе щелочных металлов, то это литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Каждый из них имеет свои уникальные свойства и применения в научных и промышленных областях.
Литий, например, широко используется в производстве легких металлов, а также в производстве аккумуляторов. Натрий находит свое применение в пищевой промышленности. Калий является важным элементом для жизни растений и используется в сельском хозяйстве. Рубидий и цезий находят применение в научных исследованиях и в производстве специальной электроники.
Франций, самый редкий и редкоземельный из всех щелочных металлов, имеет огромный потенциал в ядерной энергетике и других технологиях будущего. Изучение щелочных металлов и их свойств по-прежнему является одной из актуальных тем для ученых и исследователей.
Определение щелочных металлов и их особенности
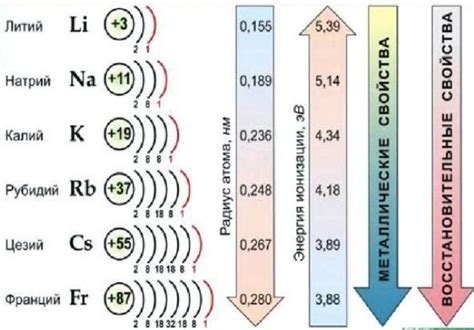
Щелочные металлы - это группа элементов, которая включает в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они являются первой группой периодической таблицы элементов и характеризуются рядом особых свойств.
Первое важное свойство щелочных металлов - их реакционная способность. Они с легкостью реагируют с кислородом, водой и многими другими веществами. Реакции щелочных металлов с водой особенно ярко проявляются: при этом образуется водород и образуется щелочная основа.
Второе важное свойство - низкая плотность. Все щелочные металлы являются легкими элементами, что делает их легкими для обработки и транспортировки. Например, литий является легким металлом, значительно легче, чем алюминий. Это свойство делает щелочные металлы востребованными в различных отраслях промышленности и техники.
Третье важное свойство - высокая химическая реакционность и токсичность. Щелочные металлы обладают способностью спонтанно воспламеняться в контакте с воздухом или водой. Они также могут вызывать раздражение кожи и слизистых. Поэтому, при работе с щелочными металлами необходимо особое внимание и меры безопасности.
Четвертое важное свойство - высокая электропроводность. Щелочные металлы обладают высокой электропроводностью, что делает их полезными в производстве аккумуляторов и других электронных устройств. Этим свойством обуславливается их применение в различных энергетических технологиях, таких как батареи и солнечные элементы.
В заключение, щелочные металлы являются важными элементами в нашей жизни и промышленности. Их уникальные свойства делают их незаменимыми во многих отраслях, от электроники до медицины. Однако при работе с ними необходимо соблюдать особые меры предосторожности, так как они являются реакционноспособными и токсичными веществами.
Перечень металлов, относящихся к щелочным металлам
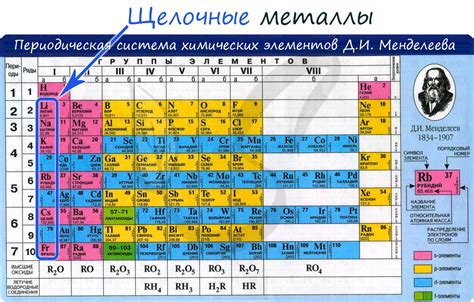
Щелочные металлы представляют собой группу химических элементов, которые обладают особыми свойствами и широко используются в различных областях. Всего к щелочным металлам относятся 6 элементов, они входят в первую группу периодической таблицы.
Первым металлом из этой группы является литий. Он обладает наименьшей атомной массой среди щелочных металлов и имеет низкую плотность. Литий находится в состоянии газообразного металла при обычных условиях.
Вторым металлом щелочной группы является натрий. Этот элемент широко используется в промышленности для производства химических соединений и в процессе пищеварения. Натрий является хорошим проводником электричества и тепла.
Калий, третий металл щелочной группы, также имеет множество применений. Он используется для удобрений, в производстве стекла и мыла, а также в лабораторных исследованиях. Калий является необходимым элементом для многих живых организмов, включая растения и животных.
Рубидий, четвертый металл из группы щелочных металлов, редко встречается в природе. Он используется в научных исследованиях, а также в производстве фотоэлементов и лазеров. Рубидий имеет свойства, похожие на свойства других щелочных металлов.
Цезий, пятое вещество группы, является наименее распространенным из всех щелочных металлов. Он используется в ядерных реакторах, в процессе изготовления стекла и в научных исследованиях. Цезий имеет низкую радиоактивность и используется в медицине для лечения рака.
Последним металлом щелочной группы является франций. Он является самым редким и самым радиоактивным элементом из всех щелочных металлов. В природе франции практически нет, он получается искусственным путем. В связи с его вредными свойствами франций имеет очень ограниченные применения.
Применение щелочных металлов в различных отраслях

Щелочные металлы включают литий, натрий, калий, рубидий, цезий и франций. Они известны своей активностью и высокой реакционностью, что делает их ценными в различных отраслях.
1. Применение в электротехнике: Щелочные металлы используются в производстве литий-ионных аккумуляторов, которые являются основным источником питания для мобильных устройств, электронных автомобилей и портативных электронных устройств. Кроме того, натрий и калий используются для создания щелочных батарей, широко применяемых в бытовых и промышленных устройствах.
2. Применение в фармацевтической промышленности: Некоторые соединения щелочных металлов используются в производстве медицинских препаратов. Например, литий используется в лекарствах, предписываемых для лечения биполярного расстройства и депрессии.
3. Применение в металлургии: Натрий и калий играют важную роль в металлургической промышленности. Натрий используется для очистки металлов от оксидов и в процессе производства алюминия. Калий используется при производстве стали и сплавов.
4. Применение в производстве стекла: Литий и натрий применяются в производстве стекла, так как они понижают температуру плавления и улучшают его механические свойства. Калий также используется в производстве стекла для улучшения его прозрачности и термической стабильности.
5. Применение в научном исследовании: Щелочные металлы широко используются в научных исследованиях и экспериментах. Например, литий используется в ядерных реакторах, рубидий применяется в атомных часах и франций используется в изучении особенностей атомного строения.
Таким образом, щелочные металлы имеют широкий спектр применения в различных отраслях, от электротехники до фармацевтики и металлургии, делая их важными материалами в современных технологиях и научных исследованиях.
Вопрос-ответ

Что такое щелочные металлы?
Щелочные металлы - это группа металлов, характеризующихся высокой химической активностью и помещающихся в первой группе периодической системы элементов. Они включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Эти металлы обладают уникальными физическими и химическими свойствами.
Какие металлы относятся к щелочным?
К щелочным металлам относятся следующие элементы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они являются самыми мягкими и легкими металлами и характеризуются высокой химической активностью.
Какие свойства характерны для щелочных металлов?
Щелочные металлы обладают рядом характерных свойств. Они являются мягкими и легкими металлами, которые легко режутся ножом. Они также имеют низкую плотность, низкую температуру плавления и высокую теплопроводность. Они реагируют с водой и кислородом, образуя гидроксиды и оксиды.
Какие особенности химической активности у щелочных металлов?
Щелочные металлы характеризуются высокой химической активностью. Они легко реагируют с водой, образуя гидроксиды и высвобождая водород. Они также реагируют с кислородом, огнем и другими веществами. Их активность возрастает по мере движения по периодической системе элементов от лития к францию.
Какие применения у щелочных металлов?
Щелочные металлы находят множество применений в различных областях. Например, литий используется в производстве аккумуляторов и лекарствах для лечения биполярного расстройства. Натрий используется в производстве стекла, щелочей и пищевой промышленности. Калий применяется в удобрениях и лекарствах. Рубидий используется в ядерной энергетике и в океанографии, а цезий находит применение в научных и медицинских исследованиях.
