Оксиды щелочных металлов представляют собой соединения, получаемые в результате реакции металлического оксида с водой. Такое взаимодействие является химическим процессом, в результате которого происходит образование щелочи – водного раствора оснований, обладающего высокой щелочностью.
Вода, как известно, является основным растворителем, способным взаимодействовать с различными веществами. Таким образом, оксиды щелочных металлов, которые растворяются в воде, вызывают химическую реакцию, в результате которой происходит образование щелочи.
Процесс образования щелочи в результате взаимодействия оксида щелочного металла с водой происходит по следующей реакции:
M2O + H2O → 2MOH
Здесь M обозначает щелочной металл, например, натрий, калий, литий и т.д. При этом оксид щелочного металла растворяется в воде, образуя щелочную соль и осаждаясь в виде щелочи. Таким образом, взаимодействие оксида щелочного металла с водой приводит к получению щелочи – важного химического соединения, применяемого в различных областях науки и промышленности.
Оксид щелочного металла и его свойства
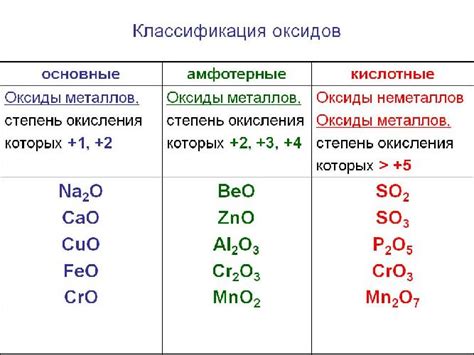
Оксид щелочного металла - это химическое вещество, состоящее из кислорода и щелочного металла. Он обладает рядом уникальных свойств, которые делают его важным в различных областях науки и промышленности.
Одним из основных свойств оксида щелочного металла является его щелочность. При контакте с водой, оксид щелочного металла образует гидроксид щелочного металла. Этот процесс называется гидратацией и сопровождается выделением большого количества тепла.
Гидроксид щелочного металла является сильным основанием и обладает высокой щелочностью. Он может быть использован в различных отраслях промышленности, включая производство стекла, мыла, бумаги и многих других продуктов.
Кроме того, оксид щелочного металла обладает высокой электропроводностью. Это свойство делает его полезным в процессах электролиза и производстве электротехнических устройств. Оксид щелочного металла также используется в качестве катализатора в различных химических процессах.
Оксиды щелочных металлов имеют различную степень растворимости в воде. Некоторые из них растворяются полностью, а некоторые образуют нерастворимые осадки. Это свойство позволяет использовать оксиды щелочных металлов для удаления загрязнений из воды и органических соединений.
В целом, оксиды щелочных металлов обладают широким спектром свойств, которые делают их важными компонентами в различных отраслях науки и промышленности. Изучение данных свойств позволяет расширить наши знания о химических соединениях и использовать их эффективно для различных приложений.
Взаимодействие оксида щелочного металла с водой

Оксиды щелочных металлов – это химические соединения, которые могут реагировать с водой, образуя щелочные растворы. При контакте с водой происходит гидратация оксида щелочного металла, что приводит к образованию гидроксида. Этот процесс является экзотермическим и сопровождается выделением тепла.
В реакции взаимодействия оксида щелочного металла с водой участвуют ионы гидроксида и гидроксония. Гидроксид щелочного металла растворяется в воде, образуя гидроксидные ионы (OH-) и оксоанионы (M(OH)n^(-m)). Гидроксонии, в свою очередь, формируются из молекул воды, которые диссоциируют под влиянием протолитических свойств оксида.
Образование щелочных растворов является важным процессом в химии и применяется в различных областях, таких как производство мыла, стекла и других продуктов. Щелочные растворы также используются в медицине, аналитической химии, бытовой химии и других областях науки и промышленности.
Оксиды щелочных металлов, такие как оксид натрия (Na2O) и оксид калия (K2O), обладают сильными щелочными свойствами и могут реагировать с водой довольно интенсивно. Однако, оксиды некоторых металлов, например, оксид лития (Li2O), реагируют с водой более медленно и менее интенсивно.
Образование щелочи при взаимодействии оксида щелочного металла с водой

Оксид щелочного металла представляет собой соединение металла с кислородом. При взаимодействии оксида щелочного металла с водой происходит химическая реакция, в результате которой образуется щелочь. Щелочь - это раствор щелочного металла в воде, обладающий щелочной реакцией.
В химической реакции между оксидом щелочного металла и водой металл замещает водород, образуя гидроксид щелочного металла. При этом происходит растворение оксида в воде, и реакция сопровождается выделением тепла.
Образование щелочи при взаимодействии оксида щелочного металла с водой имеет множество применений. Щелочи широко используются в производстве мыла, стекла, моющих средств, а также в различных химических процессах.
Химическое свойство щелочей - щелочная реакция - служит основой для их использования в нейтрализации кислот. При смешивании щелочи с кислотой образуется соль и вода.
Образование щелочи при взаимодействии оксида щелочного металла с водой является одним из основных способов получения щелочей и является важной химической реакцией с промышленным применением.
Применение щелочи, получаемой из оксида щелочного металла

Щелочь, получаемая из оксида щелочного металла, имеет широкий спектр применений в различных областях. Ее высокая щелочность и активность позволяют использовать ее в разных процессах и производствах.
В бытовых условиях, щелочь из оксида щелочного металла применяется в качестве моющего средства. Благодаря своим высоким щелочным свойствам, она удаляет жир, пятна и другие загрязнения с поверхностей. Многие моющие средства, такие как мыло и моющие порошки, содержат щелочи, полученные из оксида щелочного металла.
В промышленности, щелочь, получаемая из оксида щелочного металла, используется в процессах химического производства. Например, ее применяют для нейтрализации кислот, в производстве стекла и мыла, а также для регулирования pH в различных процессах.
В сельском хозяйстве, щелочь из оксида щелочного металла применяется для обработки почвы. Она улучшает ее структуру, повышает урожайность, а также уничтожает вредные организмы и сорняки.
В медицине, щелочь из оксида щелочного металла используется для производства лекарственных препаратов. Она может служить основой для создания различных форм медикаментов, таких как таблетки, капсулы и растворы.
В целом, щелочь, получаемая из оксида щелочного металла, играет важную роль в различных отраслях человеческой деятельности и нашла широкое применение благодаря своим уникальным свойствам.
Вопрос-ответ

Что такое оксид щелочного металла?
Оксид щелочного металла - это химическое соединение, состоящее из элемента щелочного металла и кислорода. Примеры оксидов щелочных металлов: оксид натрия (Na2O), оксид калия (K2O), оксид лития (Li2O) и другие. Они обладают щелочными свойствами и широко используются в различных отраслях промышленности.
Как происходит взаимодействие оксида щелочного металла с водой?
Взаимодействие оксида щелочного металла с водой приводит к образованию щелочного раствора. Уравнение реакции для такого процесса можно представить следующим образом: MO + H2O -> M(OH), где MO - оксид щелочного металла, M(OH) - гидроксид щелочного металла. В результате реакции окисления металла и воды образуется гидроксид и выделяется большое количество тепла.
Зачем используется взаимодействие оксида щелочного металла с водой?
Взаимодействие оксида щелочного металла с водой используется в различных сферах. Например, гидроксиды щелочных металлов часто используются в химической промышленности для производства щелочей и других химических соединений. Щелочи широко применяются в различных отраслях промышленности, например, в производстве стекла, мыла, моющих средств, бумаги и др. Также гидроксиды щелочных металлов используются в лабораторной практике и бытовых нуждах.
