Щелочные металлы весьма известны своей реакцией с водой, которая может быть как явлением спектакулярным, так и опасным. Но какой правдивой информации стоит придерживаться? Существуют множество мифов и заблуждений вокруг этой темы, и в данной статье мы попытаемся разобраться, что на самом деле происходит при реакции щелочных металлов с водой.
Щелочные металлы включают в себя литий, натрий, калий, рубидий, цезий и франций. Их химические свойства отличаются от свойств других металлов, в том числе их способностью реагировать с водой. Часто можно услышать выражение, что щелочные металлы "горят" в воде, но это не совсем точно. В действительности, реакция щелочных металлов с водой происходит под влиянием энергии, выделяемой при разрушении связей воды.
Реакция щелочных металлов с водой может проходить с выделением газа, возгоранием или даже взрывом. В результате реакции образуется гидроксид металла и выделяется водород. Какой именно будет реакция, зависит от конкретного металла и условий реакции. Однако, в любом случае, при реакции с водой необходимо соблюдать осторожность и правила безопасности, так как она может привести к серьезным последствиям.
Истинность щелочных металлов

Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, действительно обладают химическими свойствами, о которых говорят в научных источниках.
Одно из главных свойств щелочных металлов - их реакция с водой. Когда щелочный металл вступает в контакт с водой, происходит химическая реакция, в результате которой выделяется водородный газ и образуется гидроксид щелочного металла.
Кроме того, щелочные металлы известны своей большой активностью и реакционной способностью. Они легко реагируют с кислородом, хлором и другими химическими элементами, образуя различные химические соединения.
Большинство из нас могли увидеть эти реакции в школьной лаборатории, где проводились эксперименты с щелочными металлами. Эта активность и способность щелочных металлов к реакциям являются фактами, подтвержденными множеством экспериментов и исследований.
Таким образом, можно утверждать, что истинность щелочных металлов подтверждена научным сообществом и опытным путем. Их химические свойства и реакции являются действительными и широко изученными в научной среде.
Щелочные металлы и их реакция с водой
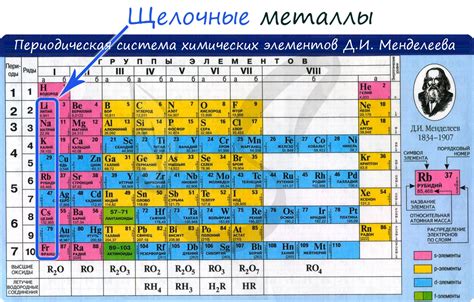
Щелочные металлы являются весьма активными элементами и легко реагируют с водой. Эти металлы включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Реакция щелочных металлов с водой иллюстрируется их способностью выделять водород. Однако, не все реакции между щелочными металлами и водой проходят одинаково.
Реакция лития с водой достаточно медленная и происходит только при нагревании. Литий постепенно реагирует с водой, образуя гидроксид лития и выделяя водород. Натрий, калий и другие щелочные металлы реагируют с водой гораздо более энергично, производя яркое пламя и выделяя большое количество водорода.
Реакция между щелочными металлами и водой основана на образовании гидроксидов металлов и водорода. Гидроксиды щелочных металлов являются лугами с высоким pH и имеют широкое применение в различных процессах, включая производство мыла, стекла и других химических соединений.
Необходимо отметить, что реакция щелочных металлов и воды может быть опасной, особенно при использовании больших количеств металлов или при неправильном обращении. Поэтому необходимо соблюдать меры предосторожности при проведении подобных экспериментов.
Между правдой и мифом

В научном мире много дискуссий вокруг щелочных металлов и их реакции с водой. Одни утверждают, что эти металлы действительно могут взрываться в контакте с водой, другие считают это всего лишь мифом. Давайте разберемся в этом подробнее.
Основной аргумент противников мифа о взрывоопасности щелочных металлов - это противоречие законам химии. По учебникам, взрывчатые вещества содержат соединения активных элементов, которые способны к самовозгоранию, в то время как щелочные металлы (например, литий, натрий и калий) являются обычными металлами, не обладающими взрывоопасностью.
Однако стоит отметить, что при взаимодействии щелочных металлов с водой может происходить крайне реактивное горение. Причина этого явления заключается в высокой реакционной способности металлов, их способности образовывать гидроксиды и выделяться большое количество водорода. Таким образом, при контакте с водой, щелочные металлы образуют гидроксиды металлов и обильное количество водорода, что может привести к вспышке горения.
Для подтверждения факта или опровержения мифа о взрывоопасности щелочных металлов существует множество экспериментов и исследований. Результаты этих исследований указывают на то, что реакция щелочных металлов с водой может быть очень опасной и даже взрывоопасной в определенных условиях.
В итоге, можно сказать, что между правдой и мифом о взрывоопасности щелочных металлов и их реакции с водой существует определенная нюансированность. Взрывы могут происходить, но не во всех случаях и только при наличии определенных условий. Тем не менее, даже при таких оговорках, взрывоопасность щелочных металлов с водой является серьезным фактором, о котором следует помнить и соблюдать необходимые меры предосторожности при работе с ними.
Наука и мифы о щелочных металлах

Щелочные металлы - это группа элементов, включающая литий, натрий, калий, рубидий, цезий и франций. В мире существует множество мифов о свойствах и реакции щелочных металлов с водой. Давайте разберемся, что же на самом деле наука говорит на этот счет.
Один из самых известных мифов гласит, что щелочные металлы взрываются при контакте с водой. Однако, это не совсем правда. Да, щелочные металлы действительно реагируют с водой, но не все они взрываются. Литий, например, реагирует очень медленно и спокойно, а вот калий и цезий могут вызвать вспышку или даже взрыв воздушно-кислородной смеси, образующейся в результате реакции. Но даже в случае с взрывами, они происходят только в определенных условиях и требуют чрезвычайно больших количеств металла.
Еще один часто встречающийся миф - это то, что при контакте щелочных металлов с водой образуется водород. Это также не совсем точно. Реакция щелочных металлов с водой действительно приводит к образованию водорода, но она не происходит мгновенно и может быть даже незаметна. Например, литий и натрий реагируют с водой очень медленно, и образование водорода может быть незначительным. Однако, калий и цезий, как уже было сказано ранее, могут привести к вспышке или даже взрыву, что связано с образованием водорода.
Еще одним распространенным мифом является то, что щелочные металлы могут реагировать с влажностью воздуха или с кожей человека и вызывать серьезные ожоги. В действительности, щелочные металлы действуют на влажность воздуха очень медленно и реакция может быть незаметной. Однако, прямой контакт кожи с щелочными металлами может вызвать ожоги, так как они обладают щелочными свойствами и могут разрушать клетки.
Вопрос-ответ

В чем заключается реакция щелочных металлов с водой?
Щелочные металлы, такие как натрий, калий и литий, реагируют с водой, образуя гидроксиды и выделяя водород. Это реакция окисления металла, при которой происходит выделение гидрогена.
Может ли реакция щелочных металлов с водой быть опасной?
Да, реакция щелочных металлов с водой может быть опасной. При взаимодействии щелочных металлов с водой выделяется водород, который может быть горючим и взрывоопасным. Кроме того, реакция может сопровождаться сильным нагреванием и выделением горячих паров.
Правда ли, что при контакте щелочных металлов с водой образуется щелочной раствор?
Да, при реакции щелочных металлов с водой образуется щелочной раствор. Это происходит из-за образования гидроксидов щелочных металлов в результате реакции. Например, при взаимодействии натрия с водой образуется натриевый гидроксид, который обладает щелочными свойствами.
Можно ли использовать щелочные металлы для получения взрывчатых веществ?
Да, щелочные металлы могут быть использованы для получения взрывчатых веществ. Например, эти металлы могут быть использованы в процессе производства динамита. Однако, из-за опасности реакции щелочных металлов с водой, такие процессы должны проводиться с осторожностью и под контролем специалистов.
Как щелочные металлы используются в повседневной жизни?
Щелочные металлы имеют широкие применения в повседневной жизни. Натрий, например, используется в производстве мыла, стекла и косметических продуктов. Калий используется в пищевой промышленности для консервирования и как добавка в удобрениях. Литий используется в производстве аккумуляторов и лекарств. При этом необходимо помнить о безопасности работы с щелочными металлами из-за их реакции с водой.
