В периодической системе элементов существует группа щелочных металлов, которая включает в себя лишь несколько элементов. Главными представителями этой группы являются литий, натрий, калий, рубидий, цезий и франций. Эти металлы характеризуются своими особыми физическими и химическими свойствами, такими как низкая плотность, низкая температура плавления и активность в реакциях с водой и кислородом.
Однако, в отличие от приведенных элементов, кальций и радий не относятся к щелочным металлам. Кальций располагается во второй группе периодической системы элементов и относится к группе щелочноземельных металлов. Он обладает большей плотностью, высокой температурой плавления и не такой высокой активностью в химических реакциях.
Что касается радия, он также относится к группе щелочноземельных металлов, которая находится во второй группе периодической системы элементов. Однако, радий отличается от остальных щелочноземельных металлов своими радиоактивными свойствами. Он является очень редким элементом и обладает высокой степенью активности.
Таким образом, кальций и радий не входят в группу щелочных металлов, хотя и относятся к близким по своим свойствам группам элементов. Их химические и физические свойства имеют некоторые отличия от остальных элементов группы, делая их уникальными в своем роде.
Щелочные металлы: что это и чем они отличаются от кальция и радия?
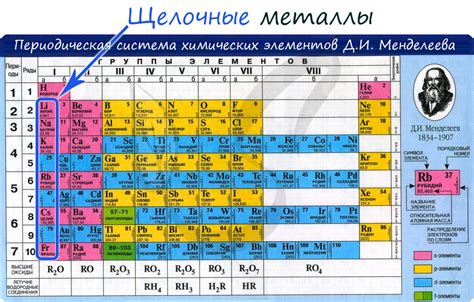
Щелочные металлы - это группа элементов периодической таблицы, которые обладают рядом общих характеристик. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Основное отличие щелочных металлов от кальция и радия заключается в их электрохимических свойствах. Щелочные металлы обладают низкой электроотрицательностью и они легко отдают свои внешние электроны, что делает их высокоактивными химическими элементами.
Кальций (Ca) и радий (Ra), несмотря на то, что они находятся в той же группе таблицы, не являются щелочными металлами. Кальций является щелочноземельным металлом, а радий - активным металлом, который является самым тяжелым из элементов группы щелочных металлов.
Кальций и радий отличаются от щелочных металлов своими физическими и химическими свойствами. Например, кальций имеет более высокую плотность и температуру плавления по сравнению с щелочными металлами. Радий, с другой стороны, является радиоактивным элементом, что делает его особенно опасным для жизни и здоровья человека.
Щелочные металлы широко используются в различных областях, таких как химическая промышленность, металлургия, электроника и медицина. Они обладают уникальными свойствами, такими как низкая плотность, высокая теплопроводность и реактивность, что делает их полезными для различных применений.
В заключение, хотя кальций и радий приближены к щелочным металлам в таблице, они все же имеют свои уникальные свойства, которые отличают их от этой группы элементов. Понимание этих различий важно для понимания химических и физических свойств данных элементов и их применения в науке и промышленности.
Что такое щелочные металлы и какова их основная химическая реакция?
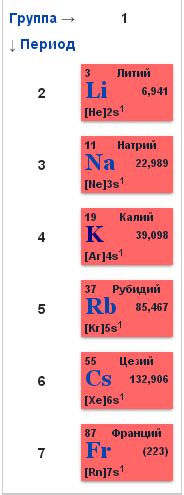
Щелочные металлы - это элементы периодической системы химических элементов, которые находятся в первой группе (семье) элементов. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они являются самыми низкими по плотности, самыми реактивными и самыми мягкими из всех металлов. Особенностями щелочных металлов являются низкая температура плавления и высокая химическая активность.
Основная химическая реакция, характерная для щелочных металлов, это реакция с водой. Когда щелочные металлы взаимодействуют с водой, происходит энергичное химическое взаимодействие, сопровождающееся выделением водорода и образованием щелочного гидроксида. Например, реакция натрия с водой выглядит следующим образом:
- 2Na + 2H2O → 2NaOH + H2
В результате этой реакции образуется щелочная соль, которая растворяется в воде, образуя щелочный раствор. Водород, выделяющийся при взаимодействии, обычно горит, поскольку он является горючим газом. Данная реакция с водой хорошо иллюстрирует и обосновывает классификацию данных элементов как щелочные металлы.
Почему кальций и радий не относятся к щелочным металлам?
Щелочные металлы - это группа элементов, которые находятся в первой группе периодической таблицы. Они имеют общие химические свойства, в том числе высокую активность и реактивность. Кальций и радий, хотя и относятся к блоку s периодической таблицы, не являются щелочными металлами из-за некоторых особенностей их свойств.
Кальций:
Кальций - это серебристо-белый металл, который является важным элементом в организме живых существ, а также широко используется в промышленности. Он обладает некоторыми характеристиками щелочных металлов, такими как мягкость и высокая температура плавления. Однако, кальций отличается от щелочных металлов тем, что он менее активен и не реагирует с водой так сильно, как щелочные металлы. Кроме того, кальций образует более стабильные соединения с другими элементами, что отличается от свойств щелочных металлов.
Радий:
Радий - это редкий радиоактивный элемент, который имеет очень высокую реактивность. Хотя радий находится в группе щелочных металлов, его радиоактивность и короткая продолжительность полураспада делают его непрактичным для практического использования. Кроме того, радий имеет низкую температуру плавления и парообразования, что также отличается от типичных свойств щелочных металлов.
В итоге, хотя кальций и радий обладают некоторыми характеристиками щелочных металлов, их более специфические свойства делают их не явными представителями данной группы элементов.
Вопрос-ответ

Какие элементы не являются щелочными металлами?
Кальций и радий не являются щелочными металлами.
Какие свойства отличают кальций и радий от щелочных металлов?
В отличие от щелочных металлов, кальций и радий имеют высокие температуры плавления и кипения, а также меньшую химическую активность.
Чем отличаются кальций и радий от щелочных металлов?
Кальций и радий отличаются от щелочных металлов своей высокой плотностью, более высокой температурой плавления и кипения, а также меньшей химической активностью.
Почему кальций и радий не являются щелочными металлами?
Кальций и радий не являются щелочными металлами из-за своих отличительных свойств, таких как высокая температура плавления и кипения, а также меньшая химическая активность по сравнению со щелочными металлами.
Каковы основные характеристики, отличающие кальций и радий от щелочных металлов?
Кальций и радий отличаются от щелочных металлов своей высокой плотностью, более высокой температурой плавления и кипения, а также меньшей химической активностью.
