Щелочные металлы — это группа химических элементов, включающая литий, натрий, калий, рубидий, цезий и франций. Эти металлы обладают рядом уникальных свойств, которые делают их весьма полезными в различных сферах науки и промышленности.
Прежде всего, щелочные металлы хорошо растворяются в воде и образуют щелочные растворы, что делает их незаменимыми в различных химических исследованиях. Благодаря своей высокой реактивности, они способны быстро взаимодействовать с другими веществами, что открывает широкие возможности для проведения химических экспериментов.
Кроме того, щелочные металлы широко используются в производстве батарей и аккумуляторов. Их высокая электропроводность и способность образовывать стабильные ионные соединения делают их идеальными материалами для создания энергетически эффективных источников питания. Благодаря этим свойствам, щелочные металлы используются во многих электронных устройствах, от мобильных телефонов до электрических автомобилей.
Также следует отметить, что щелочные металлы имеют широкое применение в медицине. Например, литий широко используется в лекарствах для лечения маниакально-депрессивных состояний и биполярного аффективного расстройства. Калий и натрий играют важную роль в работе нервной системы и сердечно-сосудистой системы. Использование щелочных металлов в медицине позволяет успешно решать множество проблем со здоровьем человека.
Щелочные металлы и их свойства

Щелочные металлы - это группа химических элементов, которые находятся в первой группе периодической таблицы. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы являются самыми реактивными металлами, что делает их полезными во многих областях науки и технологий.
Основное физическое свойство щелочных металлов - низкая плотность. Они являются легкими металлами с низкой точкой плавления и кипения. Например, литий имеет плотность всего 0,53 г/см³, что делает его самым легким металлом. Натрий и калий также имеют низкую плотность, что делает их удобными для использования в различных промышленных процессах.
Щелочные металлы обладают высокой реактивностью. Они легко соединяются с водой, образуя гидроксиды и выделяя водород. Этот процесс сопровождается сильным выделением тепла и возгоранием газа. Кроме того, щелочные металлы реагируют с кислородом, образуя оксиды и оксокислоты.
Щелочные металлы обладают хорошей проводимостью электричества и тепла. Они являются реактивными и легко вступают в химические реакции. Поэтому их часто используют в различных промышленных процессах, включая производство лития-ионных аккумуляторов, стекла, алюминия и цемента. Кроме того, щелочные металлы играют важную роль в биологических системах, так как они необходимы для нормального функционирования нервной системы и мышц организма.
Щелочные металлы и их особенности

Щелочные металлы - это группа химических элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются своими уникальными физическими и химическими свойствами.
Одной из особенностей щелочных металлов является их высокая реактивность. Они являются очень активными химическими элементами и легко вступают в реакцию с другими веществами. Это связано с тем, что у них всего один электрон во внешней электронной оболочке, что делает их нестабильными и стремящимися к окислению.
Еще одной особенностью щелочных металлов является их низкая плотность. Все щелочные металлы имеют плотность меньше 1 г/см³, что делает их легкими и удобными в использовании. Это также обусловлено их атомной структурой и электронной конфигурацией.
Щелочные металлы обладают высокой электропроводностью и теплопроводностью. Они хорошо проводят электричество и тепло, что делает их важными материалами в различных отраслях промышленности. Например, калий и натрий используются в производстве удобрений, а литий применяется в производстве аккумуляторов для электромобилей.
Также следует отметить, что щелочные металлы образуют сильные истощающие растворы. Они очень реактивны и растворяются в воде, образуя щелочные растворы. Это связано с их химическими свойствами и способностью образовывать ионы в растворе.
В целом, щелочные металлы представляют собой интересную группу химических элементов с разнообразными свойствами. Их уникальные химические и физические свойства позволяют им находить применение в различных областях науки и технологии.
Физические свойства щелочных металлов

Щелочные металлы представляют собой группу элементов, включающую литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются рядом физических свойств, которые делают их уникальными и полезными для различных приложений.
Первое заметное свойство щелочных металлов - активность. Они очень реактивны и легко реагируют с водой и кислородом воздуха. Например, натрий активно реагирует с водой, выделяя гидроген и образуя щелочную среду. Эта реакция является основой для создания иглы феникса - популярного химического опыта.
Второе важное свойство щелочных металлов - низкая плотность. Они являются самыми легкими металлами и имеют плотность, меньшую, чем у большинства других элементов. Это делает их полезными в аэрокосмической промышленности, где легкость материалов играет важную роль.
Еще одно интересное свойство щелочных металлов - способность образовывать сплавы с другими металлами. Например, сплавы калия и натрия широко используются в железнодорожной отрасли для создания высокопрочных и легких материалов.
Одним из наиболее заметных физических свойств щелочных металлов является их мягкость. Они мягкие и можно нарезать ножом, что делает их подходящими для использования в различных приложениях, таких как производство батареек и косметики.
Наконец, щелочные металлы обладают высокой электропроводностью. Они могут легко передавать электрический ток, что делает их важными для создания проводов и других электронных устройств.
Химические свойства щелочных металлов
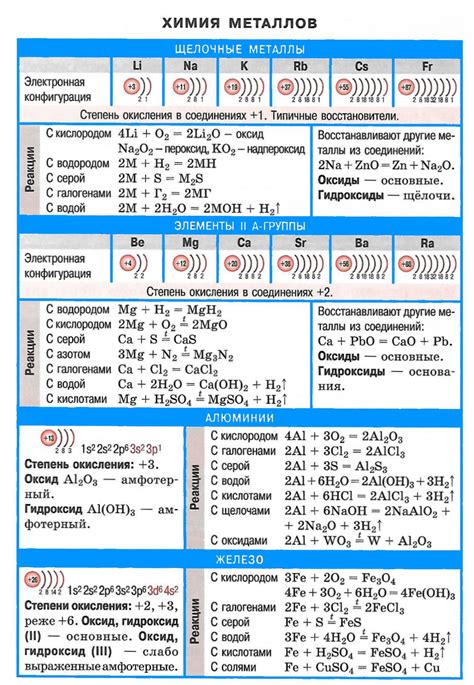
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, обладают уникальными химическими свойствами. Они являются самыми активными металлами в периодической системе элементов, и это связано с их низкой энергией ионизации.
Каждый из щелочных металлов сочетается с кислородом, образуя оксиды. Например, литий образует оксид Li2O, а калий образует оксид K2O. Оксиды щелочных металлов являются щелочными соединениями и способны реагировать с водой, образуя гидроксиды.
Натрий, калий и другие щелочные металлы образуют гидроксиды, такие как NaOH и KOH, которые широко используются в промышленности, например, в процессе производства мыла и стекла. Гидроксиды щелочных металлов обладают щелочной реакцией и могут растворять многие вещества.
Щелочные металлы имеют высокую реактивность и могут легко образовывать ионы с положительным зарядом. Они обладают способностью образовывать оксиды, гидроксиды и соли, что делает их важными компонентами во многих химических процессах.
Важно отметить, что щелочные металлы реагируют с водой, образуя газ водород и гидроксиды. Например, реакция калия с водой приводит к образованию гидроксида калия (KOH) и выделению водорода (H2). Это явление делает щелочные металлы полезными в процессе заводского производства, а также в производстве пищевых и фармацевтических продуктов.
Реактивность щелочных металлов
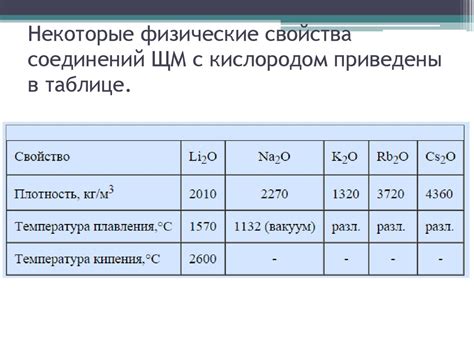
Щелочные металлы, такие как литий, натрий, калий и другие, обладают высокой реактивностью. Это связано с их низкой ионизационной энергией и способностью образовывать стабильные ионы положительного заряда. Щелочные металлы способны быстро вступать в реакцию с водой, сжигаться на воздухе и реагировать с другими веществами.
Реакция щелочных металлов с водой является одной из самых характерных для них. При контакте с водой металлы быстро реагируют, образуя щелочные растворы и выделяяся водород. Например, литий вступает в реакцию с водой, образуя литиевую щелочь и выделяя водородный газ. Это связано с тем, что вода диссоциирует и образует гидроксидные ионы, которые образуют раствор с положительно заряженными ионами щелочного металла.
Щелочные металлы также реагируют с кислородом воздуха, образуя оксиды металлов. Натрий, например, при контакте с кислородом образует оксид натрия (Na2O). При этом выделяется большое количество тепла. Этот процесс называется сжиганием щелочных металлов.
Щелочные металлы также могут реагировать с другими веществами, такими как хлор, сера и фосфор. Натрий, например, может реагировать с хлором, образуя хлорид натрия (NaCl). Такие реакции могут протекать с выделением большого количества энергии и тепла.
Применение щелочных металлов в технологиях

Щелочные металлы - это элементы группы 1 периодической системы, которые включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются высокой реактивностью и обладают рядом уникальных свойств, которые делают их ценными в различных технологиях.
Одной из ключевых областей применения щелочных металлов является электрохимическая источников энергии, такие как литиевые и натриевые ионные батареи. Литий-ионные батареи широко применяются в портативных электронных устройствах, таких как мобильные телефоны и ноутбуки, благодаря своей высокой энергетической плотности и длительному сроку службы. В то время как натриевые ионные батареи могут стать альтернативой литиевым, так как натрий является более доступным и дешевым элементом.
Щелочные металлы также находят применение в производстве стекла и керамики. Например, натрий используется для придания прозрачности и прочности стеклу, а калий является основным компонентом керамики и фарфора. Кроме того, щелочные металлы используются в производстве щелочных растворов и щелочных россыпей, которые широко применяются в процессах смачивания и очистки поверхностей в промышленности.
В ядерной энергетике щелочные металлы играют важную роль. Калий используется в качестве модератора в ядерных реакторах для замедления и контроля деления атомов. Кроме того, цезий и рубидий используются для производства источников радиационного излучения, которые находят применение в медицине и научных исследованиях.
Таким образом, применение щелочных металлов в технологиях охватывает широкий спектр областей, от энергетики до производства материалов и ядерной технологии. Их уникальные свойства делают их незаменимыми во многих процессах и служат основой для развития инновационных решений в различных областях промышленности и науки.
Использование щелочных металлов в медицине
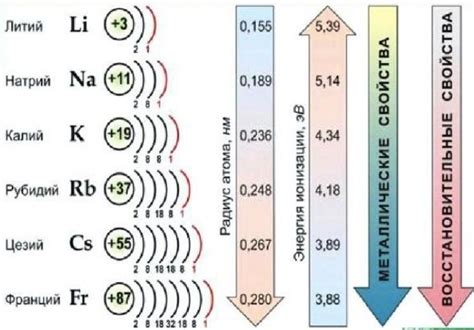
Щелочные металлы, такие как литий, натрий, калий и др., находят широкое применение в медицине благодаря своим полезным свойствам. Они активно использовались в лечении различных заболеваний и состояний человека.
Один из самых распространенных примеров использования щелочных металлов в медицинской практике - лечение биполярного аффективного расстройства. Литий является основным препаратом для этого заболевания. Его уникальные свойства помогают стабилизировать настроение пациента и уменьшить частоту эпизодов мании и депрессии.
Калий также является незаменимым элементом в медицине. Он играет важную роль в поддержании нормальных функций сердца, участвуя в проведении электрических импульсов. Препараты калия широко применяются для лечения сердечных аритмий и предотвращения повышения кровяного давления.
Значительное влияние на сохранение водно-солевого баланса и нормальной работы мышц оказывает натрий. Он применяется врачами для лечения гипонатриемии - состояния, при котором уровень натрия в организме снижается до опасного уровня. Поддержание нормального уровня натрия способствует нормализации осмотического давления и функционированию клеток организма.
Щелочные металлы также находят применение при лечении некоторых видов рака. Например, введение радиоактивного изотопа калия-цезия-137, который обладает свойствами ионного излучения, позволяет проводить брахитерапию - метод, при котором радиационная терапия проводится непосредственно внутри тканей опухоли, минимизируя воздействие на здоровые ткани.
В заключение, использование щелочных металлов в медицине обусловлено их уникальными свойствами и способностью оказывать положительное влияние на организм человека. Их применение в лечении различных заболеваний позволяет добиться эффективных результатов и улучшить качество жизни пациентов.
Проблемы использования щелочных металлов

Щелочные металлы, такие как литий, натрий и калий, имеют широкий спектр применений, однако их использование сопряжено с определенными проблемами.
Высокая реактивность: Щелочные металлы характеризуются высокой химической активностью, что делает их очень реактивными элементами. Они быстро реагируют с водой и воздухом, что может привести к возникновению опасных ситуаций при неправильном хранении или использовании.
Высокая стоимость: Некоторые щелочные металлы, такие как литий, являются редкими и дорогими элементами. Их добыча и производство также требуют особых технологий и ресурсов, что делает их использование в некоторых областях экономически нецелесообразным.
Необходимость специального обращения с отходами: Щелочные металлы могут быть вредными для окружающей среды и здоровья человека, поэтому требуется специальная обработка отходов, содержащих эти элементы. Неверная утилизация может привести к загрязнению воды, почвы и атмосферного воздуха.
Большая реакционность с другими веществами: Щелочные металлы могут реагировать с различными веществами, в том числе с кислотами или галогенами, образуя воспламеняемые или взрывоопасные соединения. Поэтому необходимо соблюдать особую осторожность при работе с ними, чтобы избежать несчастных случаев и аварий.
Ограниченные ресурсы: Некоторые щелочные металлы, особенно литий, не являются бесконечно доступными ресурсами. Необходимо соблюдать меры по энергосбережению, вторичной переработке и повторному использованию данных элементов, чтобы минимизировать негативное влияние на окружающую среду и сохранить их ресурсы для будущих поколений.
Новые технологии и исследования в области щелочных металлов

Щелочные металлы, такие как литий, натрий и калий, играют важную роль в современных технологиях и находят применение во многих отраслях. Новые исследования и технологии в области щелочных металлов позволяют сделать их использование более эффективным и устойчивым.
Одним из интересных направлений исследований является разработка более эффективных батарей на основе щелочных металлов. Новые материалы и конструкции позволяют увеличить емкость батарей, улучшить их стабильность и увеличить время работы. Это особенно актуально для электрических транспортных средств, где важно иметь батарею с большим запасом хода.
Другим перспективным направлением исследований является использование щелочных металлов в процессе производства водорода. Водород является энергоносителем будущего и может быть использован в различных отраслях, включая энергетику и транспорт. Новые технологии позволяют более эффективно производить водород из щелочных металлов, что делает этот процесс более доступным и экологичным.
Кроме того, исследователи изучают возможность использования щелочных металлов в различных электронных устройствах. Они работают над созданием новых материалов, которые можно использовать в производстве полупроводников, аккумуляторов и других электронных компонентов. Это открывает новые возможности для развития современной электроники и улучшения ее характеристик.
Таким образом, новые технологии и исследования в области щелочных металлов вносят значительный вклад в различные отрасли и способствуют развитию более эффективных и устойчивых технологий. Они помогают сделать использование щелочных металлов более эффективным, доступным и экологически безопасным.
Вопрос-ответ

Какие есть эффективные способы решения задач с использованием щелочных металлов?
Для решения задач с использованием щелочных металлов существует несколько эффективных способов. Один из них - использование щелочных металлов в качестве катализаторов в различных химических реакциях. Также, щелочные металлы могут использоваться в процессе производства электрической энергии, в частности, в батареях и аккумуляторах. Кроме того, с помощью щелочных металлов можно решать задачи по очистке отходов и загрязнений, так как они отлично реагируют с различными веществами и способны удалить даже самые стойкие загрязнения.
Какую роль играют щелочные металлы в производстве электрической энергии?
Щелочные металлы играют важную роль в производстве электрической энергии. Они используются в батареях и аккумуляторах, где являются одним из основных компонентов. Щелочные металлы, такие как литий, натрий и калий, обладают высокой энергоемкостью и способностью хорошо хранить электрический заряд. Благодаря этим свойствам, они позволяют батареям и аккумуляторам длительно работать без подзарядки, что делает их незаменимыми в различных устройствах, от мобильных телефонов до электрических автомобилей.
Какие еще полезные свойства имеют щелочные металлы?
Помимо своей роли в производстве электрической энергии, щелочные металлы обладают и другими полезными свойствами. Например, они очень реактивны и способны быстро реагировать с другими веществами, что делает их ценными катализаторами в различных химических процессах. Также, щелочные металлы хорошо растворяются в воде, что позволяет использовать их для очистки различных поверхностей и удаления загрязнений. Они также обладают низкой плотностью, что делает их легкими и удобными в использовании.
