Щелочные металлы – это группа элементов периодической системы, которые включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются высокой активностью и реакционной способностью, их соединения широко применяются в различных областях химии и техники.
Керосин – это легковоспламеняющаяся нефтяная фракция, которая используется в качестве топлива для авиационных двигателей и многих других технических целей. Однако, несмотря на свою высокую химическую активность, щелочные металлы не вступают в реакцию с керосином. Это связано с особенностями их химического строения и взаимодействия с другими веществами.
Взаимодействие щелочных металлов с керосином не происходит из-за различия в химической природе этих веществ. Щелочные металлы обладают высокой активностью и могут реагировать с многими веществами, но керосин не является одним из них. Он представляет собой смесь углеводородов, которая имеет сложную структуру и не обладает реакционной способностью по отношению к щелочным металлам.
Невозможность реакции щелочных металлов с керосином
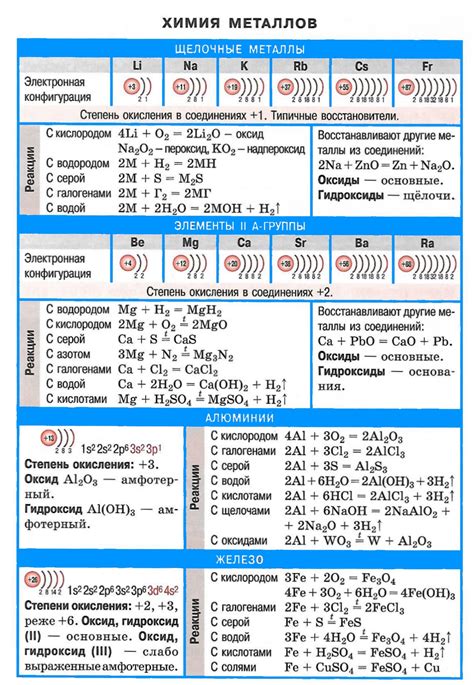
Щелочные металлы, такие как натрий и калий, обладают высокой активностью и реакционностью. Они способны взаимодействовать с различными веществами, образуя с ними химические соединения. Однако, керосин – это углеводородное соединение, которое является неполярным и не содержит активных функциональных групп.
Взаимодействие между щелочными металлами и керосином не происходит из-за отсутствия полярных химических связей в составе керосина. Щелочные металлы обладают большой аффинностью к электронам и способны образовывать ионные соединения с веществами, содержащими атомы, которые могут предоставить электроны.
Керосин состоит из углеродных и водородных атомов, которые образуют прочные неполярные связи. В результате, щелочные металлы не могут проникнуть внутрь молекулы керосина и вступить с ними в реакцию. Из-за этой неполярности и отсутствия активных функциональных групп, керосин не образует соединений с щелочными металлами.
Определение щелочных металлов

Щелочные металлы - это группа элементов периодической системы, относящаяся к первой группе и состоящая из лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Они характеризуются высокой реактивностью и способностью образовывать щелочные гидроксиды в воде.
Определение щелочных металлов можно провести по нескольким параметрам. Во-первых, они имеют низкую плотность и низкую температуру плавления, что делает их легкими для обработки и использования в различных промышленных процессах.
Кроме того, щелочные металлы обладают высокой электроотрицательностью и способностью образовывать ионы с положительным зарядом. Это позволяет им образовывать стабильные соли с отрицательными ионами других элементов.
Еще одним важным характеристикой щелочных металлов является их реакция с водой. Они образуют щелочные гидроксиды, которые обладают щелочными свойствами и широко используются в промышленности и быту.
Таким образом, определение щелочных металлов базируется на их химических свойствах, таких как низкая плотность, низкая температура плавления, высокая электроотрицательность и способность образовывать щелочные гидроксиды в воде.
Физические свойства керосина и щелочных металлов

Керосин - это жидкое топливо, которое получают из нефти с помощью специальной переработки. Он обладает рядом характеристик, которые делают его удобным и эффективным для использования в различных отраслях промышленности и транспорте.
Основные физические свойства керосина включают его прозрачность, низкую вязкость и относительно низкую температуру замерзания. Именно благодаря этим характеристикам керосин обладает способностью легко перетекать и сжигаться в различных условиях.
Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, характеризуются наличием свободных электронов в своей валентной оболочке. Они обладают низкой плотностью, низкой температурой плавления и относительно мягкой структурой.
Одной из важных характеристик щелочных металлов является их активность, то есть способность вступать в реакцию с другими веществами. Однако, несмотря на свою высокую реакционность, щелочные металлы не реагируют с керосином.
Причина отсутствия реакции между керосином и щелочными металлами связана с их химической структурой. Щелочные металлы образуют ионы положительного заряда, которые обычно вступают в реакцию с веществами, содержащими ионы отрицательного заряда. Керосин же, в свою очередь, является нейтральным веществом, не содержащим заряженных частиц.
Таким образом, физические свойства керосина и щелочных металлов определяют их поведение в химических реакциях. Взаимодействие керосина с щелочными металлами не происходит из-за отсутствия совпадения зарядов ионов.
Химическое взаимодействие щелочных металлов и керосина

Щелочные металлы, такие как литий, натрий и калий, обладают химическими свойствами, которые отличают их от других элементов. В частности, они обладают высокой реакционной способностью и могут взаимодействовать с различными веществами.
В отношении керосина, слабо окисляющего вещества, щелочные металлы не проявляют химической реакции.
Это можно объяснить тем, что керосин - это смесь углеводородов, а щелочные металлы обладают свойством реагировать с водой или другими веществами, содержащими активные группы, такие как кислород или азот.
При взаимодействии с водой, ѩелочные металлы образуют гидроксиды с образованием газа в виде пузырьков, такой реакции не происходит при соприкосновении с керосином.
Таким образом, химическое взаимодействие между щелочными металлами и керосином ограничивается абсорбцией, то есть простым поглощением щелочными металлами керосина без образования химических соединений.
Безопасность использования керосина с щелочными металлами
Керосин — это легковоспламеняющееся вещество, которое широко используется в различных областях человеческой деятельности, включая домашнюю и промышленную сферы. При использовании керосина рекомендуется соблюдать определенные меры безопасности, особенно при работе с щелочными металлами.
Щелочные металлы, такие как натрий, калий и литий, имеют свойства, способные вызывать реакцию с воспламеняющимися веществами, включая керосин. При контакте керосина с щелочными металлами, возможно возгорание или даже взрыв.
Для обеспечения безопасности при обращении с керосином и щелочными металлами необходимо соблюдать ряд предосторожностей. Во-первых, рекомендуется хранить керосин и щелочные металлы в отдельных упаковках или контейнерах, чтобы предотвратить их случайное соприкосновение. Во-вторых, при работе с керосином руками следует использовать защитные перчатки, чтобы избежать контакта с кожей и предотвратить возможное воспламенение.
Также рекомендуется хранить керосин в прохладных и хорошо проветриваемых помещениях, вдали от источников тепла и огня. При использовании керосина с щелочными металлами, не стоит пренебрегать правилами пожарной безопасности и иметь под рукой средства для тушения возможного пожара, такие как огнетушитель или воду.
Однако, несмотря на потенциальную опасность, при соблюдении указанных мер безопасности риск возгорания или взрыва при использовании керосина с щелочными металлами минимален. Важно ответственно подходить к использованию данных веществ и всегда быть готовыми к предотвращению и ликвидации возможных происшествий.
Альтернативные химические реакции с щелочными металлами
Щелочные металлы, такие как литий (Li), натрий (Na) и калий (K), известны своей реактивностью и способностью взаимодействовать с различными веществами. Однако, несмотря на то, что они обычно не реагируют с керосином, существуют альтернативные химические реакции, которые металлы могут претерпеть.
Одной из возможных реакций щелочных металлов является их реакция с водой. Когда щелочные металлы погружаются в воду, они быстро реагируют, выделяя водород. Эта реакция является экзотермической, то есть сопровождается выделением тепла. Например, литий при контакте с водой образует гидроксид лития и выделяет водородный газ.
Другой альтернативной реакцией щелочных металлов может быть их взаимодействие с кислородом. Например, натрий может реагировать с кислородом из воздуха, образуя оксид натрия. Это происходит при достаточно высокой температуре, например, при нагревании натрия в открытой атмосфере. Образовавшийся оксид натрия может иметь различные применения в промышленности.
Также щелочные металлы могут реагировать с некоторыми кислотами, образуя соли. Например, калий может реагировать с соляной кислотой, образуя хлорид калия и выделяя водород. Эта реакция используется в лабораторных условиях для получения соли калия.
Однако, реакция щелочных металлов с керосином на практике обычно не происходит. Керосин не содержит активных функциональных групп, способных провести реакцию с щелочными металлами. Таким образом, альтернативные химические реакции с щелочными металлами чаще происходят с другими веществами, такими как вода и кислород.
Вопрос-ответ

Какие щелочные металлы не реагируют с керосином?
Все щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, не провоцируют реакцию с керосином.
Почему щелочные металлы не реагируют с керосином?
Щелочные металлы не реагируют с керосином из-за своей химической природы. Они обладают низкой электроотрицательностью и не проявляют активность в реакциях с органическими соединениями, такими как керосин.
Можно ли использовать керосин в присутствии щелочных металлов?
Да, керосин безопасно использовать в присутствии щелочных металлов, так как они не вызывают реакций с ним.
Каковы особенности взаимодействия керосина с щелочными металлами?
Взаимодействие керосина с щелочными металлами не происходит в силу различия в их химических свойствах. Керосин является органическим веществом, а щелочные металлы обладают гидроксидами, которые могут реагировать только с кислотами, и не обладают активностью в отношении органических соединений.
Может ли реагировать керосин с другими типами металлов?
Керосин может реагировать с некоторыми другими типами металлов, особенно активными металлами, такими как щелочно-земельные металлы (кальций, магний и т. д.). Однако керосин не реагирует с щелочными металлами, такими как литий, натрий, калий и др.
