Щелочноземельные металлы — это группа элементов в периодической таблице, которая включает гелий, бериллий, магний, кальций, стронций, барий и радий. В данном конспекте урока мы рассмотрим основные свойства и применение данных элементов в различных областях нашей жизни.
Первым элементом щелочноземельных металлов является гелий, который обладает атомным номером 2. Этот элемент является безцветным, негорючим и инертным газом. Бериллий, второй элемент этой группы, обладает высокой прочностью и легкостью, поэтому успешно применяется в производстве летательных аппаратов и спутников связи.
Магний, третий элемент этой группы, широко используется в автомобильной промышленности, так как способен взаимодействовать с кислородом и способствовать понижению воспламеняемости топливных смесей. Кальций, стронций и барий применяются в медицине, в частности, для рентгенологических исследований и получения изображений костной системы человека.
Радий является самым тяжелым и менее стабильным элементом в этой группе. Его использование ограничено из-за его радиоактивности, однако он находит применение в исследованиях по радиоактивности и в медицине для радиотерапии различных видов рака.
Химические элементы в 9 классе: основные их свойства

1. Металлы:
- Щелочные металлы: литий, натрий, калий, рубидий, цезий, франций. Они имеют малую плотность, низкую температуру плавления и кипения, способны реагировать с водой, образуя щелочные растворы.
- Щелочноземельные металлы: бериллий, магний, кальций, стронций, барий, радий. Они более твердые и плотные, чем щелочные металлы, образуют оксиды, сильные основания и растворы солей.
- Тяжелые металлы: железо, медь, цинк, свинец, марганец, никель. Они обладают высокой плотностью, твердостью и тугоплавкостью, многие из них имеют радиоактивные изотопы.
2. Неметаллы:
- Водород: самый легкий элемент, входит в состав воды и числа органических соединений.
- Кислород: образует оксиды, растворимые в воде, недорогой живительный газ.
- Углерод: ключевой элемент органической химии, образует огромное количество соединений.
- Азот: основной компонент атмосферы Земли, входит в состав многих питательных веществ.
- Фосфор: необходимый элемент для роста и развития организмов, является ключевым в составе ДНК и РНК.
3. Полуметаллы:
- Кремний: применяется в электронике и солнечных батареях, является важным элементом для живых организмов.
- Бор: применяется в производстве стекол, ядерных реакторах и лекарственных препаратах.
- Сурьма: используется в производстве полупроводниковых материалов и других технологических процессах.
4. Инертные газы:
- Гелий: использование в заполнении атмосферы воздушных шаров и в процессе охлаждения.
- Неон: применяется в световых рекламных установках и лазерах.
- Аргон: используется в заполнении ламп для сварки и веществ, требующих защиты от окисления.
Изучение основных свойств различных химических элементов в 9 классе позволяет ученикам получить представление о разнообразии и важности элементов в химических реакциях и повседневной жизни. Знание их химических свойств дает возможность понять, какие реакции они могут совершать, какие соединения образуют и какие функции выполняют в различных системах и процессах.
Осознание таблицы Менделеева: простые и лёгкие металлы
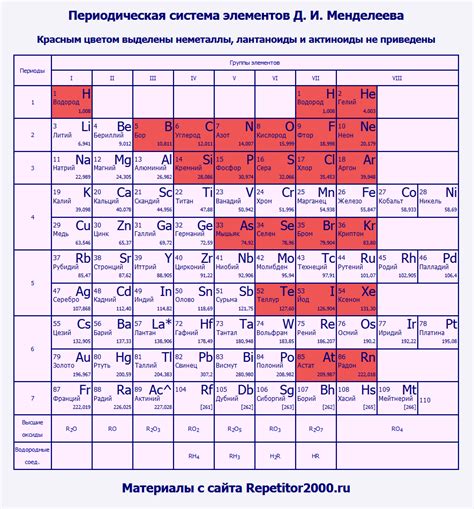
В ходе изучения химии в школе ученики знакомятся с таблицей Менделеева. Эта таблица представляет собой удобную и систематическую классификацию химических элементов. Осознание таблицы Менделеева позволяет лучше понять строение атомов и их свойства.
Одна из групп элементов в таблице Менделеева называется щелочноземельные металлы. Щелочноземельные металлы находятся во второй группе таблицы и включают шесть элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают рядом общих свойств. Во-первых, они являются лёгкими металлами. Это означает, что они обладают низкой плотностью и хорошей ударопрочностью. Благодаря этим свойствам щелочноземельные металлы широко используются в промышленности, строительстве и электронике.
Во-вторых, щелочноземельные металлы образуют щелочные оксиды в реакции с кислородом. Щелочные оксиды обладают щелочными свойствами и растворяются в воде, образуя щелочные растворы. Это свойство делает щелочноземельные металлы важными в химической промышленности и сельском хозяйстве.
- Бериллий - лёгкий металл, используется для производства сплавов и ядерных реакторов.
- Магний - важный элемент для нашего организма, используется в производстве сплавов и легких металлических конструкций.
- Кальций - основной компонент костей и зубов, используется в производстве цемента и стекла.
- Стронций - используется в ядерной энергетике и производстве световых приборов.
- Барий - используется в медицине и производстве стекла.
- Радий - радиоактивный элемент, используется в исследованиях и лучевой терапии.
В заключение, осознание таблицы Менделеева и разбирательство внутреннего устройства атомов позволяет лучше понять исследования в области химии и применение различных элементов в промышленности и повседневной жизни.
Щелочноземельные металлы: строение, характеристики и применение

Щелочноземельные металлы – это группа химических элементов, которые находятся во второй группе периодической таблицы. К этой группе относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Щелочноземельные металлы являются мягкими, относительно активными веществами с низкой плотностью.
Строение атомов щелочноземельных металлов характеризуется наличием двух электронов в внешней оболочке, что делает их наклонными к образованию ионов с положительным зарядом. Эти металлы обладают высокой теплопроводностью и являются химически активными веществами.
Важной характеристикой щелочноземельных металлов является их реактивность. Они легко реагируют с водой, кислотами и некоторыми другими веществами. Это свойство делает их полезными во многих промышленных процессах, включая производство металлургических сплавов, алюминия, магния и других металлов. Они также используются в производстве стекла, керамики, лекарственных средств и косметических продуктов.
Щелочноземельные металлы также играют важную роль в биологических системах. Например, кальций является ключевым компонентом костей и зубов, а магний необходим для нормального функционирования многих ферментов и мышц. Бериллий, хотя и является токсичным веществом, используется в некоторых медицинских технологиях, включая рентгеновскую ионизационную терапию.
В заключение, щелочноземельные металлы являются важными химическими элементами с множеством применений в различных отраслях науки и промышленности. Их характеристики, такие как мягкость, реактивность и способность образовывать ионы, делают их неотъемлемой частью современной жизни.
Урок по Габриеляну: практические эксперименты с щелочноземельными металлами

На уроке по химии мы провели интересные и познавательные практические эксперименты с щелочноземельными металлами.
Щелочноземельные металлы – это элементы второй группы периодической системы: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они обладают рядом уникальных свойств и являются важными для нашей жизни.
Первым экспериментом было определение металлических свойств щелочноземельных металлов. Мы получили небольшие образцы каждого металла и исследовали их физические свойства. Они оказались мягкими, легкими и обладали серебристым блеском.
Далее мы провели эксперимент с водой. Мы опустили образцы металлов в контейнеры с водой и наблюдали, что бериллий и магний реагируют с водой, выделяя газ. Кальций и барий реагируют с водой более интенсивно, происходит выделение водорода и образование гидроксидов. Стронций и радий не реагируют с водой.
В заключение урока мы провели опыт с пламенем. Мы подожгли образцы металлов и наблюдали окраску пламени. Каждый металл давал своеобразную окраску, что связано с выделением характеристических энергонавантов при сгорании металлов.
Такие практические эксперименты помогли нам лучше понять свойства и химическую активность щелочноземельных металлов.
Вопрос-ответ

Каково происхождение названия щелочноземельные металлы?
Название "щелочноземельные металлы" происходит от слов "щелочные" и "земельные". Щелочноземельные металлы получили такое название потому, что они реагируют с водой, образуя щелочь, и находятся в земной коре.
Каковы основные свойства щелочноземельных металлов?
Основные свойства щелочноземельных металлов: высокая химическая реактивность, низкая температура плавления, низкая плотность, мягкость и низкая твердость.
В чем состоит роль щелочноземельных металлов в природе?
Щелочноземельные металлы являются важными компонентами земной коры и играют важную роль в биологических процессах. Они участвуют в формировании почвы и влияют на рост растений.
Какие применения имеют щелочноземельные металлы?
Щелочноземельные металлы находят применение в различных отраслях промышленности. Например, магний используется в автомобильной и авиационной промышленности, кальций -- в строительстве и производстве стекла, а бериллий -- в производстве электроники.
Какие опасности сопряжены с использованием щелочноземельных металлов?
Щелочноземельные металлы могут быть опасными при неправильном обращении с ними. Некоторые из них, например, бериллий, являются токсичными и могут вызывать заболевания легких. Также они могут быть пирофорными, то есть воспламеняться при контакте с воздухом.
