Щелочноземельные металлы представляют собой вторую группу периодической таблицы химических элементов. В данную группу входят шесть элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы обладают рядом сходных свойств, которые делают их схожими как по химическим, так и по физическим характеристикам.
Щелочноземельные металлы обладают химическими свойствами, которые отличаются от свойств элементов первой группы – щелочных металлов, но при этом они все же сохраняют некоторые общие черты. Все металлы данной группы обладают двумя электронами в своей внешней электронной оболочке и, соответственно, обладают положительным зарядом. Кроме того, они являются химически активными элементами и способны легко образовывать соединения с другими химическими элементами.
Свойства щелочноземельных металлов делают их полезными в различных областях науки и промышленности. Например, бериллий широко используется в производстве сплавов и специальной электроники, а магний обладает высокой прочностью и легкостью, поэтому его часто используют в авиационной и автомобильной промышленности.
Группа щелочноземельных металлов в периодической таблице находится под группой щелочных металлов и над группой элементов, принадлежащих к группе переходных металлов. Важно отметить, что химические и физические свойства щелочноземельных металлов определяются их положением в периодической таблице и особенностями их внутреннего строения атомов.
Щелочноземельные металлы:
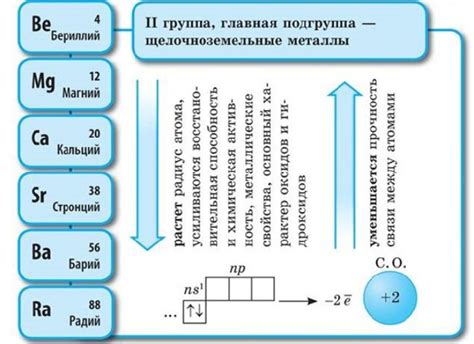
Щелочноземельные металлы – это группа элементов, которая находится во второй группе периодической таблицы Менделеева. Они включают в себя бериллий, магний, кальций, стронций, барий и радий. Химические свойства этих металлов характеризуются присутствием двух электронов на внешней энергетической оболочке.
Из-за своих свойств щелочноземельные металлы являются хорошими проводниками электричества и тепла. Они мягкие, легко отдают электроны и образуют ионы с положительным зарядом. Эти металлы отличаются хорошей реактивностью, особенно с кислородом и водой.
Щелочноземельные металлы имеют широкое применение в различных областях, таких как металлургия, электроника, строительство и медицина. Бериллий, например, используется для производства ядерных реакторов, а магний – для создания легких сплавов. Кальций является важным элементом для строения костей и зубов, а барий используется в рентгенологии для получения качественных изображений.
Однако некоторые щелочноземельные металлы, такие как бериллий и стронций, могут иметь токсическое воздействие на человека и окружающую среду, поэтому их использование требует особой осторожности и контроля.
Определение и свойства

Щелочноземельные металлы представляют собой группу химических элементов, входящих во второй группе периодической таблицы.
К ним относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы располагаются сразу за щелочными металлами и обладают схожими характеристиками.
Основные свойства щелочноземельных металлов включают высокую электропроводность, мягкость, низкую плотность и химическую активность.
- Бериллий – легковоспламеняемый металл, обладающий высокой термической и электрической проводимостью. Он также является прочным и легким материалом.
- Магний – легкий, огнеупорный металл, который широко используется в авиации и машиностроении.
- Кальций – сильно реактивный металл, используемый в производстве стали и в качестве дополнительного питания для растений.
- Стронций – мягкий, серебристый металл, который используется в производстве огней фейерверков и посуды для ядерных реакторов.
- Барий – мягкий и реактивный металл, который находит применение в производстве стекла, электродов и медицинской диагностики.
- Радий – радиоактивный металл, который имеет очень короткое полувремя распада и используется в научных и медицинских исследованиях.
Все щелочноземельные металлы реагируют с водой и кислородом, образуя оксиды и гидроксиды. Они также обладают тенденцией к образованию ионов с положительным зарядом.
Щелочноземельные металлы являются важными элементами в нашей жизни, применяемыми в различных отраслях промышленности и науки.
Расположение в периодической таблице
Щелочноземельные металлы представлены второй группой периодической таблицы Менделеева. Эта группа находится слева от группы благородных газов и включает в себя шесть элементов: магний (Mg), кальций (Ca), стронций (Sr), барий (Ba), радий (Ra) и рентгений (Rf).
В периодической таблице эти элементы расположены под литием (Li) и над бором (B). Они образуют группу с тугоплавкими металлами и являются переходом от щелочных металлов к плавким металлам.
Элементы группы щелочноземельных металлов имеют характерные свойства, такие как относительно низкая электроотрицательность, высокая реактивность и образование окислов с двойным зарядом. Они также характеризуются металлическим блеском и способностью легко образовывать ионы положительного заряда.
Важно отметить, что в данной группе элементов электроотрицательность и плотность металлов возрастают с увеличением атомного номера. Например, магний обладает меньшей электроотрицательностью и плотностью по сравнению с радием.
Щелочноземельные металлы находят широкое применение в различных областях, таких как металлургия, строительство, медицина и электроника. Их соединения используются как катализаторы, дополнительное питание для растений, добавки в лекарства и многое другое.
Группа щелочноземельных металлов

Щелочноземельные металлы — это группа элементов в периодической таблице, которая расположена сразу после группы щелочных металлов. Они включают в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Группа щелочноземельных металлов отличается от группы щелочных металлов тем, что они имеют два электрона в своей внешней электронной оболочке. Это делает их более реактивными, чем их щелочные соседи.
Щелочноземельные металлы обладают множеством различных химических свойств и имеют широкий спектр применений. Например, бериллий используется в производстве легких и прочных сплавов, магний — в авиационной и автомобильной промышленности, кальций — в производстве стали и строительстве.
Они также являются важными элементами для живых организмов. Кальций, например, необходим для костей и зубов, а магний — для работы многих ферментов в организме.
Щелочноземельные металлы имеют гладкую поверхность и серебристо-белый цвет. Они реагируют с водой, образуя щелочные растворы и выделяя водород. Они также образуют соединения с другими элементами, такие как оксиды и гидроксиды.
- Бериллий (Be) является легким и жестким металлом, который используется в производстве промышленных сплавов.
- Магний (Mg) используется в авиации, автомобильной промышленности и в производстве огнеупорных материалов.
- Кальций (Ca) является необходимым элементом для роста и развития растений, а также для здоровых костей у людей.
- Стронций (Sr) используется в производстве пиротехнических смесей и в ядерной энергетике.
- Барий (Ba) используется в медицинских исследованиях, также в промышленности для производства стекла и керамики.
- Радий (Ra) является радиоактивным элементом и используется в медицинской терапии и в исследованиях ядерных реакций.
Щелочноземельные металлы играют важную роль в промышленности, науке и жизни в целом. Их уникальные свойства делают их важными для различных технологий и приложений.
Основные представители

Щелочноземельные металлы – группа химических элементов, состоящая из 6 элементов: магний (Mg), кальций (Ca), стронций (Sr), барий (Ba), ридий (Ra) и уннилпентиум (Upt). Все эти элементы находятся во второй группе периодической таблицы химических элементов и имеют атомные номера от 12 до 118.
Основные представители щелочноземельных металлов имеют много общих химических свойств. Они, в основном, относятся к металлам средней жесткости, хорошо проводят электричество и тепло, а также обладают невысокой плотностью. Эти элементы образуют двувалентные положительные ионы, т.е. теряют два электрона, образуя стабильные положительные заряды.
Магний является наиболее легким из всех представителей группы щелочноземельных металлов. Он широко применяется в промышленности благодаря своим физическим и химическим свойствам. Кальций в основном извлекается из месторождений природных солей, и используется, например, в производстве строительных материалов. Стронций включен в состав различных материалов, используемых в электронике и оптике.
Барий, благодаря своим рентгеноконтрастным свойствам, применяется в медицине, например, для проведения рентгенологических исследований. Ридий используется в литейной промышленности, а его сплавы находят применение в изготовлении специальных инструментов. Уннилпентиум является искусственным элементом и может быть получен только в лабораторных условиях.
Химические свойства щелочноземельных металлов

Щелочноземельные металлы - это группа элементов в периодической таблице, которая включает в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они расположены во второй группе и имеют сходные химические свойства.
Важной особенностью щелочноземельных металлов является их способность образовывать двухвалентные положительные ионы. Они обладают двумя электронами в своей внешней энергетической оболочке, что делает их более реактивными, чем щелочные металлы.
При взаимодействии с кислородом, щелочноземельные металлы образуют оксиды, такие как оксид бериллия (BeO), оксид магния (MgO) и оксид кальция (CaO). Эти соединения являются щелочно-земельными оксидами и обладают щелочными свойствами.
Щелочноземельные металлы также реагируют с водой, образуя соответствующие гидроксиды. Например, реакция магния с водой приводит к образованию гидроксида магния (Mg(OH)2) и выделению водорода.
В реакциях с кислотами щелочноземельные металлы образуют соли. Например, реакция кальция с соляной кислотой приводит к образованию хлорида кальция (CaCl2).
Щелочноземельные металлы являются хорошими проводниками электричества благодаря наличию двух электронов в своей внешней энергетической оболочке. Они также характеризуются высокой температурой плавления и плотностью.
Выводя свои свойства в таблицу, можно отметить, что щелочноземельные металлы реактивны, образуют оксиды и гидроксиды при взаимодействии с водой и кислотами. Они являются хорошими проводниками электричества и обладают высокой температурой плавления и плотностью.
Применение щелочноземельных металлов
Щелочноземельные металлы – это группа элементов в периодической таблице, которые включают бериллий, магний, кальций, стронций, барий и радий. Эти металлы обладают рядом уникальных свойств, что делает их полезными и важными в различных областях промышленности и научных исследований.
Один из самых широко применяемых щелочноземельных металлов – магний. У него легкий вес и хорошие механические свойства, поэтому он используется в авиационной и автомобильной промышленности для создания легких и прочных сплавов. Магний также используется при производстве спортивных товаров, таких как велосипеды и гольф-клюшки, благодаря своей легкости и прочности.
Другой важный щелочноземельный металл – кальций. Он широко используется в строительстве, так как его соединения придают прочность бетону и используются для производства цемента. Кальций также используется в производстве стекла и сплавов, а его соединения используются в медицине для лечения заболеваний связанных с недостатком этого элемента в организме.
Бериллий, один из самых легких щелочноземельных металлов, обладает высокой коррозионной стойкостью и является отличным проводником тепла и электричества. Это делает его незаменимым в производстве электроники, такой как компьютеры, мобильные телефоны и другие электронные устройства. Бериллий также используется в ядерной индустрии, а его соединения применяются в медицине для диагностики рака.
Стронций и барий применяются в производстве ярких светящихся красок и пигментов, которые используются в флуоресцентных лампах и светодиодах. Эти металлы также используются в производстве стекла и керамики, а их соединения находят применение в медицинской диагностике и радиотерапии.
Щелочноземельные металлы имеют широкий спектр применения и являются важными материалами в различных отраслях промышленности и научных исследованиях. Их уникальные свойства делают их незаменимыми в создании легких, прочных сплавов, производстве электроники, строительстве, медицине и других областях.
Биологическая роль щелочноземельных металлов

Щелочноземельные металлы играют важную биологическую роль в организмах живых существ. Они необходимы для многих процессов, связанных с обменом веществ и функционированием различных органов и систем организма.
Кальций, один из щелочноземельных металлов, является основной составной частью костей и зубов человека. Он также играет роль в сократительной активности мышц, передаче нервных импульсов и свертываемости крови. Недостаток кальция может привести к остеопорозу, нарушению сердечно-сосудистой системы и другим проблемам со здоровьем.
Магний, еще один щелочноземельный металл, является важным компонентом ферментов, участвующих в регуляции обмена веществ. Он также играет роль в передаче нервных импульсов, сокращении мышц и поддержании здоровья сердца. Недостаток магния может привести к мышечным судорогам, повышенной раздражительности и другим негативным последствиям.
Стронций, еще один щелочноземельный металл, может замещать кальций в костях и зубах. Он также может участвовать в обмене кальция в организме. Стронций может быть использован в медицине для облучения опухолей при лечении рака.
Общая биологическая роль всех щелочноземельных металлов связана с участием в процессах синтеза и разрушения молекул, передаче нервных импульсов, сокращении мышц и поддержании здоровья различных органов и систем организма.
Вопрос-ответ

Какие металлы относятся к группе щелочноземельные металлы?
К группе щелочноземельные металлы относятся следующие элементы: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Какие особенности характерны для щелочноземельных металлов?
Щелочноземельные металлы обладают свойствами, такими как мягкость, низкая плотность, низкая температура плавления и кипения, а также высокая химическая активность. Они реагируют с водой с образованием щелочей и обладают высокой электропроводностью.
Для чего используются щелочноземельные металлы?
Щелочноземельные металлы имеют различные применения. Например, бериллий используется в производстве сплавов и металлических конструкций, магний применяется в авиационной и автомобильной промышленности, кальций используется в производстве цемента и медицине, стронций применяется в цветных телеэкранах, барий используется в производстве стекла и радий применяется в радиотерапии и исследованиях ядерного разделения.
Какие соединения могут образовывать щелочноземельные металлы?
Щелочноземельные металлы могут образовывать соединения со многими другими элементами. Например, они образуют оксиды (например, оксид бериллия - BeO), гидроксиды (например, гидроксид магния - Mg(OH)2), хлориды (например, хлорид кальция - CaCl2) и многое другое.
Какова роль щелочноземельных металлов в живых организмах?
Некоторые щелочноземельные металлы играют важную роль в живых организмах. Например, кальций является необходимым элементом для строительства костей и зубов, магний участвует в активации многих ферментов и позволяет нервной системе нормально функционировать, барий используется в рентгенологии для повышения контрастности изображений.
