Электронная формула внешнего уровня щелочного металла представляет собой абстрактную запись, которая показывает количество электронов во внешней оболочке атома щелочного металла. Внешняя оболочка включает последние энергетические уровни и определяет химические свойства элемента. Щелочные металлы, такие как литий, натрий и калий, относятся к первой группе периодической системы элементов и характеризуются одной валентной электронной оболочкой.
Внешняя оболочка щелочных металлов всегда содержит один электрон. Они способны легко отдавать внешний электрон и образовывать положительные ионы с зарядом +1. Это явление объясняется наличием одного электрона в свободной s-орбитали на внешнем энергетическом уровне. Такая способность щелочных металлов образовывать ионы является причиной их проявления на химических реакциях и использование в различных областях науки и промышленности.
Электронная формула внешнего уровня щелочного металла позволяет ученым легче изучать их свойства и взаимодействия с другими веществами. Она представляет собой абстрактную запись, где валентный электрон представлен значком "e-", а внешний уровень обозначается как последний энергетический уровень других оболочек, разделенных нижними индексами. Например, электронная формула натрия будет выглядеть как " [Ne] 3s1", где "[" и "]" обозначают внешний уровень, а "Ne" - электронную конфигурацию аргоновой оболочки. Такая запись позволяет быстро определить количество электронов во внешнем энергетическом уровне и понять основные свойства щелочных металлов.
Определение и значение

Электронная формула внешнего уровня щелочного металла — это химическая формула, которая показывает состояние и количество электронов на внешнем энергетическом уровне атома щелочного металла. Внешний энергетический уровень, также известный как валентный уровень, играет ключевую роль в реакциях и свойствах атома.
Значение электронной формулы внешнего уровня щелочного металла заключается в том, что она позволяет определить, сколько электронов доступно для связывания с другими атомами. Щелочные металлы отличаются наличием одного электрона на внешнем уровне, что делает их очень реакционноспособными. Это, в свою очередь, делает их важными компонентами множества химических соединений и материалов.
Зная электронную формулу внешнего уровня щелочного металла, можно определить, какие ионы и соединения он может образовывать. Эта информация имеет практическое применение в различных областях, включая химическую промышленность, материаловедение и электронику.
Важно отметить, что электронная формула внешнего уровня щелочного металла может меняться в зависимости от условий и окружающей среды. Присутствие других веществ и условий реакции может привести к изменению количества связей и электронов на внешнем уровне. Поэтому электронная формула внешнего уровня щелочного металла должна рассматриваться в контексте конкретных условий и свойств вещества.
Строение атома щелочного металла
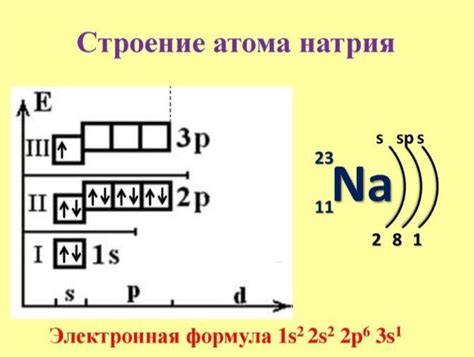
Атом щелочного металла представляет собой сложную систему, состоящую из ядра и электронной оболочки. Ядро атома находится в его центре и состоит из протонов, обладающих положительным зарядом, и нейтронов, не имеющих заряда.
Электронная оболочка атома щелочного металла состоит из электронов, которые обращаются на определенных орбиталях или энергетических уровнях вокруг ядра. Первый энергетический уровень может вместить не более 2 электронов, второй — не более 8, третий — не более 18 и так далее.
Электроны на внешнем энергетическом уровне называются валентными электронами. Для щелочных металлов внешний энергетический уровень может вместить не более 1 электрона.
Электронная формула внешнего уровня щелочного металла показывает количество валентных электронов на его внешней оболочке. Например, у лития на внешней оболочке находится 1 электрон, у натрия – 1 электрон, у калия – также 1 электрон.
Электронная формула внешнего уровня
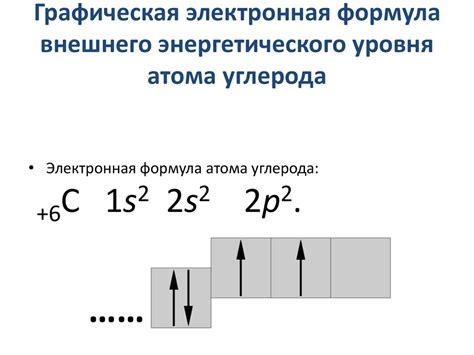
У атомов щелочных металлов внешний электронный уровень обладает свойством быть наиболее удаленным от ядра и содержит только один электрон. Внешний электрон заполняет s-подуровень.
Электронная формула внешнего уровня для атома щелочного металла может быть представлена в форме общей формулы "s1", где "s" указывает на наличие одного электрона, а число "1" обозначает количество электронов на данном уровне.
Например, у атома лития атомный номер равен 3, что означает, что у него есть 3 электрона. Внешний уровень атома лития содержит только один электрон, следовательно, его электронная формула внешнего уровня будет "s1".
Также стоит отметить, что у всех атомов щелочных металлов электронная формула внешнего уровня будет иметь такой же вид - "s1", так как число электронов на внешнем уровне всегда равно одному.
Общие принципы определения

Электронная формула внешнего уровня щелочного металла описывает распределение электронов в атомах этого металла на самом высокоэнергетическом уровне. Щелочные металлы относятся к первой группе периодической системы и состоят из элементов: лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Каждый из этих элементов имеет один электрон на внешнем энергетическом уровне, несмотря на различную зарядность ядра.
Основной принцип определения электронной формулы внешнего уровня щелочного металла основывается на расположении элемента в периодической системе. Так, внешний энергетический уровень щелочных металлов содержит один электрон в с оболочке соответствующего атома. Например, в атоме лития на внешнем энергетическом уровне находится 2s^1-энергоактивный электрон, а в атоме натрия - 3s^1. Этот принцип справедлив для всех щелочных металлов.
Исходя из электронной формулы внешнего уровня щелочного металла, можно сделать вывод о его химической реактивности и физических свойствах. Например, наличие одного электрона на внешнем уровне делает металл очень реактивным и способным легко образовывать ионы с положительным зарядом. Это объясняет высокую активность щелочных металлов в химических реакциях и их способность реагировать с водой и воздухом.
Примеры электронной формулы внешнего уровня щелочного металла

Щелочные металлы представляют собой группу элементов первой группы периодической системы. Эти элементы характеризуются наличием одного электрона на внешнем энергетическом уровне, что делает их особенно реактивными и способными образовывать ионные соединения. Давайте рассмотрим примеры электронной формулы внешнего уровня для трех щелочных металлов: лития, натрия и калия.
Литий (Li) находится в первой группе периодической системы и имеет электронную конфигурацию 1s² 2s¹. Его внешний энергетический уровень заполнен одним электроном. Таким образом, электронная формула внешнего уровня лития будет представлена как 2s¹.
Натрий (Na) также принадлежит к группе щелочных металлов и имеет электронную конфигурацию 1s² 2s² 2p⁶ 3s¹. Внешний энергетический уровень натрия также заполнен одним электроном на 3s подуровне. Поэтому электронная формула внешнего уровня натрия будет выглядеть как 3s¹.
Калий (K) является еще одним щелочным металлом, находящимся в первой группе периодической системы. Его электронная конфигурация состоит из следующих уровней: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹. Внешний энергетический уровень калия в данном случае заполнен одним электроном на 4s подуровне. Таким образом, электронная формула внешнего уровня калия будет представлена как 4s¹.
Эти примеры демонстрируют, что щелочные металлы имеют по одному электрону на своем внешнем энергетическом уровне, что делает их особенно реактивными и способными образовывать ионные соединения с другими элементами.
Свойства внешнего уровня щелочного металла

Внешний уровень щелочного металла представлен последней электронной оболочкой, содержащей одну электронную подуровень s. Эта оболочка полностью заполнена и, таким образом, электрон внешнего уровня щелочного металла является "самым свободным" электроном, который легко вступает в химические реакции.
Свойства внешнего уровня щелочного металла определяют его активность и реакционную способность. Эти металлы имеют низкую электроотрицательность и тенденцию отдавать электроны, поэтому они легко реагируют с другими веществами, особенно с кислородом и водой.
Щелочные металлы обладают хорошими проводимостью тепла и электричества. Это связано с наличием свободно движущихся электронов на внешнем уровне. Вполне логично, что наличие этих электронов делает металлы хорошими электропроводниками и отличными теплопроводниками.
Чтобы облегчить изучение химии щелочных металлов, люди разработали электронные формулы внешнего уровня, которые помогают лучше понять их химические свойства и возможности. Электронная формула внешнего уровня щелочного металла представляет собой запись электронного конфигурации внешнего уровня, что позволяет предсказывать реакционную способность металла.
Вопрос-ответ

Что такое электронная формула внешнего уровня щелочного металла?
Электронная формула внешнего уровня щелочного металла показывает количество электронов на внешней оболочке атома металла, которая определяет его химические свойства и способность образовывать соединения.
Как определить электронную формулу внешнего уровня щелочного металла?
Электронную формулу внешнего уровня щелочного металла можно определить по номеру группы, в которой находится данный металл в периодической системе. Например, у лития (находящегося в первой группе) электронная формула внешнего уровня будет 1s²2s¹.
Какая электронная формула внешнего уровня у щелочного металла калия?
У щелочного металла калия электронная формула внешнего уровня будет 2s²2p⁶3s²3p⁶4s¹. Это означает, что на внешней оболочке атома калия находится один электрон, который может участвовать в химических реакциях и образовании соединений.
