Как получают щелочной металл калий электролизом
Щелочные металлы, такие как калий, являются одними из наиболее важных элементов в химии. Калий используется в различных отраслях промышленности, включая производство удобрений, стекла и щелочно-литиевых батарей. Один из способов получения калия - электролиз щелочной соли калия.
Процесс электролиза заключается в разложении химического соединения с помощью электрического тока. Для получения калия электролиз проводят с использованием раствора гидроксида калия (KOH) или расплава хлорида калия (KCl). Оба этих вещества содержат ионы калия, которые при электролизе могут быть освобождены и собраны.
Процесс электролиза происходит в электролизере, который представляет собой специальную ячейку соответствующей формы, где проводят электролиз. Ячейка содержит пару электродов - анод и катод, разделенных мембраной, которая позволяет лишь ионам проходить через нее. При подаче электрического тока в ячейку, ионы калия перемещаются к аноду, где происходит окисление, а свободные электроны движутся по внешней цепи к катоду. На катоде происходит восстановление ионов калия в металлический калий.
По завершению электролиза, металлический калий собирают на катоде, где он образует небольшие шарики металла. Полученный металл очищают от примесей и упаковывают для дальнейшего использования в различных отраслях промышленности.
Процесс получения щелочного металла калия электролизом
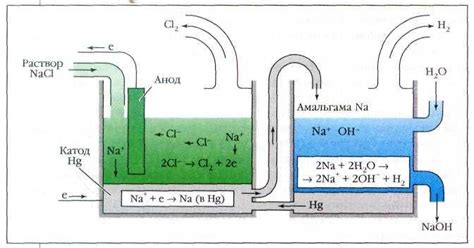
Щелочной металл калий является одним из самых важных элементов при производстве различных химических соединений. Он используется во многих областях, включая фармацевтику, сельское хозяйство и производство удобрений. Основной способ получения калия основан на его электролизе.
Процесс получения калия электролизом происходит в специальной ячейке, которая состоит из анода и катода, разделенных электролитической средой. Анодом служит графитовый стержень, а катодом – металлическая сетка из цинка. В качестве электролита используется плавящийся галогенид калия, обычно – хлорид. Во время процесса электролиза в ячейку подается электрический ток.
При электролизе стержень анода окисляется, атомы калия иодид значения не имеют и, сдвигаясь, образуют ионные соединения, оседая на специально подготовленный катод. На верхушку катода подают дополнительную каменную угольную пыль. После окончания процесса на дне ячейки скапливается чистый калий, который извлекают и далее изготавливают в нужной массе и форме.
Преимуществом электролиза при получении калия является его эффективность и относительная низкая стоимость процесса. Этот метод позволяет получать высококачественный металл с минимальными примесями. Однако электролиз калия – очень сложный и опасный процесс, который требует высокой квалификации персонала и соблюдения всех мер безопасности.
Электролиз: основные принципы и применение

Электролиз - это процесс, при котором разложение химических соединений происходит под действием электрического тока. Основными компонентами электролиза являются электролит, протекающий через его электролитический сосуд, и электроды, через которые проходит электрический ток. Причем положительный электрод называется анодом, а отрицательный - катодом.
Процесс электролиза имеет широкое применение в различных областях. В первую очередь, электролиз используется для получения различных металлов. Например, в результате электролиза можно получить калий, натрий или алюминий. Это позволяет не только снизить затраты на производство металлов, но и улучшить их качество.
Кроме того, электролиз применяется в гальванической отрасли, где используется для покрытия различных поверхностей металлом. Например, в процессе электролиза можно покрыть детали автомобиля слоем никеля, чтобы защитить их от коррозии. Также электролиз применяется в процессе электрохимического синтеза органических соединений и в производстве электрической энергии.
Значимость электролиза заключается не только в его применении для получения различных веществ, но и в возможности контролировать химические реакции. Электролиз позволяет выбирать направление реакции, регулировать скорость ее протекания и получать вещества с нужными свойствами.
Калий: свойства и применение

Калий (K) – химический элемент из группы щелочных металлов, обладающий мягким металлическим блеском. Он обладает рядом уникальных свойств, которые нашли применение в различных областях жизни.
Физические свойства калия:
- Калий имеет серебристо-белый цвет и мягкую консистенцию, благодаря чему его легко можно резать ножом.
- При комнатной температуре калий является твёрдым металлом, но при нагревании быстро плавится и превращается в жидкость.
- Калий обладает низкой плотностью, что делает его лёгким металлом. Он даже плавает в воде.
- Однако калий очень реактивен и сильно реагирует с кислородом воздуха, поэтому его часто хранят под слоем минерального масла или в инертной атмосфере.
Применение калия:
- Калий является необходимым макроэлементом для живых организмов, так как участвует в биохимических процессах. Благодаря этому он применяется в сельском хозяйстве в качестве удобрения для повышения урожайности растений.
- Калий также широко используется в производстве удобрений, например, калийных солей, которые содержат питательные элементы для растений.
- Калийные соединения имеют многочисленные применения в различных отраслях промышленности, включая производство стекла, мыла, шампуней и других бытовых товаров.
- Калийные соли применяются в медицине для лечения различных заболеваний и для поддержания нормального функционирования организма человека.
Таким образом, калий является важным элементом как для живых организмов, так и для многих отраслей промышленности. Его уникальные свойства и широкий спектр применения делают его необходимым в нашей повседневной жизни.
Электролиз калийной соли для получения металла
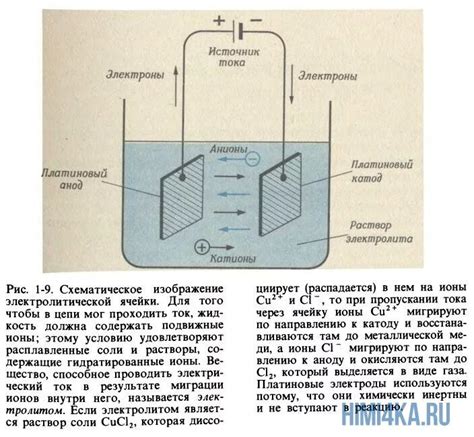
Щелочной металл калий можно получить путем электролиза калийной соли. Этот процесс основан на разложении компонентов соли под воздействием электрического тока.
Для проведения электролиза обычно используют специальный аппарат, называемый электролизером. В его центральной части устанавливают два электрода: анод и катод. Анодом служит проточный графитовый стержень, а катодом – нержавеющая стальная сетка.
Вначале анод и катод погружают в калийную соль, растворенную в воде. Затем включают электролизер, и через его анод и катод подается электрический ток. Под воздействием тока происходит диссоциация калийной соли на ионы калия и ионы хлора.
Ионы калия, перемещаясь к катоду, принимают отрицательный заряд и выделяются в виде металлического калия на поверхности сетки. Ионы хлора, перемещаясь к аноду, принимают положительный заряд и выделяются в виде газообразного хлора.
Таким образом, при электролизе калийной соли получается чистый металлический калий. Этот процесс является эффективным способом получения металла и широко применяется в промышленности.
Вопрос-ответ

Каким образом происходит получение щелочного металла калия электролизом?
Для получения щелочного металла калия электролизом используется процесс, называемый электролизом расплава. В этом процессе калий получают путем проведения электрического тока через тугоплавкий калиевый гидроксид. Электролиз проводится в специальных электролизерных ячейках, в которых используются катоды и аноды из платины или других редких металлов. При электролизе калийионы переходят на катод, где превращаются в калиевый металл, а кислородионы переходят на анод и взаимодействуют с атомами воды, образуя молекулы кислорода.
Какой электролит используется при процессе электролиза калия?
В процессе электролиза калия используется тугоплавкий калиевый гидроксид (КОН) в качестве электролита. Калиевый гидроксид представляет собой сильный щелочной раствор с высокой проводимостью электрического тока. Он обеспечивает необходимую среду для проведения электролиза и разложения калия в металлическую форму.
Какие материалы используются для анодов и катодов в процессе электролиза калия?
В процессе электролиза калия используются аноды и катоды, изготовленные из платины или других редких металлов. Это связано с тем, что эти материалы обладают высокой химической стойкостью и электропроводностью, что позволяет им эффективно справляться с высокими температурами и агрессивными условиями, характерными для процесса электролиза.
Какие основные реакции происходят в процессе электролиза калия?
В процессе электролиза калия происходят две основные реакции: на катоде происходит редукция калияионов (K+) с образованием металлического калия (K), а на аноде происходит окисление кислородаионов (O2-) с образованием кислорода (O2). Эти реакции происходят в результате воздействия электрического тока на тугоплавкий калиевый гидроксид (КОН), который является электролитом в процессе электролиза.
