Щелочи - это класс химических соединений, обладающих щелочными свойствами и способных растворяться в воде, образуя ионы гидроксидов. Одним из важных свойств щелочей является их реакция с металлами, в результате которой выделяется водород.
Реакция щелочи с металлом основана на способности металла отдавать электроны, а щелочи принимать электроны. При взаимодействии щелочи с металлом образуется ион гидроксида металла и молекула водорода. Например, при реакции натрия с водой образуется гидроксид натрия и водород:
2Na + 2H₂O → 2NaOH + H₂
Выделение водорода при реакции щелочи с металлом является важным процессом в химической промышленности. Выделенный водород может использоваться в процессе водородной сварки, в производстве аммиака и других химических веществ, а также в энергетике как источник экологически чистой энергии.
Кроме того, реакция выделения водорода при взаимодействии щелочи с металлом может быть использована в химических опытах и демонстрациях в образовательных целях. Эта реакция является достаточно быстрой и заметной, что делает ее привлекательной для показа в классе или на химической лабораторной работе.
Металлическое натрий реагирует с щелочью
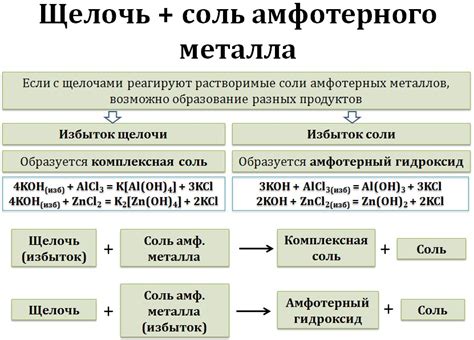
Щелочи являются химическими соединениями, обладающими высокой щелочностью, и широко используются в различных сферах промышленности и научных исследований. Одной из характеристик щелочей является их способность реагировать с металлами, в результате чего выделяется водород. В данном случае рассматривается реакция металлического натрия с щелочью.
Металлический натрий - это стабильный металлический элемент, относящийся к группе щелочных металлов. Он обладает высокой химической активностью и способен реагировать с такими веществами, как вода и кислоты. При взаимодействии с щелочами, металлический натрий выделяет водородный газ.
Водородное выделение при реакции металлического натрия с щелочью происходит по принципу активного замещения. Металлический натрий отдает свои электроны щелочи, что приводит к образованию гидроксида натрия и выделению молекул водорода. Реакция происходит с выделением тепла и сопровождается образованием белого осадка гидроксида натрия.
Реакция металлического натрия с щелочью может быть представлена уравнением:
2Na + 2OH → 2NaOH + H2
В результате данной реакции образуется гидроксид натрия и молекулы водорода, которые выделяются в виде газа. Выделение водорода - это одна из характеристик реакции металла с щелочью и имеет практическое применение в различных отраслях науки и промышленности.
Калий: реакция с щелочью

Калий (K) - химический элемент периодической системы, алкалий, который активно взаимодействует с щелочами, включая гидроксид натрия (NaOH) и гидроксид калия (KOH).
В результате реакции калия с щелочью образуется гидроксид калия (KOH) и выделяется водород (H2) в газообразном состоянии. Реакция сопровождается выделением тепла и образованием пены или шлака на поверхности реагирующих веществ.
Реакция калия с гидроксидом натрия проводится при нагревании или путем смешивания взрывоопасных соединений. Уравнение реакции выглядит следующим образом: 2K + 2NaOH -> 2KOH + H2O + H2.
Результатом реакции калия с гидроксидом калия также является образование гидроксида калия (KOH) и выделение водорода (H2). Уравнение реакции имеет вид: 2K + 2KOH -> 2K2O + H2.
При проведении реакции следует соблюдать меры предосторожности, так как реакция между калием и щелочью может быть весьма взрывоопасной.
Таким образом, реакция калия с щелочью приводит к образованию гидроксида калия и выделению водорода в газообразном состоянии.
Различия в реакции щелочи с натрием и калием
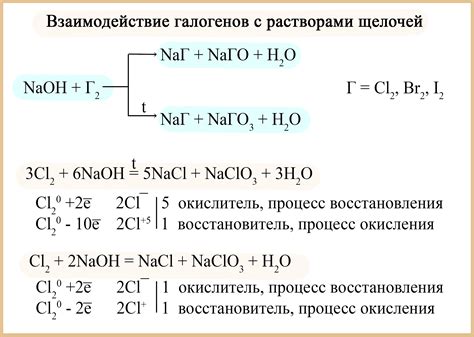
Реакция щелочи с металлами, такими как натрий и калий, происходит с выделением водорода. Однако, натрий и калий имеют свои отличительные особенности в данной реакции.
Скорость реакции: Калий реагирует с щелочью более быстро, чем натрий. Это объясняется тем, что калий является более реакционноспособным металлом.
Выделение водорода: При взаимодействии натрия с щелочью образуется газообразный водород, который легко обнаружить по его характеристическим свойствам – горению. В случае с калием, при реакции с щелочью также выделяется водород, но за счет более интенсивной горючести самого калия. Выделение водорода при реакции с калием обычно сопровождается звуковыми и световыми эффектами.
Реакция с водой: Калий реагирует агрессивнее с водой, чем натрий. При взаимодействии с водой калий выделяет еще больше водорода и возгорается пламенем. Натрий также реагирует с водой, но его реакция менее активна по сравнению с калием.
В целом, реакция щелочи с натрием и калием похожа, но имеет свои отличительные особенности. Понимание этих различий позволяет лучше понять химические свойства и поведение металлов в реакциях с другими веществами.
Вода и реакция металла с щелочью

Вода является одним из основных веществ на планете Земля, и ее свойства играют важную роль в химических реакциях. Реакция металла с щелочью также связана с водой, так как вода является средой, в которой происходят эти реакции.
Реакция металла с щелочью, такой как натрий или калий, с водой приводит к образованию гидроксида металла и выделению водорода. Эта реакция может быть представлена следующим образом:
- Металл реагирует с водой, образуя гидроксид металла (NaOH или KOH).
- При этом выделяется водородный газ (H2), который можно заметить по появлению пузырьков водорода на поверхности реакционной смеси.
- Происходит образование раствора гидроксида металла, который может быть щелочью. Щелочь обладает основными свойствами, такими как щелочность и способность нейтрализовать кислоты.
Реакция металла с щелочью и водой является эндотермической, то есть требует поглощения тепла для протекания. При этом поглощение тепла среды снижает температуру окружающей среды и делает реакцию охлаждающей.
Такая реакция имеет множество практических применений. Например, выделение водорода при реакции щелочи с металлом может быть использовано в процессах получения водорода для использования в качестве топлива или в химической промышленности.
Выделение водорода во время реакции щелочи с металлом
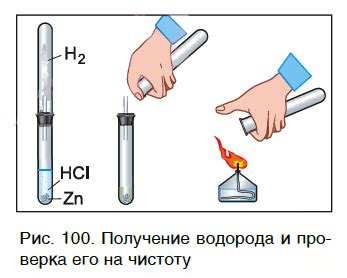
Реакция щелочи с металлом является химическим процессом, в результате которого образуется водород и соответствующее солевое соединение. Эта реакция часто используется в химических исследованиях и промышленности, так как выделение водорода является одной из определенных химических реакций.
Щелочные металлы, такие как натрий, калий, литий и другие, обладают способностью реагировать с водой и образовывать щелочную растворимую основу и водород. При этом происходит окислительно-восстановительная реакция, в результате которой металл окисляется, а протоны восстанавливаются, образуя молекулу водорода.
Реакция щелочи с металлом происходит по следующему общему уравнению:
Металл + Щелочь → Соль + Водород
Во время реакции щелочи с металлом, газовый водород выделяется в виде пузырьков, которые видны в реакционной среде. Это происходит благодаря тому, что молекулы водорода мало взаимодействуют с водой и легко выходят на поверхность. Основа, образовавшаяся в результате реакции, остается в растворе как соль.
Выделение водорода во время реакции щелочи с металлом является примером одного из способов получения этого газа. Водород обладает рядом полезных свойств и широко используется в многих отраслях промышленности и научных исследованиях.
Значение реакции щелочи с металлом в химических процессах

Реакция щелочи с металлом является одним из важных химических процессов, которые происходят в нашей жизни. Она имеет значительное значение в различных областях, включая промышленность, науку и повседневную жизнь.
Наиболее распространенной реакцией щелочи с металлом является выделение водорода. В результате этой реакции образуется гидроксид металла и водородный газ, который представляет собой важный сырьевой материал для многих процессов в промышленности, таких как производство аммиака и водородных топливных элементов.
Реакция щелочи с металлом также применяется в лаборатории для получения чистых образцов металлов или для определения их содержания в различных материалах. Например, в аналитической химии щелочи используются для титрования проб, чтобы определить их содержание металлов.
Одним из важных примеров реакции щелочи с металлом является процесс очистки поверхности металлов перед их покрытием пленкой. Щелочные растворы обладают высокой щелочностью, что позволяет эффективно удалять загрязнения с поверхности металла, обеспечивая лучшее сцепление пленки и повышая её стойкость.
В целом, реакция щелочи с металлом играет важную роль в химических процессах, обеспечивая получение необходимых продуктов, очищение и анализ металлов, а также реализацию различных технологических процессов в промышленности.
Применение выделения водорода в промышленности

Выделение водорода является важным процессом в промышленности и имеет широкий спектр применений. Данный газ является одним из основных сырьевых материалов для производства аммиачной селитры, которая широко применяется в сельском хозяйстве в качестве удобрения. Водород используется и в других процессах производства удобрений, таких как аммиачная сода и аммиачная селитра.
Водород также находит применение в процессе прямого синтеза аммиака, который используется в производстве азотных удобрений. Синтез аммиака осуществляется путем соединения азота и водорода. При этом водород служит в качестве реагента и обеспечивает необходимое количество атмосферного давления для реакции.
Кроме того, водород применяется как источник энергии в различных отраслях промышленности. Его высокая энергетическая плотность и отсутствие вредных выбросов при сгорании делают его привлекательным средством для производства электроэнергии, а также топлива для автомобилей с горючими элементами.
Также стоит отметить использование водорода в процессе производства металлов и металлообработки. Выделение водорода позволяет уменьшить содержание примесей в металлах и обеспечить большую чистоту продукта. Кроме того, водород используется для очистки металлических поверхностей и удаления окислов, что обеспечивает более эффективную обработку и улучшает качество конечного продукта.
Таким образом, выделение водорода в промышленности играет важную роль и находит широкое применение в различных отраслях. Он служит сырьем для производства удобрений, источником энергии и необходимым компонентом в производстве металлов. Благодаря своим свойствам, водород становится все более востребованным в промышленности и является одним из ключевых компонентов современной экономики.
Вопрос-ответ

Какая реакция происходит между щелочью и металлом?
Реакция между щелочью и металлом называется реакцией щелочи с металлом. В результате этой реакции образуется соль и выделяется водород.
Как выделяется водород при реакции щелочи с металлом?
Водород выделяется при реакции щелочи с металлом из-за способности щелочи превращать воду в водород и гидроксид металла. Гидроксид металла растворяется в воде и образуется соль, а водород выделяется в виде газа.
Какие металлы реагируют с щелочью?
Щелочные металлы, такие как натрий (Na), калий (K), рубидий (Rb) и цезий (Cs), реагируют с щелочью. Реакция протекает с выделением водорода и образованием щелочного гидроксида.
Что происходит с раствором щелочи при реакции с металлом?
При реакции щелочи с металлом раствор щелочи становится щелочным гидроксидом. Например, реакция натрия с щелочью приведет к образованию натриевого гидроксида (NaOH).
В чем состоит практическое значение реакции щелочи с металлом?
Реакция щелочи с металлом имеет практическое значение в различных областях. Например, выделение водорода при этой реакции может использоваться в химической промышленности для производства аммиака и металлов, а также в водородной энергетике в качестве источника энергии.
