Серная концентрированная кислота, химическая формула H2SO4, является одним из самых сильных и распространенных минеральных кислот. Эта кислота имеет ряд уникальных свойств, которые делают ее полезной для многих приложений в промышленности и научных исследованиях.
Кристаллическая серная кислота является бесцветным веществом и обладает высокой плотностью. Она образует гигроскопичные кристаллы, которые легко растворяются в воде. Раствор серной кислоты обычно имеет молекулярное строение H3O+HSO4-, которое обеспечивает ему свойства кислоты.
Серная концентрированная кислота обладает ярко выраженной коррозионной активностью и способна растворять многие металлы. При контакте с металлом, серная кислота ожидаемо окисляет его, выделяя серу и образуя соли металлосульфатов. Однако, в некоторых случаях, некоторые металлы могут проявлять пассивность в отношении серной кислоты, образуя защитную пленку на поверхности, которая будет предотвращать дальнейшую реакцию.
Знание свойств серной концентрированной кислоты и ее взаимодействия с металлами является важным для успешной подготовки к экзамену ЕГЭ по химии. Умение анализировать и предсказывать результаты таких реакций поможет в формировании навыков химического расчета и решения задач.
Основные свойства серной концентрированной кислоты
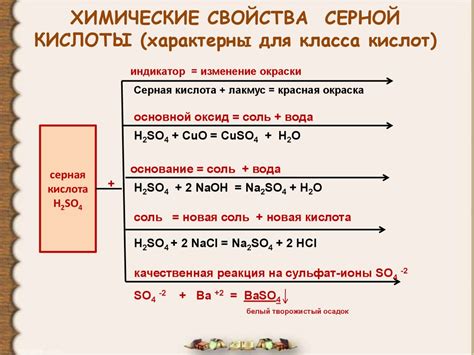
Серная концентрированная кислота (H2SO4) – это одна из наиболее распространенных химических соединений, которая обладает рядом особенных свойств.
- Сильная кислотность: Серная концентрированная кислота является одной из самых сильных кислот, которые существуют. Поэтому она обладает способностью эффективно диссоциировать в воде и отдавать протоны (Н+), что делает ее отличным растворителем для многих веществ.
- Окислительные свойства: Серная концентрированная кислота обладает сильно окислительными свойствами. Взаимодействуя с некоторыми веществами, она способна передавать кислород или принять электроны, что позволяет ей проявлять окислительное действие.
- Коррозивность: Серная концентрированная кислота обладает высокой коррозивной активностью. Она способна разрушать и растворять многие материалы, включая металлы, минеральные вещества и органические соединения.
- Высокая плотность: Серная концентрированная кислота имеет плотность, превышающую плотность воды. Это свойство делает ее отличным лейком для разделения различных смесей веществ.
- Теплоемкость: Серная концентрированная кислота обладает высокой теплоемкостью, то есть она способна поглощать и отдавать большое количество тепла при реакциях.
Использование серной концентрированной кислоты может быть опасным и требует соблюдения особых мер предосторожности.
Физические и химические характеристики

Серная концентрированная кислота (H2SO4) является бесцветной жидкостью с острой идентичностью. Она обладает высокой плотностью и кипит при температуре около 337 градусов Цельсия.
В химии серная кислота считается кислотой Бренстеда-Лоуренса и является одним из самых сильных кислотных соединений. Она обладает высокой степенью ионизации и диссоциации: каждая молекула кислоты может отдать два протона. Благодаря этой способности серная кислота широко используется в лабораторной работе и промышленности.
Серная кислота также является сильным окислителем. Она способна окислять различные вещества, включая металлы. Взаимодействие с металлами приводит к образованию солей и выделению газа водорода. Некоторые металлы, такие как алюминий и цинк, реагируют с серной кислотой с выделением тепла и возгоранием.
Физические и химические свойства серной концентрированной кислоты делают ее важным реагентом в различных отраслях науки и промышленности, включая производство удобрений, пластмасс и взрывчатых веществ. Однако, из-за ее высокой коррозионной активности и агрессивности, серную кислоту необходимо использовать с предосторожностью и соблюдением соответствующих мер безопасности.
Свойства кислоты: кислотность и агрессивность

Свойства кислоты включают в себя ее кислотность и агрессивность. Кислотность - это характеристика кислоты, обусловленная ее способностью отдавать протоны. Чем больше протонов способна отдать кислота, тем выше ее кислотность. Кислотность кислот определяется по их реакции с щелочами: сильные кислоты полностью диссоциируют в воде, отдавая все свои протоны, а слабые кислоты диссоциируют лишь частично.
Агрессивность кислоты - это ее способность разрушать другие соединения, включая металлы. Чаще всего кислоты вступают в реакцию с металлами, образуя соли и выделяя водородный газ. При этом агрессивность кислоты зависит от ее концентрации и силы разрушающего действия на металлы. Некоторые кислоты, например, серная концентрированная кислота, обладают высокой агрессивностью и способны разрушать металлы даже при низкой концентрации. Чем сильнее агрессивность кислоты, тем она опаснее и требует особой осторожности при работе с ней.
Таким образом, кислотность и агрессивность кислоты являются основными свойствами кислот и определяют ее химическую активность. Знание этих свойств позволяет установить ее потенциальное влияние на другие соединения, а также принять необходимые меры безопасности при работе с кислотами.
Взаимодействие серной концентрированной кислоты с металлами
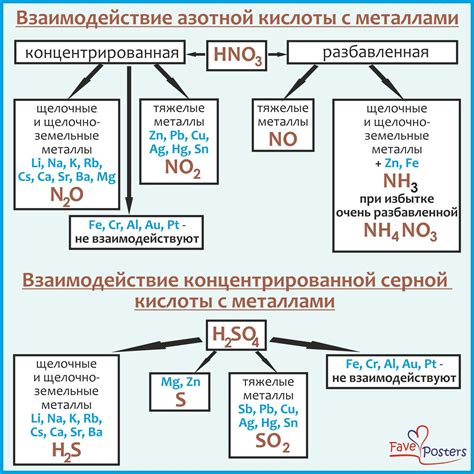
Серная концентрированная кислота, также известная как серная кислота или H2SO4, является одной из наиболее распространенных и сильных кислот. Она широко используется в промышленности и лабораториях для множества процессов, включая очистку, растворение и окисление. Взаимодействие серной концентрированной кислоты с металлами является одним из важных аспектов ее химического свойства.
Серная концентрированная кислота проявляет сильные окислительные свойства и может взаимодействовать с большинством металлов. Однако, с химической точки зрения, реакция кислоты с металлами может быть различной в зависимости от их электрохимического потенциала.
Взаимодействие металлов с серной концентрированной кислотой может привести к образованию солей серной кислоты и выделению водорода. Некоторые металлы, такие как цинк, магний и алюминий, образуют защитную пленку оксида на своей поверхности, которая предотвращает дальнейшее растворение. Другие металлы, например, железо, реагируют с кислотой с образованием соли и выделением водорода.
В реакции между серной концентрированной кислотой и металлами можно наблюдать выделение воспламеняющегося водорода, что представляет опасность в лабораторной практике. Поэтому, при обработке металлов с кислотой, необходимо соблюдать осторожность и принимать все необходимые меры предосторожности, чтобы избежать аварийных ситуаций.
Итак, взаимодействие серной концентрированной кислоты с металлами является сложным процессом, который зависит от свойств и реактивности самой кислоты и металлов. Знание этих свойств поможет правильно организовать работу с ними и избежать негативных последствий.
Коррозия и разрушение металлических поверхностей

Коррозия – это процесс повреждения металлических поверхностей, который происходит под воздействием окружающей среды. При коррозии на металлической поверхности образуется слой оксидов, гидроксидов или солей металла, что приводит к разрушению и потере свойств материала.
Коррозия металла может происходить под воздействием различных факторов, таких как влага, кислоты, щелочи, соли и др. Особенно активно происходит коррозия в присутствии кислорода, поэтому металлы при взаимодействии с воздухом склонны к окислению и разрушению.
В результате коррозии металлической поверхности происходит образование коррозионных процессов, таких как питтинг, образование трещин, локальная и общая коррозия. При этом, металл может потерять свою прочность, становиться хрупким и не пригодным для использования в конструкциях, механизмах и других сферах применения.
Коррозия может быть предотвращена или замедлена с помощью применения защитных покрытий, антикоррозионных покрытий, гальванической защиты, а также контролирования условий окружающей среды. Также важно систематическое осуществление профилактического обслуживания и регулярная проверка состояния металлических поверхностей для своевременного выявления и устранения начинающейся коррозии.
Серные соединения в результате реакции с металлами

Серная концентрированная кислота обладает значительной реакционной способностью и способна взаимодействовать с металлами. В результате такой реакции образуются соединения между серной концентрированной кислотой и металлами, которые имеют различные свойства и применения.
Одним из наиболее известных комплексных соединений между серной концентрированной кислотой и металлами является сульфат. Сульфаты обладают высокой растворимостью в воде и широко используются в промышленности. Например, сульфат меди (II) используется при производстве пигментов и во многих других отраслях химической промышленности.
Кроме сульфатов, в результате взаимодействия серной концентрированной кислоты и металлов могут образовываться и другие соединения, например, сульфиды. Сульфиды часто обладают характерным запахом, низкой растворимостью в воде и применяются в различных областях науки и промышленности.
Важно отметить, что реакция между серной концентрированной кислотой и металлами является химической реакцией, сопровождающейся выделением газа, например, сероводорода (H2S). Сероводород обладает сильным запахом гнили и может оказывать вредное действие на организм человека. Поэтому данная реакция требует особого внимания и проведения в безопасных условиях.
Подготовка к ЕГЭ по серной концентрированной кислоте и ее взаимодействию с металлами
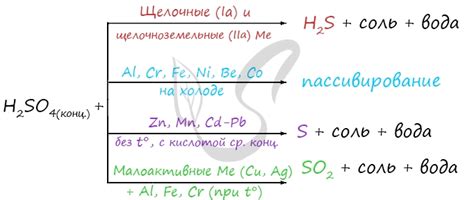
Серная концентрированная кислота (H2SO4) является одной из наиболее известных и широко используемых кислот в химии. Ее основным свойством является высокая степень концентрации и сильная кислотность.
При взаимодействии с металлами серная концентрированная кислота проявляет различные реакции. Например, она способна растворять щелочные металлы, такие как натрий и калий, образуя соли и выделяя водород. Данная реакция протекает очень быстро и с большим выделением газа.
Однако серная кислота не реагирует с большинством неметаллических элементов, таких как углерод, кислород и азот. Это связано с ее высокой кислотностью и необходимостью высокой температуры или присутствия катализатора для проведения реакции.
Важным аспектом подготовки к ЕГЭ по серной концентрированной кислоте и ее взаимодействию с металлами является умение распознавать и анализировать реакции, а также проводить расчеты по количеству веществ и измерению pH. Все эти навыки позволят успешно справиться с задачами ЕГЭ и получить высокий балл на экзамене.
Подведем итоги. Серная концентрированная кислота - это сильная кислота, которая обладает высокой степенью концентрации. Она взаимодействует с металлами, растворяет щелочные металлы и образует соли. Однако она не реагирует с неметаллами без использования высоких температур или катализаторов. Для успешной подготовки к ЕГЭ необходимо развивать навыки распознавания реакций и проведения расчетов по количеству веществ и pH.
Теоретические основы и принципы

Серная концентрированная кислота (H2SO4) - это одна из наиболее популярных и широко используемых кислот в химической промышленности. Ее свойства и принципы взаимодействия с металлами основываются на ее строении и свойствах.
Кислота образуется при соединении двух молекул воды (H2O) с молекулой серни (S). Результатом этой реакции является образование серной кислоты и выделение тепла. Кислота характеризуется высокой концентрацией и является сильным оксидирующим агентом.
Серная концентрированная кислота проявляет активность при взаимодействии с металлами. В результате реакции между кислотой и металлом, молекулы H2SO4 распадаются на ионы H+ и HSO4-. Свободные ионы H+реагируют с металлом, образуя гидроген, который выделяется в виде пузырьков, а HSO4- остается в растворе.
Взаимодействие с металлами зависит от их активности. Самые активные металлы, такие как натрий и калий, реагируют с H2SO4 виолентно и могут вызвать взрыв. Менее активные металлы, такие как медь и железо, реагируют с кислотой более медленно и без опасности.
Практические навыки и эксперименты

Получение и исследование свойств серной концентрированной кислоты является важным аспектом изучения данного вещества. Для выполнения экспериментов необходимо организовать рабочее место с необходимым оборудованием и реактивами.
Первым шагом при практическом изучении серной концентрированной кислоты является ее получение. Для этого можно воспользоваться методом постепенного разбавления серной кислоты с водой или синтезом из серы и концентрированной серной кислоты. Полученную кислоту следует хранить в специальной посуде, защищенной от света и взаимодействия с окружающими веществами.
Полученная серная концентрированная кислота обладает рядом характерных свойств. За счет своей высокой концентрации и кислотности, она способна быстро разрушать органические вещества и многие неорганические материалы. Она также обладает сильным окислительным и дезинфицирующим свойствами, что позволяет использовать ее в промышленности и лабораторных условиях.
Серная концентрированная кислота взаимодействует с большим количеством металлов, образуя с ними соответствующие соли. Взаимодействие серной кислоты с металлами может сопровождаться выделением водорода и образованием солей серной кислоты. Это свойство можно наблюдать при проведении экспериментов, добавляя металлы в раствор серной кислоты и наблюдая химическую реакцию.
Практические навыки и эксперименты с серной концентрированной кислотой позволяют не только изучить ее свойства, но и получить практически полезные знания о химических реакциях с участием этого вещества. Важно соблюдать все меры предосторожности при проведении таких экспериментов, так как серная концентрированная кислота обладает высокой токсичностью и может нанести вред здоровью человека.
Вопрос-ответ

Какие свойства имеет серная концентрированная кислота?
Серная концентрированная кислота обладает рядом свойств: она обладает сильной коррозионной способностью, она абсорбирует влагу, показывает свойства окислителя и действует на органику.
Как происходит взаимодействие серной концентрированной кислоты с металлами?
Серная концентрированная кислота может реагировать с металлами различными способами: окислять их, образуя сернистые оксиды или сульфаты, также она может диспропорционировать, образуя сернистый газ, который в дальнейшем окисляется до серной кислоты. Некоторые металлы, такие как железо и алюминий, способны образовывать защитные пленки, которые защищают их от дальнейшего воздействия кислоты.
Какие реакции совершает серная концентрированная кислота?
Серная концентрированная кислота может участвовать в различных реакциях, например: окисление металлов, образование сернистых оксидов, гидратация, диспропорционирование, образование эфиров, реакции с неорганическими соединениями и органическими веществами.
Как серная концентрированная кислота воздействует на органику?
Серная концентрированная кислота способна действовать на органические вещества, протекает образование эфиров, взаимодействие с аминами, гидролиз эстеров и другие реакции. Также она может использоваться в органическом синтезе для проведения реакций обезвоживания или сульфонирования.
