Семейство щелочных земельных металлов состоит из шести элементов: бериллия (Be), магния (Mg), кальция (Ca), стронция (Sr), бария (Ba) и радия (Ra). Каждый из этих металлов обладает определенными особенностями, которые делают их уникальными и полезными в различных областях.
Начнем с бериллия, которое является легким, прочным и химически стойким металлом. Бериллий применяется в промышленности для производства легких сплавов, смазок и керамики. Он также используется в производстве ядерных реакторов и в медицине для создания рентгеновских лучей.
Магний, в свою очередь, является легким и прочным металлом, который широко используется в авиационной и автомобильной промышленности. Магнийные сплавы обладают высокой прочностью при небольшом весе, что делает их идеальными для производства легких и прочных конструкций.
Кальций, стронций, барий и радий также являются важными элементами в химической и промышленной сфере. Кальций используется в производстве стали и цемента, стронций применяется в производстве пиротехники и световых элементов, барий используется в производстве радиологических контрастных веществ, а радий используется в исследованиях радиоактивности и в медицине.
Семейство щелочных земельных металлов

Щелочные земельные металлы — это группа элементов, состоящих из 6 элементов: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они расположены во второй группе периодической системы элементов и имеют сходные химические свойства.
Характеристика щелочных земельных металлов:
- Бериллий (Be): Устойчивый металл с высокой температурой плавления. Используется в производстве сплавов, лазеров, ядерных реакторов и космических аппаратов.
- Магний (Mg): Легкий металл с высокой прочностью и хорошей коррозионной стойкостью. Широко используется в авиационной и автомобильной промышленности, медицине и пищевой промышленности.
- Кальций (Ca): Реактивный металл, широко распространенный в земной коре. Используется для производства стали, строительных материалов, химических соединений и лекарств.
- Стронций (Sr): Мягкий и серебристый металл, обладающий способностью светиться в темноте. Применяется для изготовления люминесцентных материалов, пиротехники и ядерных батарей.
- Барий (Ba): Мягкий металл, имеющий высокую плотность. Используется в производстве рентгеновских экранов и специальных стекол для оптики.
- Радий (Ra): Радиоактивный металл, являющийся естественным источником радиации. Используется в научных исследованиях и лечении некоторых заболеваний.
Щелочные земельные металлы обладают разнообразными химическими и физическими свойствами, что делает их важными и полезными элементами в промышленности и научных исследованиях.
Особенности состава и строения

Семейство щелочных земельных металлов включает в себя элементы, относящиеся к 2-й группе периодической таблицы: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они имеют общую степень окисления +2 и образуют односложные положительные ионы.
Атомы щелочно-земельных металлов обладают устойчивой внешней электронной конфигурацией s2. Внутренние электроны заполняют энергетические уровни 1s и 2s, а валентные электроны находятся на энергетическом уровне 2s. У этих элементов более низкая энергия ионизации по сравнению с другими элементами периодической таблицы, что объясняет их высокую химическую активность.
Особенностью щелочно-земельных металлов является их мягкость и низкая плотность. Они обладают низкой температурой плавления и кипения, а также высокой электроотрицательностью. Более тяжелые элементы этого семейства, такие как барий и радий, являются радиоактивными и имеют краткое продолжительное время жизни.
Физические и химические свойства
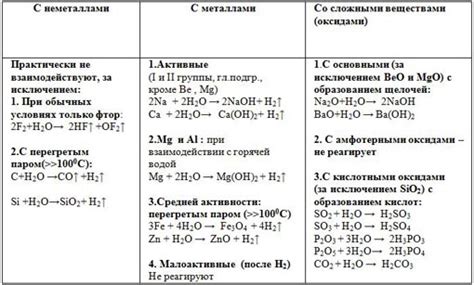
Физические свойства:
- Щелочные земельные металлы представляют собой мягкие металлы серебристо-белого цвета.
- Они обладают низкой плотностью, что делает их наиболее легкими металлами среди всех элементов.
- Имеют низкую температуру плавления и кипения.
- Эти элементы хорошо проводят электричество и тепло.
Химические свойства:
- Щелочные земельные металлы являются активными химическими элементами.
- Встречаются в природе только в соединениях, так как они реактивны и очень реакционные по отношению к кислороду и воде.
- Легко окисляются на воздухе, образуя оксидные пленки на поверхности.
- Обладают свойством образовывать ионы с положительным зарядом.
- Самыми реакционными из щелочных земельных металлов являются литий и калий.
Применение и значение

Щелочные земельные металлы имеют широкое применение в различных отраслях науки и промышленности. Они играют ключевую роль в разработке и производстве специальных материалов, а также в электронике, металлургии и многих других областях.
Одно из главных применений щелочных земельных металлов - в производстве щелочных элементов. Например, литий используется в литий-ионных аккумуляторах, которые широко применяются в мобильных устройствах, электромобилях и других устройствах. Калий используется в производстве удобрений и синтезе некоторых лекарственных препаратов. Рубидий и цезий используются в оптических приборах, радиолокации, ядерной энергетике и других областях.
Щелочные земельные металлы также используются в производстве стекла и керамики. Они придают материалам особую структуру и свойства, такие как прозрачность, цветность и высокая термическая стабильность. Кроме того, эти металлы используются в производстве специального стекла для оптики, лазеров и световых приборов.
Значение щелочных земельных металлов в науке и технологиях трудно переоценить. Они являются неотъемлемой частью современной технологии и находят применение в самых разных сферах, от электроники до металлургии. Исследования и разработки в области щелочных земельных металлов продолжаются и вносят значительный вклад в научный прогресс и технологическое развитие.
Вопрос-ответ

Какие элементы входят в семейство щелочных земельных металлов?
Семейство щелочных земельных металлов включает в себя шесть элементов: бериллий, магний, кальций, стронций, барий и радий.
Какие особенности присущи щелочным земельным металлам?
Основные особенности щелочных земельных металлов: низкая электроотрицательность, мягкость, низкая плотность и хорошая теплопроводность. Они также реагируют с водой, образуя щелочные растворы и выделяя водород.
