Литий - самый лёгкий металл из щелочных элементов периодической системы и одновременно самый сильный щелочной металл. Он обладает изумительными физическими свойствами, которые позволяют ему находить широкое применение в различных сферах науки и промышленности.
Литий имеет наименьшую атомную массу среди всех щелочных металлов и самую низкую плотность. Однако, несмотря на свою лёгкость, он обладает очень высокой жёсткостью и прочностью, что делает его одним из самых прочных металлов в мире.
Кроме того, литий является очень реактивным металлом, обладающим высокой электроотрицательностью. Это означает, что литий проявляет большую активность при взаимодействии с другими веществами, особенно с кислородом и водой. Благодаря этому свойству, литий используется в создании батарей и аккумуляторов, а также в производстве сплавов и синтезе органических соединений.
Самый сильный щелочной металл - литий, благодаря своим уникальным физическим и химическим свойствам, находит широкое применение в различных отраслях науки и технологий, делая его одним из наиболее важных элементов в периодической системе.
Щелочные металлы
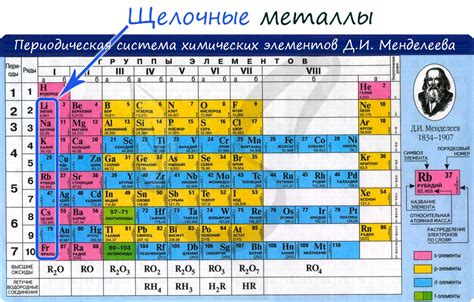
Щелочные металлы - это элементы, атомы которых обладают одним валентным электроном и легко удаляют его, образуя положительно заряженные ионы. Они входят в первую группу периодической системы элементов и включают литий, натрий, калий, рубидий, цезий и франций.
Самым сильным щелочным металлом является цезий. Он обладает наибольшей реактивностью с водой и воздухом, что делает его очень опасным и определенно не рекомендуется использовать людям, не обладающим специальными знаниями и навыками работы с ним.
Щелочные металлы находят широкое применение в различных отраслях промышленности. Например, натрий используется для производства щелочей, стекла, пластмасс, а также в пищевой и фармацевтической промышленности. Калий применяется в производстве удобрений, а литий находит применение в производстве аккумуляторов, стекломассы и лекарственных препаратов.
- Литий - легкий и наименее реактивный из щелочных металлов.
- Натрий - обширно используется в пищевой промышленности.
- Калий - важный элемент для растений и животных.
- Рубидий - применяется в производстве фотоэлементов, лазеров и ядерных батарей.
- Цезий - наиболее реактивный и опасный из щелочных металлов.
- Франций - самый редкий и радиоактивный щелочный металл.
Также стоит отметить, что уровень реактивности щелочных металлов увеличивается с увеличением атомного номера в группе. Это связано с увеличением радиуса атомов и уменьшением ионизационной энергии.
Определение щелочных металлов

Щелочные металлы - это группа элементов, которые обладают высокими активностью и химической реактивностью. Они входят в первую группу периодической системы элементов и включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Щелочные металлы характеризуются низкой плотностью, низкой температурой плавления и кипения, а также высокой электроотрицательностью. Они также легко реагируют с водой, образуя щелочные растворы и выделяя водород.
Эти элементы широко используются в различных областях, таких как производство щелочных батарей, производство стекла и керамики, а также в различных химических процессах. Они также играют важную роль в биологии, где они являются неотъемлемыми элементами жизненно важных органических соединений.
В целом, щелочные металлы обладают уникальными химическими свойствами, которые делают их важными для многих процессов и промышленных приложений. Изучение и понимание свойств этих элементов позволяют улучшить их использование и способствуют развитию науки и технологий.
Химические свойства щелочных металлов
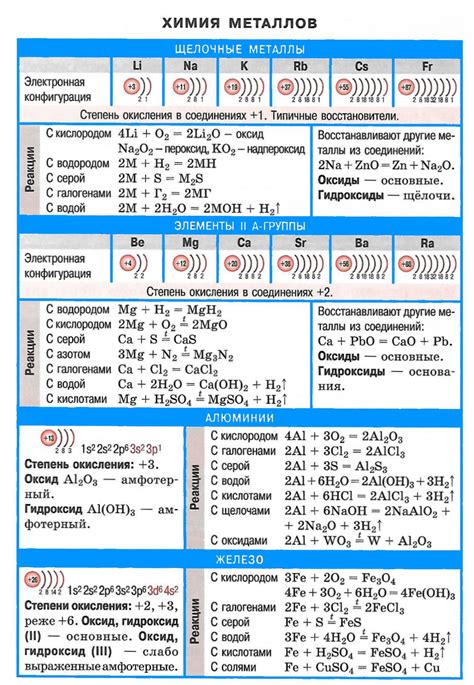
Щелочные металлы являются самыми активными металлами в периодической системе элементов. Они входят в первую группу элементов и включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Химические свойства щелочных металлов определяются их низкой ионизационной энергией и большой реактивностью.
Одним из характерных свойств щелочных металлов является их способность сильно реагировать с водой. При контакте с водой, щелочные металлы образуют щелочные растворы, выделяя большое количество водорода. Например, реакция натрия с водой выглядит следующим образом: 2Na + 2H2O = 2NaOH + H2. Это явление объяснимо высокой активностью этих металлов и их способностью образовывать ионы гидроксида.
Щелочные металлы также обладают способностью реагировать с кислородом и образовывать оксиды. Реактивность щелочных металлов с кислородом возрастает при движении по группе от лития к цезию. Литий, наиболее легкий из щелочных металлов, реагирует с кислородом атмосферы и образует оксид Li2O. В то же время, цезий, самый тяжелый щелочный металл, может реагировать с кислородом даже при низких температурах и образовывать оксид Cs2O.
Кроме того, щелочные металлы обладают хорошей способностью образовывать соли. Их ионные соединения, известные как щелочные металлические галогениды, имеют высокую стабильность и широкое применение в различных отраслях науки и промышленности. Они образуют кристаллические решетки с высокой температурой плавления и в большинстве случаев обладают хорошей проводимостью электрического тока.
Применение щелочных металлов

Литий – самый легкий металл и один из щелочных металлов, широко применяется в производстве аккумуляторов. Это связано с его высокой электрохимической активностью и способностью образовывать стабильные соединения. Например, литиевые батареи используются в мобильных телефонах, ноутбуках, электромобилях и других устройствах. Благодаря своей небольшой массе, литий также используется в аэрокосмической и авиационной промышленности для производства легких конструкций.
Натрий – еще один щелочной металл, имеет широкое практическое применение. Натрий широко используется в пищевой промышленности для консервирования и соления продуктов, а также в производстве стекла и мыла. Также натрий применяется в садоводстве для борьбы с сорняками и в экологических системах для очистки воды.
Калий – третий по активности щелочной металл, используется в сельском хозяйстве в качестве удобрения. Калийные удобрения позволяют повысить урожайность и качество сельскохозяйственных культур. Калий также применяется в производстве стекла, мыла, косметических средств, а также в лабораториях и медицине. Он играет важную роль в работе человеческого организма, особенно в нервной и сердечно-сосудистой системе.
Рубидий – редкий щелочной металл, применение которого в основном связано с научными исследованиями. Рубидий используется в лазерной технологии, в оптических приборах и в качестве катализатора при синтезе различных органических соединений.
Цезий – самый реактивный из всех щелочных металлов, его применение связано с синтезом органических соединений и в оптической электронике. Цезий используется в производстве ламп, фотоэлементов, тепловых датчиков, а также в атомных часах и гравитометрии.
Самый сильный щелочной металл в чем?

Самым сильным щелочным металлом является франций. Он был открыт в 1939 году и получил свое название в честь родины одного из открытителей - Франции. Франций является последним элементом из группы щелочных металлов в периодической таблице.
Одной из главных характеристик, делающих франций самым сильным щелочным металлом, является его электроотрицательность, которая составляет всего 0,7. Это означает, что франций имеет очень низкую способность привлекать электроны к себе, что делает его крайне реактивным и химически активным элементом.
Еще одной важной характеристикой, отличающей франций от других щелочных металлов, является его точка плавления, которая составляет всего около 27 градусов Цельсия. Это значительно ниже точек плавления других щелочных металлов, таких как цезий и калий. Благодаря этому франций является одним из самых низкоплавких металлов во всей периодической таблице.
Из-за своей высокой реактивности и низкой стабильности, франций является очень редким элементом на Земле. Его содержание в земной коре составляет всего около 30 граммов, что делает его одним из самых редких элементов. В основном франций образуется в результате распада радия и тория.
Таким образом, самый сильный щелочной металл - франций. Он отличается своей высокой реактивностью, низкой точкой плавления и редкостью на Земле. Несмотря на это, франций является важным объектом исследований в области химии и физики, и его свойства продолжают быть предметом дальнейших исследований и открытий.
Вопрос-ответ

Какой металл считается самым сильным щелочным?
Самым сильным щелочным металлом считается литий.
Почему литий считается самым сильным щелочным металлом?
Литий считается самым сильным щелочным металлом из-за его высокой электроотрицательности и низкой ионизационной энергии.
Какие еще металлы относятся к щелочным?
К щелочным металлам относятся литий, натрий, калий, рубидий, цезий и франций.
