Переходные металлы - это элементы, которые находятся в периодической таблице между группами 2 и 13. Они имеют большую переменность степеней окисления и способность образовывать комплексные соединения с различными лигандами. Все это делает переходные металлы незаменимыми во многих процессах и технологиях.
Самостоятельная работа с переходными металлами имеет важное значение в различных областях науки и промышленности. Основная задача заключается в изучении свойств и реакций данных элементов, а также в разработке методов их применения. Для этого проводятся исследования как в лабораторных условиях, так и на производстве.
Одной из основных принципов самостоятельной работы с переходными металлами является правильный выбор методов изучения и анализа. Измерения проводятся с использованием различных физических и химических методов, таких как спектроскопия, рентгеноструктурный анализ, хроматография и др. Эти методы позволяют определить состав соединений, их структуру и свойства.
Самостоятельная работа с переходными металлами направлена на создание новых материалов с заданными свойствами, разработку катализаторов и специальных соединений для промышленных процессов, а также на изучение и понимание фундаментальных закономерностей взаимодействия переходных металлов с другими веществами.
В целом, самостоятельная работа с переходными металлами важна для науки и промышленности и играет ключевую роль в развитии новых технологий и материалов, что в свою очередь способствует развитию различных отраслей промышленности и повышению качества жизни людей.
Основные принципы самостоятельной работы переходных металлов
Взаимодействие переходных металлов с другими элементами зависит от их электронной структуры и возможности принять различные окислительные состояния. Одним из основных принципов самостоятельной работы переходных металлов является их способность образовывать комплексные соединения. Это связано с наличием неполностью заполненных d-оболочек электронов, что позволяет переходным металлам образовывать координационные соединения с различными лигандами.
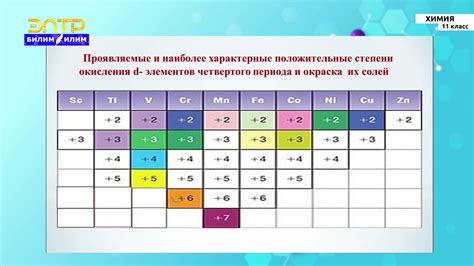
Важным принципом самостоятельной работы переходных металлов является возможность изменения степени окисления. Переходные металлы способны принимать разные окислительные состояния, что позволяет им участвовать в реакциях с различными окислителями и восстановителями. Изменение степени окисления переходных металлов обусловлено возможностью перераспределения электронов в d-оболочке, что влияет на их химическую активность и способность образовывать различные соединения.
Еще одним принципом самостоятельной работы переходных металлов является их способность образовывать различные типы связей. Переходные металлы могут образовывать ионные, ковалентные и металлические связи. Это связано с особенностями их электронной структуры и способностью образовывать комплексные соединения. Благодаря разнообразию типов связей, переходные металлы обладают широким спектром физических и химических свойств, что делает их основой для многих технологических процессов и приложений в различных областях науки и промышленности.
Работа с катализаторами и реактивами

Катализаторы – это вещества, которые ускоряют химическую реакцию, не участвуя в ней непосредственно. Использование катализаторов в переходных металлах позволяет существенно увеличить скорость реакции и облегчить процесс синтеза различных соединений.
- Гетерогенные катализаторы представляют собой физически раздельный состав, где активные центры находятся на поверхности материала. Такие катализаторы широко используются в промышленности, например, для синтеза аммиака или метанола.
- Гомогенные катализаторы – это однородные системы, где катализатор находится в одной фазе с реагентами. Такие катализаторы обладают высокой активностью и способны работать при более низких температурах.
Реактивы – это химические вещества, используемые для проведения химических реакций в лаборатории и промышленности. При работе с переходными металлами необходимо учитывать их особенности и правильно подбирать реактивы для конкретной реакции.
- Кислоты и щелочи – широко используемые реактивы для регулирования pH среды и образования комплексных соединений с переходными металлами.
- Растворители – необходимы для растворения переходных металлов и их соединений в реакционной среде.
- Лиганды – органические соединения, которые образуют стабильные комплексы с переходными металлами и могут оказывать влияние на характер проводимой реакции.
| Категория | Примеры реагентов |
|---|---|
| Кислоты | Соляная кислота (HCl), серная кислота (H2SO4) |
| Щелочи | Гидроксид натрия (NaOH), гидроксид калия (KOH) |
| Растворители | Вода (H2O), этиловый спирт (C2H5OH), ацетон (CH3COCH3) |
| Лиганды | Этилендиамин (C2H8N2), ацетилациклогексанонат (C11H18O3) |
Оптимизация процессов и достижение целей

Самостоятельная работа переходных металлов направлена на оптимизацию различных химических процессов и достижение поставленных целей. Знание основных принципов и задач в этой области позволяет исследователям и инженерам эффективно управлять реакционными системами и создавать новые катализаторы с улучшенными свойствами.
Основной принцип работы переходных металлов заключается в использовании их электронного строения и дислокаций для активации реакций. Высокая реакционная активность переходных металлов обусловлена их способностью образовывать разнообразные комплексы с молекулами реагентов, что позволяет изменять энергетические барьеры реакций.
Одной из основных задач самостоятельной работы с переходными металлами является разработка новых катализаторов с улучшенными свойствами. Катализаторы на основе переходных металлов используются в широком спектре промышленных процессов, начиная от производства пластмасс и пищевой промышленности, заканчивая катализом воздушного окисления.
Оптимизация процессов с использованием переходных металлов имеет широкий спектр применений и позволяет решать различные задачи, такие как повышение селективности реакции, повышение скорости реакции, снижение стоимости процесса и уменьшение вредных выбросов.
Вопрос-ответ

Что такое переходные металлы?
Переходные металлы - это элементы, которые находятся в блоке d таблицы периодических элементов. Они обладают характерными свойствами, такими как высокая термическая и электрическая проводимость, изменчивость валентности и способность образовывать комплексные соединения.
Какая основная задача самостоятельной работы переходных металлов?
Основная задача самостоятельной работы переходных металлов - активировать и катализировать химические реакции. Благодаря своим уникальным свойствам, переходные металлы способны участвовать в множестве реакций, включая окислительно-восстановительные процессы, полимеризацию, газовые реакции и другие.
Какие принципы лежат в основе самостоятельной работы переходных металлов?
Основные принципы самостоятельной работы переходных металлов - это изменчивость валентности и способность образовывать комплексные соединения. Изменчивость валентности означает, что переходные металлы могут изменять свою степень окисления и участвовать в реакциях с различными веществами. Образование комплексных соединений позволяет переходным металлам вступать в стабильные взаимодействия с другими веществами и проявлять свои каталитические свойства.
Какие примеры самостоятельной работы переходных металлов можно привести?
Примерами самостоятельной работы переходных металлов являются множество химических реакций, в которых переходные металлы участвуют в качестве катализаторов. Например, палладий и платина используются в катализаторах для снижения выбросов вредных веществ в выхлопных газах автомобилей. Рутений и родий применяются в катализаторах для превращения азотных оксидов в безопасные газы. Это лишь некоторые примеры применения переходных металлов в самостоятельной работе.
