Сульфаты являются важным классом химических соединений, которые образуются в результате взаимодействия различных металлов с серной кислотой (H2SO4) или солей серной кислоты (SO4). Эти соединения имеют широкий спектр применений, включая использование в фармацевтической, пищевой, химической и других отраслях промышленности. Однако важно отметить, что реакция металлов с сульфатами может иметь различные особенности в зависимости от конкретных условий.
Взаимодействие металлов с сульфатами обычно происходит в результате реакции замещения, при которой металл вытесняет из соли серный катион. К примеру, взаимодействие цинка (Zn) с сульфатом меди (CuSO4) приводит к образованию сульфата цинка (ZnSO4) и осаждению меди на поверхности цинка. Такие реакции могут быть использованы для получения металлов из руд или восстановления окисленных металлов.
Особенности реакции металлов с сульфатами могут быть связаны с различными факторами, включая степень окисления металла, концентрацию и температуру реагирующих веществ, а также наличие катализаторов. Например, взаимодействие сульфата железа (FeSO4) с цинком (Zn) будет протекать быстрее при повышенной температуре и в присутствии катализатора, такой как соляная кислота (HCl).
Важно отметить, что реакция металлов с сульфатами может протекать с выделением газа, такого как водород (H2), или с образованием осадка, который может быть использован для разделения металлов или получения материалов с желаемыми свойствами.
В целом, взаимодействие металлов с сульфатами является важным аспектом в химической промышленности и науке. Понимание особенностей и условий, при которых происходят эти реакции, позволяет улучшить процессы получения и использования сульфатов и обогащает наши знания о химических свойствах металлов.
Взаимодействие SO4 с металлами: что это такое?

SO4 представляет собой сульфатный ион, который образуется при диссоциации серной кислоты. Этот ион широко встречается в природе и может образовывать стабильные соединения с различными металлами.
Взаимодействие SO4 с металлами является одним из примеров реакции окисления-восстановления, которая имеет место при образовании сульфатов металлов. При этой реакции сульфатный ион передает электроны металлу, что приводит к его окислению. В результате образуется сульфат металла и сернистокислый ион.
Важно отметить, что скорость и характер реакции SO4 с металлами зависят от различных факторов, таких как тип металла, его электрохимический потенциал и концентрация SO4. Некоторые металлы могут быстро реагировать с SO4, выделяясь в виде растворимых сульфатов, в то время как другие могут быть менее реактивными или вообще не вступать в реакцию с SO4.
Взаимодействие SO4 с металлами имеет широкое применение в различных областях, включая производство металлических сульфатов, электролиз сульфатных растворов и другие процессы. Кроме того, этот процесс может иметь важное значение в окружающей среде, так как взаимодействие SO4 с металлами может повлиять на биохимические процессы и качество воды.
Общая информация о взаимодействии SO4 с металлами
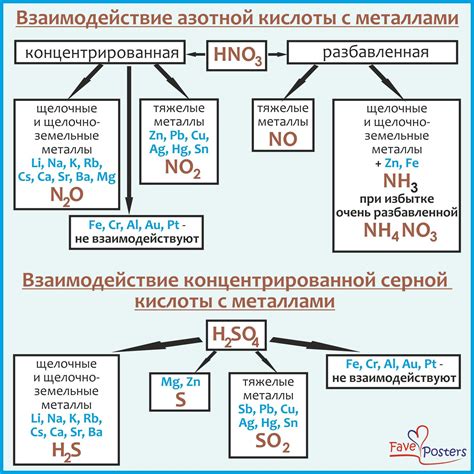
SO4 (сульфат) — анион серной кислоты, который может образовывать соединения с различными металлами. Взаимодействие сульфата с металлами может иметь различные особенности и сочетать в себе как химические, так и физические превращения.
Многие металлы имеют способность реагировать с SO4, образуя соединения сульфата металла. Эти реакции могут происходить с общим участием воды или без нее и могут сопровождаться выделением газов, образованием осадков или изменением цвета реакционной смеси.
Взаимодействие металлов с SO4 может происходить различными способами. Некоторые металлы могут растворяться в серной кислоте, образуя гидратированные ионные соединения. Другие металлы могут образовывать сульфиды при взаимодействии с сульфатом. Еще другие металлы могут образовывать гидроксосульфаты или осадки при реакции с SO4.
Важно отметить, что скорость реакции металлов с SO4, а также продукты реакции зависят от ряда факторов, таких как концентрация реагентов, температура, pH и наличие катализаторов. Также влияние на взаимодействие металлов с SO4 может оказывать их структура и химическая активность.
Взаимодействие SO4 с металлами имеет широкий спектр применений, включая промышленное производство, пищевую и фармацевтическую промышленности, а также в науке и технологии. Изучение этих реакций позволяет углубить понимание химических свойств и поведения металлов в различных условиях и дает возможность разрабатывать новые материалы и технологии на основе этих взаимодействий.
Химические свойства SO4 и их роль в реакции с металлами
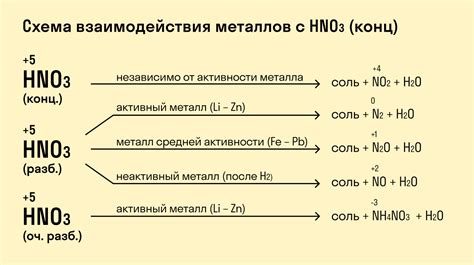
SO4 (сульфат) – наиболее распространенный анион в химии, образующий соли. Обладая отрицательным зарядом, сульфаты активно взаимодействуют с положительно заряженными ионами металлов в реакцияхю Сульфаты имеют высокую устойчивость, что позволяет применять их в различных областях химической промышленности и научных исследованиях.
Во время реакции с металлами, сульфаты обычно выделяются в виде растворов, в которых присутствуют положительно заряженные ионы металлов и отрицательно заряженные ионы сульфата (SO4). Этот процесс называется образованием сульфата металла.
Реакция между SO4 и металлами может протекать по различным механизмам. Например, в некоторых случаях происходит простое обменное взаимодействие, при котором анион сульфата вытесняет другой анион, связанный с металлом. В результате образуется новое соединение, состоящее из металла и сульфата.
Также SO4 может реагировать с металлами путем образования комплексных соединений, где сульфат является лигандом – частицей, образующей координационную связь с металлом. Этот процесс происходит за счет образования новых химических связей между атомами металла и сульфата.
Химические свойства SO4 и ее взаимодействие с металлами играют важную роль в различных областях науки и техники. Например, соединения сульфатов используются в фармацевтической промышленности для производства лекарственных препаратов. Также сульфаты широко применяются в производстве минеральных удобрений, стекла, аккумуляторов и других продуктов. Понимание химических свойств SO4 позволяет оптимизировать процессы синтеза и применять эти соединения в различных сферах деятельности.
Реакция SO4 с различными металлами: особенности и примеры
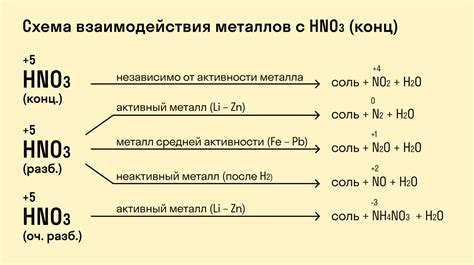
Сульфаты (SO4) являются солями серной кислоты и образуются при реакции металлов с серной кислотой.
Реакция SO4 с металлами может проходить по различным путям в зависимости от свойств металла. Например, активные металлы, такие как натрий (Na) и калий (K), реагируют с сульфатами, образуя сульфат металла и выделяя водород (H2). Такая реакция может быть представлена следующим образом:
2Na + SO4 -> Na2SO4 + H2↑
Другие металлы, такие как железо (Fe) или цинк (Zn), также могут реагировать с сульфатами, но в этом случае выделяется сернистый газ (SO2) вместо водорода. Например:
Zn + H2SO4 -> ZnSO4 + SO2↑ + H2O
Сульфаты некоторых металлов, таких как серебро (Ag) или свинец (Pb), малорастворимы в воде и образуют осадок. Это может быть использовано для определения наличия таких металлов в реакции с сульфатами.
Таким образом, реакция металлов с сульфатами является важным процессом, который может быть использован для получения сульфатов различных металлов или для анализа наличия определенных металлов в реакции.
Влияние физических условий на взаимодействие SO4 с металлами
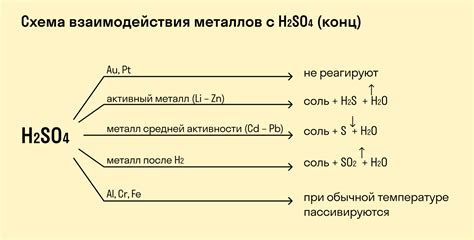
Температура: Взаимодействие металлов с SO4 зависит от температуры. При повышении температуры увеличивается скорость реакции, что способствует активному образованию соединений между металлами и SO4. Однако слишком высокая температура может привести к разрушению соединений и образованию нежелательных продуктов.
Растворимость: Растворимость SO4 в воде также влияет на взаимодействие с металлами. Чем больше растворимость SO4, тем легче осуществляется его вступление в реакцию с металлами. Следует отметить, что некоторые металлы могут быть нерастворимыми в воде, что может затруднить их взаимодействие с SO4.
Концентрация: Концентрация SO4 в реакционной среде оказывает влияние на скорость и характер взаимодействия. При повышении концентрации SO4 увеличивается вероятность столкновения молекул с поверхностью металла, что способствует активации реакции. Однако слишком высокая концентрация SO4 может вызвать насыщение реакционной среды и снижение скорости реакции.
Наличие катализаторов: Некоторые вещества (катализаторы) могут ускорять или замедлять реакцию между SO4 и металлами. Катализаторы повышают эффективность реакции, ускоряя процесс формирования соединений. Однако некоторые катализаторы могут также вызывать побочные реакции или изменять характер образующихся соединений.
Вид и состояние металла: Реакция SO4 с металлами может зависеть от их вида и состояния. Некоторые металлы обладают высокой активностью и быстро реагируют с SO4, в то время как другие металлы могут проявлять меньшую активность или быть пассивными. Также состояние металла (например, его поверхность или форма) может влиять на скорость и характер реакции с SO4.
Аппликации в промышленности и научных исследованиях
Взаимодействие сульфатов (SO4) с металлами является одним из ключевых процессов, используемых в промышленности для получения различных продуктов и материалов.
В промышленности сульфаты применяются в качестве реагентов для осаждения и обработки металлов. Например, сульфат цинка (ZnSO4) используется в гальваническом производстве для электролитического осаждения цинка на металлических поверхностях. Этот процесс позволяет защитить поверхность от коррозии и придать ей декоративное покрытие.
Научные исследования также активно используют взаимодействие сульфатов с металлами. Например, это может быть связано с изучением кинетики реакции между сульфатами и металлами, анализом полученных продуктов и исследованием их свойств и применений.
Также в промышленности очень важен контроль содержания сульфатов в водных системах. Высокая концентрация сульфатов может привести к образованию нерастворимых отложений на поверхностях и в системах теплообмена. Поэтому проводятся научные исследования по разработке и оптимизации методов анализа сульфатов и их удаления, а также по исследованию воздействия сульфатов на окружающую среду и здоровье человека.
В целом, взаимодействие сульфатов с металлами имеет широкое применение в промышленности и научных исследованиях, и его изучение является актуальной темой для разработки новых технологий и материалов.
Безопасность при работе с SO4 и металлами

Работа с SO4 и металлами требует соблюдения определенных мер безопасности, чтобы избежать возможных опасностей и рисков. Во-первых, необходимо обеспечить достаточную вентиляцию места работы, так как при взаимодействии SO4 с металлами выделяются вредные газы.
При контакте SO4 с кожей следует немедленно промыть затронутые участки водой и обратиться за медицинской помощью, так как вещество является раздражающим. Для защиты кожи необходимо использовать защитные перчатки, рукавицы и защитные очки при работе с SO4 и металлами.
Дополнительно следует быть осторожным при работе с металлами, так как они могут быть острыми или горячими. Чтобы избежать порезов и ожогов, необходимо использовать специальный инструментарий и термостойкие перчатки.
Помимо этого, важно соблюдать правила пожарной безопасности при работе с SO4 и металлами. Не рекомендуется хранить и использовать вещества вблизи открытого огня или источников искр. При необходимости использования огня, следует проконсультироваться с профессионалами и принять соответствующие меры предосторожности.
В заключение, безопасность при работе с SO4 и металлами является приоритетом, и необходимо соблюдать все меры предосторожности и инструкции для защиты своего здоровья и предотвращения возможных опасностей.
Вопрос-ответ

Каким образом металлы реагируют с SO4?
Металлы могут взаимодействовать с SO4 посредством окисления металла или редокс-реакции. SO4 может принимать электроны от металла, что приводит к образованию соответствующего оксида металла и сульфата.
Какие металлы могут реагировать с SO4?
Реакция металлов с SO4 возможна для широкого спектра металлов, включая щелочные металлы, щелочноземельные металлы, переходные металлы и даже некоторые полупроводники.
Может ли реакция SO4 с металлом протекать без внешнего источника энергии?
Во многих случаях реакция SO4 с металлом может протекать без внешнего источника энергии, так как это реакция окисления, которая может быть спонтанной при наличии достаточной разницы в энергии между реагентами и продуктами.
Какие особенности имеет реакция SO4 с металлами?
Одной из особенностей реакции SO4 с металлами является образование сульфатов металлов. Также в некоторых случаях могут образовываться газы, такие как SO2, при высокой температуре или концентрации SO4. Кроме того, реакция может быть катализирована или ускорена использованием кислоты или других веществ.
