Взаимодействие разбавленной серной кислоты (H2SO4) с различными металлами является важным объектом исследования в химии. Сульфатная кислота, которая распадается на ионы водорода (H+) и сульфатные ионы (SO42-) в растворе, обладает довольно высокой реакционной способностью.
Взаимодействие металлов с разбавленной серной кислотой может приводить к образованию сульфатов металлов и выделению водорода. Некоторые металлы, такие как цинк (Zn), железо (Fe) и алюминий (Al), реагируют с серной кислотой с образованием соответствующих сульфатов и выделением водорода.
Взаимодействие разбавленной серной кислоты с металлами может быть использовано для получения соединений металлов и доказательства их активности. Также это взаимодействие имеет промышленное применение в процессах очистки металлических поверхностей от ржавчины и других загрязнений.
Однако некоторые металлы, например медь (Cu) и серебро (Ag), не реагируют с разбавленной серной кислотой и не образуют соответствующих сульфатов. Это связано с их относительной пассивностью по отношению к серной кислоте. Такие металлы называются инертными или неподвижными.
Роль разбавленной серной кислоты в реакциях с металлами
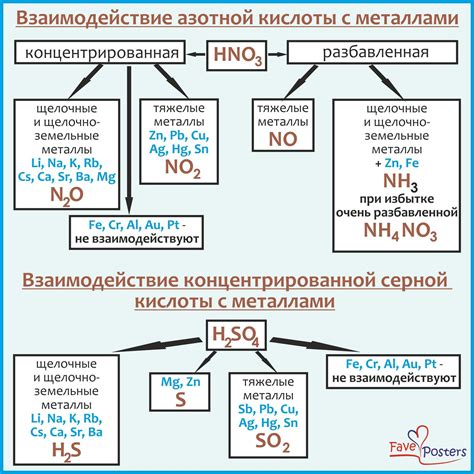
Разбавленная серная кислота является одним из наиболее распространенных реагентов при взаимодействии с металлами. Эта кислота обладает сильными окислительными свойствами, что позволяет ей активно взаимодействовать с различными металлами.
В реакциях с металлами разбавленная серная кислота проявляет свою активность благодаря образованию аниона сернокислого радикала. Взаимодействие разбавленной серной кислоты и металлов сопровождается выделением водорода и образованием соответствующих солей.
Реакция разбавленной серной кислоты с металлами может происходить также с образованием оснований. В этом случае наблюдается образование солей и воды. Примером такой реакции является взаимодействие серной кислоты с натрием, при котором образуется натриевая соль и вода.
Важно отметить, что разбавленная серная кислота является агрессивным химическим соединением и требует осторожного обращения. При взаимодействии с металлами она может вызывать образование взрывоопасных смесей, поэтому необходимо соблюдать меры безопасности и проводить реакции в специально оборудованных условиях.
Влияние концентрации разбавленной серной кислоты на реакцию
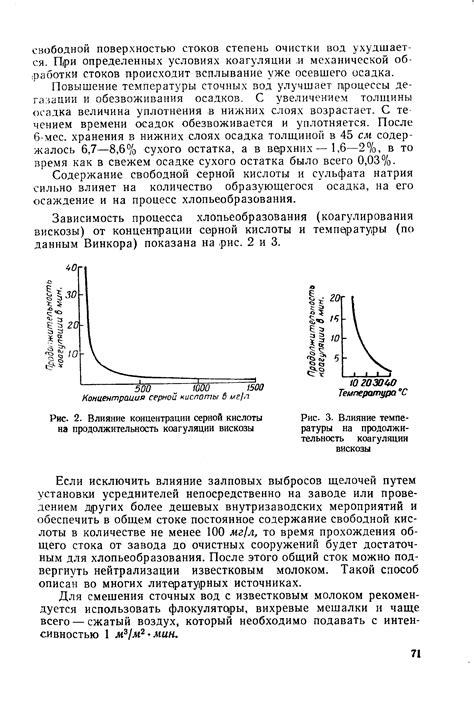
Разбавленная серная кислота, взаимодействуя с различными металлами, проявляет разную активность в зависимости от своей концентрации. Концентрация серной кислоты определяет скорость протекания реакции и степень ее завершенности.
Повышенная концентрация разбавленной серной кислоты повышает скорость реакции с металлами. Это связано с тем, что высокая концентрация серной кислоты обеспечивает большее количество активных ионов в растворе, способных образовывать химические соединения с металлами. Более высокая активность ионов увеличивает количество возможных столкновений между ионами и металлами, что способствует ускорению реакции и повышению степени ее завершенности.
Однако слишком высокая концентрация серной кислоты может привести к разрушению металла и образованию нестабильных соединений. Это связано с высокой кислотностью раствора, которая может вызвать коррозию металла. Для сохранения интегритета металла и предотвращения его разрушения необходимо контролировать концентрацию разбавленной серной кислоты при взаимодействии с металлами.
В итоге, концентрация разбавленной серной кислоты играет важную роль в регулировании реакции с различными металлами. Оптимальная концентрация будет зависеть от конкретных условий и требований процесса. Подбор оптимальной концентрации серной кислоты позволит достичь наилучших результатов взаимодействия металлов и серной кислоты с минимальными потерями и коррозией металла.
Особенности взаимодействия разбавленной серной кислоты с щелочными металлами
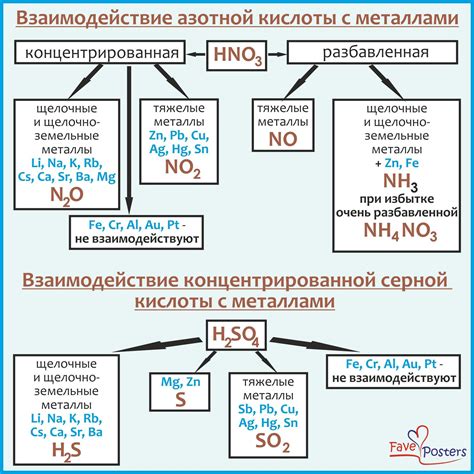
Разбавленная серная кислота является сильным окислителем и реагирует с многими металлами, в том числе с щелочными металлами – натрием, калием и литием. Взаимодействие серной кислоты и щелочных металлов обладает своими особенностями и имеет ряд характерных признаков.
Первым признаком взаимодействия разбавленной серной кислоты с щелочными металлами является выделение водорода. При контакте щелочного металла с разбавленной серной кислотой происходит образование соли и молекулы водорода. Реакция происходит с выделением тепла. Отмечается резкое пенение и шипение смеси.
Вторым характерным признаком является образование соли с шестивалентным состоянием серы. В результате реакции серная кислота окисляет металл до шестивалентного состояния. Образовавшаяся соль может быть растворимой или не растворимой в воде в зависимости от концентрации серной кислоты и исходного металла.
Третьим особенным моментом является возможное образование газа двуокиси серы (SO2). Если концентрация серной кислоты невысока, то при реакции может образоваться SO2. Это связано с реакцией между серной кислотой и образующимся водородом, при которой образуется двуокись серы. Газовый продукт выпускается в виде белой или желтой газовой смеси.
Таким образом, взаимодействие разбавленной серной кислоты с щелочными металлами сопровождается выделением водорода, образованием соли с шестивалентным состоянием серы и возможным образованием газа двуокиси серы. Эти особенности реакции имеют значительное значение в химической промышленности и лабораторных исследованиях.
Реакции между разбавленной серной кислотой и щелочно-земельными металлами

Разбавленная серная кислота – это вещество, которое активно взаимодействует с различными металлами, в том числе и с щелочно-земельными металлами. Щелочно-земельные металлы, такие как магний, кальций, барий и стронций, обладают особыми свойствами и отличаются от других металлов.
При взаимодействии разбавленной серной кислоты с щелочно-земельными металлами происходят химические реакции, в результате которых образуется соответствующий соль и выделяется водород. Данные реакции являются экзотермическими, то есть сопровождаются выделением тепла.
Примером реакции между разбавленной серной кислотой и щелочно-земельным металлом может служить реакция с магнием. При этом образуется магниевая соль и выделяется водородный газ:
- Магний + серная кислота → магниевая соль + водород
Реакция аналогична для других щелочно-земельных металлов.
Целесообразность взаимодействия разбавленной серной кислоты с щелочно-земельными металлами связана с получением соответствующих солей для дальнейшего использования в различных областях промышленности и науки. Также данная реакция может использоваться для получения водорода, важного энергоносителя и промышленного сырья.
Взаимодействие разбавленной серной кислоты с тяжелыми металлами
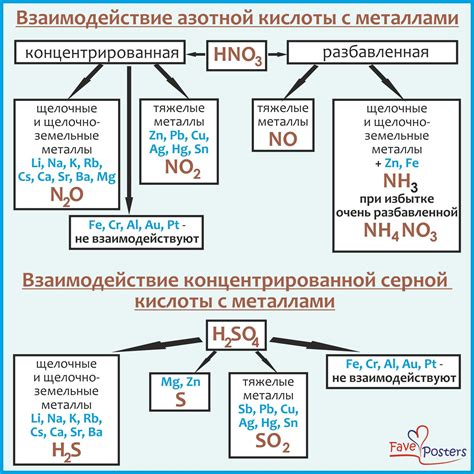
Взаимодействие разбавленной серной кислоты с тяжелыми металлами является важным объектом исследования в химии. Серная кислота (H2SO4) обладает сильно кислотными свойствами и может реагировать с разными металлами.
Тяжелые металлы, такие как свинец (Pb), ртуть (Hg), кадмий (Cd) и другие, обладают высокой плотностью и являются токсичными для организмов живых существ. Изучение взаимодействия этих металлов с серной кислотой позволяет понять механизмы их химической реакции и влияние на окружающую среду.
При взаимодействии разбавленной серной кислоты с тяжелыми металлами происходит образование солей и выделение газов. Например, реакция свинца с серной кислотой приводит к образованию соли свинца (PbSO4) и выделению сероводорода (H2S). Сероводород является ядовитым газом и обладает характерным запахом гнилой яйцекожи.
Изучение взаимодействия разбавленной серной кислоты с тяжелыми металлами позволяет оценить их реакционную способность и определить возможность использования серной кислоты в различных химических процессах. Также это позволяет разработать методы очистки от токсичных металлов и предотвращения загрязнения окружающей среды.
Вклад разбавленной серной кислоты в образование сульфатов
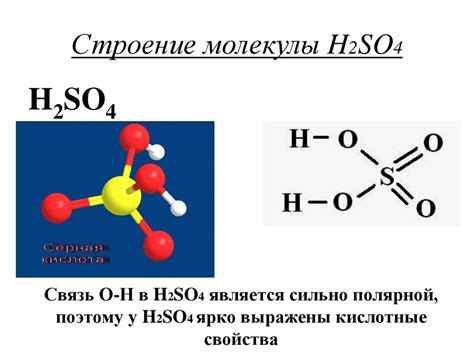
Серная кислота является одним из наиболее распространенных химических соединений, используемых в различных отраслях промышленности. Высокая растворимость серной кислоты в воде способствует ее активному взаимодействию с различными металлическими соединениями, что приводит к образованию сульфатов.
Сульфаты – это соли, образованные в результате реакции серной кислоты с металлами или их оксидами. Разбавленная серная кислота (H2SO4) играет ключевую роль в процессе образования сульфатов. Когда разбавленная серная кислота контактирует с металлом, происходит окислительно-восстановительная реакция, в результате которой металлные ионы переходят в раствор, а водородные атомы присоединяются к серной кислоте.
Важно отметить, что скорость образования сульфатов зависит от ряда факторов, включая концентрацию разбавленной серной кислоты, температуру, время взаимодействия и особенности поверхности металла. Некоторые металлы, такие как цинк и железо, реагируют с серной кислотой достаточно интенсивно и образуют стабильные сульфаты. В то время как некоторые металлы, например, золото или платина, практически не взаимодействуют с серной кислотой.
Таким образом, разбавленная серная кислота играет важную роль в образовании сульфатов путем активного взаимодействия с различными металлами. Это свойство серной кислоты широко используется в различных производственных процессах, а также в химическом анализе для определения присутствия и концентрации металлов в различных образцах.
Опасность взаимодействия разбавленной серной кислоты с металлами
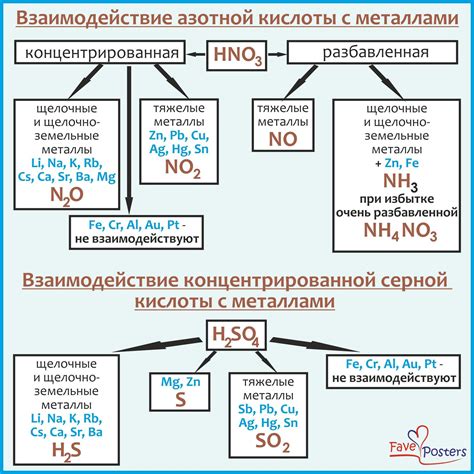
Взаимодействие разбавленной серной кислоты с металлами может представлять опасность для здоровья и безопасности.
Серная кислота, также известная как сульфатная кислота, является химическим соединением, широко используемым в промышленных и лабораторных процессах. Она обладает высокой степенью коррозивности, что делает ее опасной при контакте с металлами.
При взаимодействии разбавленной серной кислоты с металлами, такими как железо, алюминий или цинк, может происходить химическая реакция, называемая окислительно-восстановительной реакцией. В результате этой реакции металл может разлагаться, образуя газы или искры.
Опасность заключается не только в химическом воздействии на металлы, но и в выделении вредных газов. При взаимодействии разбавленной серной кислоты с алюминием, например, выделяются газы диоксид серы и сульфат алюминия, которые могут вызвать раздражение дыхательных путей и кожи, а также негативно повлиять на окружающую среду.
Чтобы предотвратить опасности при работе с разбавленной серной кислотой, необходимо соблюдать все меры предосторожности. Работа с кислотой должна осуществляться в хорошо проветриваемом помещении или под вытяжкой. Рабочее место должно быть оборудовано необходимыми средствами индивидуальной защиты, такими как защитные очки, резиновые перчатки и халат. Также необходимо обращать внимание на совместимость разбавленной серной кислоты с металлами и избегать их взаимодействия.
Выводя информацию на представленной таблицешолучить, что разбавленная серная кислота является опасным химическим соединением при работе с металлами. Необходимо соблюдать все меры предосторожности и профессиональные стандарты безопасности для минимизации рисков и обеспечения безопасности рабочего процесса.
Вопрос-ответ

Какое влияние оказывает разбавленная серная кислота на металлы?
Разбавленная серная кислота обладает коррозионной активностью, поэтому ее взаимодействие с металлами может вызвать коррозию поверхности металла.
Какие металлы реагируют с разбавленной серной кислотой?
Разбавленная серная кислота реагирует с многими металлами, такими как железо, цинк, алюминий, медь, никель и др. Однако, скорость реакции и характер происходящих процессов могут зависеть от концентрации кислоты и особенностей поверхности металла.
Какие продукты образуются в результате взаимодействия разбавленной серной кислоты с железом?
В результате реакции разбавленной серной кислоты с железом образуется железный сульфат и молекулярный водород. Формирующийся железный сульфат может быть в виде раствора или осадка, в зависимости от концентрации и условий проведения эксперимента.
Чем объясняется различие в скорости реакции разбавленной серной кислоты с разными металлами?
Скорость реакции разбавленной серной кислоты с металлами зависит от активности металла и концентрации кислоты. Металлы с большей активностью, такие как алюминий и цинк, быстрее реагируют с кислотой, чем металлы с меньшей активностью, например, медь и серебро.
Может ли разбавленная серная кислота вызвать повреждение металлических изделий или поверхностей?
Да, разбавленная серная кислота может повредить металлические изделия или поверхности, так как она обладает агрессивными коррозионными свойствами. Поэтому при работе с кислотой необходимо соблюдать меры безопасности и использовать средства защиты.
