Щелочные металлы - это группа химических элементов, которые находятся в первой группе периодической таблицы. Этот ряд состоит из лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Щелочные металлы имеют много различных физических и химических свойств, которые делают их особенно интересными для изучения.
Все щелочные металлы обладают свойствами, общими для этой группы элементов. Они очень реактивны и легко образуют ионы с положительным зарядом, потому что имеют только один электрон в своей внешней оболочке. Это делает их хорошими источниками электронов и позволяет им вырабатывать энергию при взаимодействии с другими веществами.
Щелочные металлы также хорошо проводят электричество и тепло. Это свойство делает их полезными в различных приложениях, включая производство батарей, стеклопроизводство и использование в электронике. Однако, из-за их высокой реактивности, они должны быть обрабатываться с осторожностью, чтобы избежать взрывоопасных ситуаций и опасного воздействия на человека и окружающую среду.
Важно отметить, что какие-то отличия в свойствах между щелочными металлами существуют. Например, наиболее примечательным является то, что их плотности и точки плавления возрастают по мере движения вниз по группе. Кроме того, щелочные металлы образуют различные соединения и имеют разные реакционные способности в химических реакциях, что делает каждый элемент в группе неповторимым и интересным для исследования.
Свойства щелочных металлов

Щелочные металлы – это особая группа металлов, которые обладают рядом характерных свойств. В их число входят литий, натрий, калий, рубидий, цезий и франций.
Первое свойство, характерное для щелочных металлов, это низкая плотность. Они являются легкими металлами и обладают малыми атомными массами. Например, литий имеет плотность всего 0,53 г/см³, а калий – 0,86 г/см³.
Еще одно свойство щелочных металлов – очень низкая температура плавления. Литий плавится при температуре всего 180 градусов Цельсия, а калий – при 63 градусах Цельсия. Это обусловлено слабой металлической связью между атомами, которая не требует большого количества энергии для разрыва.
Щелочные металлы активно реагируют с водой, выделяя водород. Это свойство объясняется их низкой ионизационной энергией и способностью сильно окисляться. Реакция с водой протекает взрывоопасно, особенно в случае с калием и цезием.
Щелочные металлы обладают высокой электроотрицательностью, что позволяет им образовывать ионы с положительным зарядом. Они легко отдают электроны в химических реакциях, что делает их сильными окислителями.
Также щелочные металлы имеют низкую температуру кипения и высокие значения энтальпии испарения. Литий, например, кипит при 1347 градусах Цельсия и имеет теплоту испарения 147 кДж/моль.
Что такое щелочные металлы?
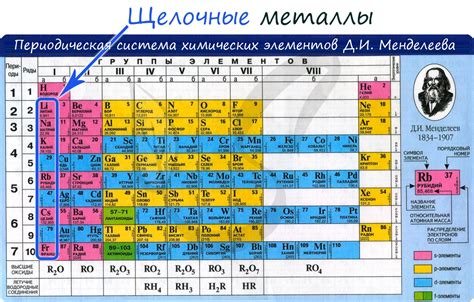
Щелочные металлы - это группа элементов, расположенных в первой группе периодической системы. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы получили свое название из-за своей реактивности и способности образовывать щелочные растворы при взаимодействии с водой.
Основные свойства щелочных металлов:
- Щелочные металлы имеют мягкую текстуру и низкую плотность. Литий является самым легким металлом, а цезий - самым плотным.
- Они обладают низкой температурой плавления и кипения, что делает их хорошими материалами для использования в различных промышленных процессах.
- Щелочные металлы очень реактивны и легко образуют соединения с другими элементами. Они реагируют с водой, кислородом и многими органическими соединениями.
- У них низкая ионизационная энергия, что означает, что они легко отдают электроны и образуют положительные ионы. Это делает их хорошими реагентами и прекрасными проводниками электричества.
- Щелочные металлы имеют низкую электроотрицательность, что делает их активными металлами в химических реакциях и способствует образованию ионов.
Щелочные металлы находят широкое применение в различных отраслях промышленности, включая производство стекла, лекарств, батарей и многих других продуктов. Они играют важную роль в нашей повседневной жизни и имеют большое значение для развития технологий и науки.
Ряд щелочных металлов
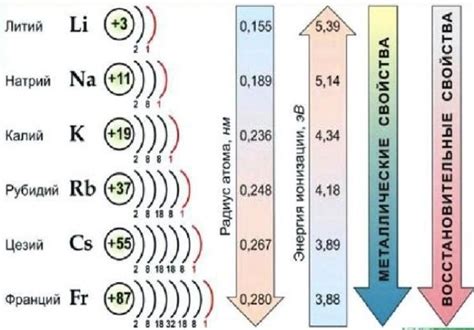
Щелочные металлы - это элементы, которые относятся к первой группе периодической системы. В этой группе находятся литий, натрий, калий, рубидий, цезий и франций. Они имеют очень низкую плотность и мягкость, а также низкую температуру плавления и кипения.
Плотность щелочных металлов увеличивается в ряду от лития до франция. Литий - самый легкий металл, его плотность составляет всего около 0,5 г/см³. Франций, самый тяжелый металл в этой группе, имеет плотность около 1,87 г/см³.
Щелочные металлы обладают высокой атомарной массой и атомным радиусом, что делает их хорошими химическими исследовательскими материалами. Они также хорошо проводят электричество и тепло, и используются в различных электротехнических и теплоотводящих приложениях.
Кроме того, щелочные металлы легко реагируют с водой и воздухом, образуя щелочные растворы и оксиды. Например, натрий реагирует с водой, выделяясь водородом и образуя щелочное растворение натриевого гидроксида. Эти реакции могут быть очень бурными и выделять много тепла.
Физические свойства щелочных металлов

Щелочные металлы - это группа химических элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). У этих металлов есть ряд характерных физических свойств, которые отличают их от других элементов.
1. Мягкость и низкое плавление: Щелочные металлы обладают мягкой текстурой, их можно легко резать ножом. В связи с этим, они имеют низкую точку плавления (ниже 500 °C), что делает их хорошими плавильными металлами.
2. Низкая плотность: Щелочные металлы обладают низкой плотностью, что означает, что они очень легкие. Например, литий является самым легким металлом в периодической таблице. Это делает их полезными в различных областях, включая авиацию и космическую промышленность.
3. Активность: Щелочные металлы очень активны и реагируют с кислородом и водой. Например, натрий и калий реагируют с водой с выделением водорода и образованием гидроксидов щелочных металлов. Их активность также проявляется в способности легко образовывать ионы с положительным зарядом.
4. Низкая электроотрицательность: Щелочные металлы имеют низкую электроотрицательность, что делает их отличными металлическими проводниками электричества. Благодаря своим свойствам они широко используются в различных электрических приборах.
5. Одинаковые химические свойства: У всех щелочных металлов есть схожие химические свойства. Они легко образуют соли и гидроксиды, но не растворяются в спирте. Также они способны образовывать различные соединения и проводить химические реакции с другими элементами.
Химические свойства щелочных металлов
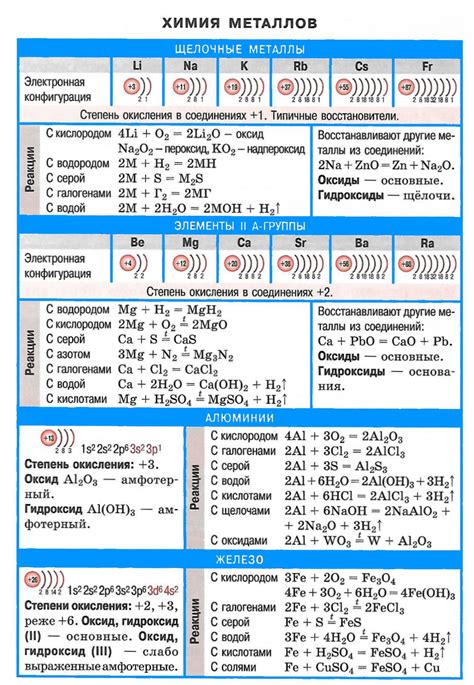
Щелочные металлы представляют собой ряд элементов, включающих литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). У этих металлов есть несколько общих химических свойств, которые они проявляют благодаря наличию одного электрона во внешней электронной оболочке.
Одним из основных свойств щелочных металлов является активность. Они легко реагируют с кислородом и водой, образуя щелочные оксиды и гидроксиды соответственно. Например, натрий при контакте с водой выделяет водород и образует гидроксид натрия (щелочной раствор). Эта способность щелочных металлов реагировать с водой также приводит к тому, что они легко растворяются в этом растворителе.
Другим важным свойством щелочных металлов является их реактивность с другими веществами, такими как кислоты и хлор. Они образуют соль и выделяются водородные газы. Например, натрий реагирует с хлором, образуя хлорид натрия, одну из наиболее распространенных солей.
Также следует отметить, что щелочные металлы обладают способностью образовывать различные соединения и смеси, включая сплавы с другими металлами. Некоторые из этих сплавов имеют большое значение в промышленности, например, легированные алюминий-литиевые сплавы, которые отличаются высокой прочностью и низкой плотностью.
Вопрос-ответ

Какие металлы входят в щелочные ряды?
Щелочные ряды включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Какие свойства характерны для щелочных металлов?
Щелочные металлы обладают такими свойствами, как мягкость, низкую плотность, низкую температуру плавления и кипения, яркую металлическую блескость, низкую твердость и хорошую проводимость электричества и тепла.
