Активные металлы являются важной группой химических элементов, которые взаимодействуют с водородом и образуют так называемый ряд активных металлов до водорода. Этот ряд состоит из элементов периодической таблицы, которые расположены выше водорода и включают литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs).
Основная особенность активных металлов до водорода заключается в их способности реагировать с водородом, образуя соединения, называемые гидридами. Эти гидриды обладают высокой химической активностью и могут быть использованы в различных химических реакциях и промышленных процессах.
Также активные металлы до водорода обладают низкой плотностью, что делает их легкими и подходящими для использования в различных технических приложениях. Они также обладают хорошей электропроводностью и высокой теплопроводностью, что делает их ценными материалами для производства электроники и других устройств.
Примечательно, что активные металлы до водорода имеют низкую температуру плавления и кипения, что делает их подходящими для использования в низкотемпературных приложениях, таких как жидкий азот и жидкий гелий.
Исследования и применение активных металлов до водорода продолжаются, и их свойства и потенциал в различных областях все еще являются предметом интереса для ученых и инженеров.
Химическое свойство металлов

Металлы обладают рядом химических свойств, которые отличают их от других элементов. Одной из основных характеристик металлов является их способность образовывать ионные соединения. Это означает, что металлы часто теряют электроны и образуют позитивно заряженные ионы, которые после могут образовывать связи с отрицательно заряженными ионами или не-металлами.
Еще одной важной особенностью металлов является их химическая активность. Большинство металлов имеют высокую активность и легко реагируют с другими веществами. Например, металлы могут реагировать с кислородом, образуя оксиды, или с водой, образуя гидроксиды. Такие реакции часто сопровождаются выделением тепла и света. Это объясняет, почему большинство металлов можно увидеть блестящими поверхностями.
Также металлы обладают характеристикой подобной возможности смены степени окисления. Некоторые металлы могут образовывать несколько степеней окисления, что позволяет им образовывать различные соединения с разными электрохимическими свойствами. Это отражает способность металлов образовывать различные ионы и находиться в разных химических состояниях.
Таким образом, химическое свойство металлов определяется их способностью образовывать ионные соединения, высокой химической активностью и возможностью смены степени окисления. Эти свойства делают металлы полезными в различных областях, включая промышленность, электронику и строительство.
Физические свойства металлов
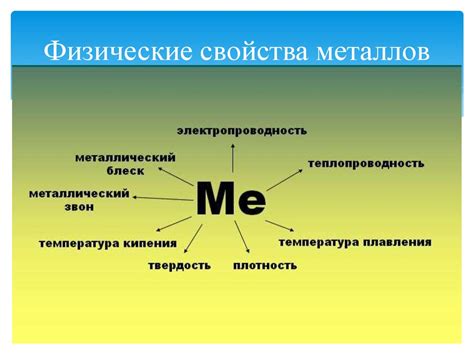
Металлы обладают рядом характерных физических свойств, которые отличают их от других классов материалов. Во-первых, металлы обладают высокой тепло- и электропроводностью. Это связано с наличием свободных электронов, которые могут свободно двигаться под влиянием приложенного электрического поля. Благодаря этому, металлы применяются в электротехнике и электронике.
Во-вторых, металлы обладают блестящей поверхностью, которая проявляется в ярком отражении света. Это свойство называется металлическим блеском. Благодаря этому, металлы использовались в производстве украшений и драгоценных металлов.
Третья характеристика металлов - пластичность. Металлы легко принимают форму ковки, прокатки и вытягивания под действием давления. Это свойство позволяет создавать сложные и устойчивые конструкции, такие как мосты, здания и машины.
Другой важной характеристикой металлов является их высокая плотность. Металлы обладают высокой массой на единицу объема, что делает их тяжелыми. Из-за высокой плотности металлы применяются в авиации и строительстве для создания прочных и надежных конструкций.
Наконец, металлы имеют высокую температуру плавления, которая позволяет им переходить из твердого состояния в жидкое при достаточно высокой температуре. Это свойство делает металлы подходящими для использования в различных промышленных процессах и производстве различных материалов.
Активные металлы в химической промышленности

Активные металлы, такие как литий, натрий, калий, магний и алюминий, являются неотъемлемой частью химической промышленности. Они обладают рядом уникальных свойств, которые делают их незаменимыми материалами для различных процессов и производств.
Литий используется в производстве аккумуляторов, а также в качестве катализатора и растворителя. Его низкая плотность и высокая энергетическая ёмкость делают его идеальным материалом для создания легких и эффективных аккумуляторов для электромобилей и портативных устройств.
Натрий широко используется в промышленности для производства щелочных металлов, стекла, органических соединений и многих других веществ. Он также используется в пищевой промышленности в качестве пищевой добавки E-500 для регулирования pH и улучшения текстуры и структуры продуктов.
Калий является одним из основных элементов плодородной почвы и используется в сельском хозяйстве в виде удобрений. Он также используется в промышленности для производства стекла, мыла, красителей и других продуктов.
Магний широко применяется в автомобильной и аэрокосмической промышленности из-за его низкой плотности, жаропрочности и прочности. Он используется для создания легких сплавов, которые используются в производстве автомобилей, самолетов и других транспортных средств.
Алюминий является одним из самых распространенных металлов в мире. Он используется во многих отраслях промышленности, включая автомобильную, строительную, упаковочную и даже космическую. Алюминиевые сплавы обладают высокой прочностью, низкой плотностью и хорошей стойкостью к коррозии, что делает их идеальными для создания легких и прочных конструкций.
Все эти активные металлы играют важную роль в химической промышленности, обеспечивая различные процессы и производства в разных отраслях.
Окисление активных металлов

Активные металлы, такие как натрий, калий и литий, легко окисляются при взаимодействии с кислородом из воздуха. Окисление активных металлов происходит в результате химических реакций, в которых активный металл соединяется с кислородом.
Окисление активных металлов может приводить к образованию оксидов и гидроксидов. Например, окисление натрия приводит к образованию оксида натрия (Na2O) или гидроксида натрия (NaOH). Окисление калия приводит к образованию оксида калия (K2O) или гидроксида калия (KOH).
Окисление активных металлов может происходить при обычной комнатной температуре, однако оно ускоряется при повышенной температуре или в присутствии катализаторов. Также окисление активных металлов может происходить в более агрессивных условиях, например, при контакте с кислотами или другими окислителями.
Окисление активных металлов является химической реакцией, которая может приводить к образованию новых химических соединений. Это явление имеет важное значение как в химических процессах, так и в промышленности. Окисление активных металлов может быть как полезным, так и опасным явлением, в зависимости от контекста его применения.
Металлы в периодической системе
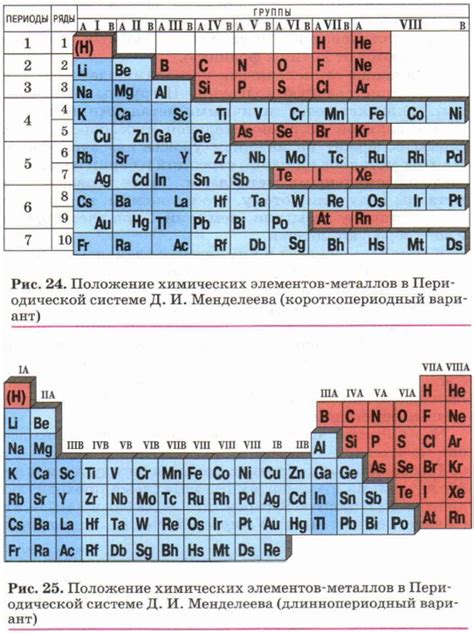
Металлы занимают большую часть таблицы Менделеева и представлены во всех строках. Они обладают характерными свойствами: высокой пластичностью, проводимостью электричества и тепла, блеском, твердостью и хорошей коррозионной стойкостью.
В таблице Менделеева металлы организованы в левой части и в центре. В левой части таблицы расположены щелочные металлы (литий, натрий, калий, рубидий, цезий и франций) и щелочноземельные металлы (бериллий, магний, кальций, стронций, барий и радий). Они обладают низкой плотностью и низкой температурой плавления.
Металлы в центре таблицы Менделеева, такие как алюминий, железо, медь, никель, свинец, алюминий, цинк, железо и титан, являются переходными металлами. Они имеют разную степень валентности и формируют многообразные соединения с другими элементами.
В таблице Менделеева также присутствуют лантаноиды и актиноиды, которые являются редкоземельными металлами и имеют сложные электронные конфигурации. Они имеют множество применений в различных областях, от техники до медицины.
Металлы в периодической системе играют важную роль в нашей жизни, используя свои свойства для создания различных материалов и продуктов, которые мы ежедневно используем.
Вещества, образуемые активными металлами
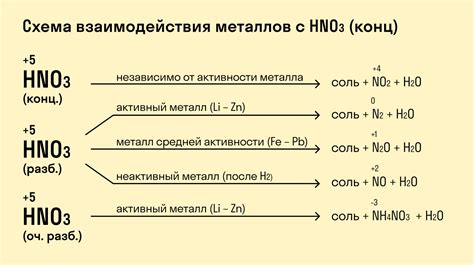
Активные металлы обладают высокой реакционной способностью, что позволяет им образовывать различные вещества. Одним из наиболее распространенных соединений, которые образуют активные металлы, являются гидроксиды. Гидроксиды активных металлов обычно имеют формулу MOH, где M - металл, а OH - гидроксильная группа. Они обладают щелочными свойствами и широко применяются в промышленности и быту.
Активные металлы также образуют соли, в частности хлориды, нитраты, сульфаты и другие. Например, хлориды активных металлов обычно обладают высокой растворимостью в воде и образуют бесцветные или белые кристаллы. Они находят широкое применение в химической промышленности, медицине и других отраслях.
Кроме того, активные металлы могут образовывать соединения с кислородом, например, оксиды. Оксиды активных металлов могут иметь различные цвета и физические свойства. Некоторые из них являются основными оксидами, образуя гидроксиды при контакте с водой. Оксиды активных металлов широко применяются в качестве катализаторов, конструкционных материалов и в других областях промышленности.
Также активные металлы могут образовывать сплавы с другими металлами. Сплавы активных металлов обладают уникальными свойствами, которые позволяют им применяться в различных отраслях промышленности, включая авиацию, энергетику и машиностроение.
Вопрос-ответ

Какие металлы входят в ряд активных металлов до водорода?
В ряд активных металлов до водорода входят следующие элементы: литий, натрий, калий, рубидий и цезий.
Какие основные свойства активных металлов до водорода?
Основные свойства активных металлов до водорода включают высокую реактивность, низкую плотность, низкую температуру плавления и кипения, а также способность образовывать ионы положительного заряда (катионы) в химических соединениях.
