Хром – один из самых распространенных и важных химических элементов, обладающий поразительными химическими свойствами. В зависимости от своей окислительной способности, хром может образовывать различные соединения, проявляющиеся в его разнообразных химических активностях. Этот элемент способен как окисляться, так и восстанавливаться, что является основой для многих химических реакций и процессов.
Одно из самых известных проявлений активности хрома – его способность образовывать сложные соединения, такие как хроматы и дихроматы. Хроматы – соли хромовой кислоты, обладающие ярким цветом. В зависимости от различных условий, они могут иметь разные оттенки, от желтого до оранжевого. Дихроматы – вещества, содержащие два атому хрома, которые проявляют активность при окислении органических соединений. Они широко используются в химической промышленности, включая процессы окисления и выведения веществ из органических соединений.
Хром также активно взаимодействует с кислородом, образуя оксиды хрома. В зависимости от степени окисления элемента, могут образовываться различные соединения, такие как трехвалентный оксид хрома (Cr2O3) или шестивалентный оксид хрома (CrO3). Эти соединения являются важными сырьевыми материалами для производства различных химических соединений и применяются в разных отраслях промышленности, включая керамику, стекло и лакокрасочную промышленность.
Роль хрома в химических процессах

Хром является одним из самых активных химических элементов, который активно участвует во многих процессах. Одной из главных ролей хрома является его способность окисляться и восстанавливаться. Благодаря этому, хром может образовывать различные оксиды, которые обладают разной степенью окислительной активности.
Хром также принимает участие в образовании сложных соединений. Он способен формировать комплексные соединения с разными лигандами, такими как аммиак, воды, карбонаты и другие. Эти соединения обладают разными свойствами и могут применяться в различных областях, включая каталитические процессы и производство лекарственных препаратов.
Хром также широко используется в производстве различных материалов, включая стали, сплавы и покрытия. Он добавляется к металлическим сплавам, чтобы улучшить их прочность и устойчивость к коррозии. Хром-покрытия также применяются для придания декоративного эффекта и защиты от внешних воздействий.
Кроме того, хром является важным компонентом в процессе травления и гальванического осаждения. Он используется для удаления оксидных пленок с поверхности металлов и создания равномерного и гладкого покрытия на разных материалах.
Важность хрома в организме

Хром является одним из важных микроэлементов, необходимых для нормального функционирования организма человека. Он играет ключевую роль в регуляции уровня глюкозы в крови, обмене веществ и работы некоторых ферментов.
Хром является важным компонентом гормона инсулина, который отвечает за регулирование уровня сахара в крови. Он помогает инсулину доставлять глюкозу в клетки, где она используется для получения энергии. Недостаток хрома может привести к снижению чувствительности клеток к инсулину и развитию сахарного диабета.
Хром также участвует в обмене жиров и белков. Он помогает усваивать и использовать жиры и белки, что является важным для поддержания здорового обмена веществ. Недостаток хрома может привести к нарушению обмена веществ и набору лишнего веса.
Кроме того, хром имеет антиоксидантные свойства. Он помогает защищать организм от вредного воздействия свободных радикалов, которые могут привести к повреждению клеток и возникновению различных заболеваний. Хром также способствует активации некоторых ферментов, которые участвуют в процессе детоксикации организма.
Выводя итог, хром является неотъемлемым элементом для поддержания нормального метаболизма, работы инсулина и защиты организма от окислительного стресса. Для обеспечения достаточного уровня хрома необходимо правильное питание, включающее продукты, богатые этим микроэлементом, такие как орехи, цельнозерновые продукты, мясо, рыба и некоторые овощи и фрукты.
Реакции окисления хрома
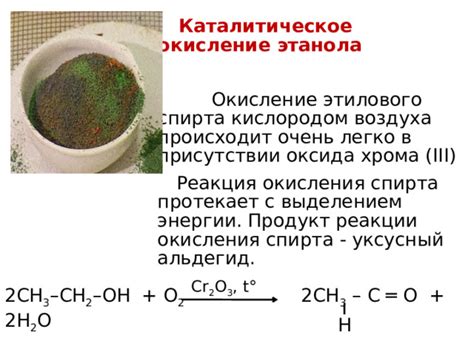
Хром является химическим элементом, обладающим выраженными окислительно-восстановительными свойствами. Реакции окисления хрома имеют множество применений и оказывают значительное влияние на различные процессы в природе и в промышленности.
Одной из наиболее известных реакций окисления хрома является образование оксида хрома(III) при вступлении хрома в контакт с кислородом. Эта реакция широко применяется в производстве окрасочных материалов, так как оксид хрома обладает ярким зеленым цветом и обеспечивает стойкость окраски.
Еще одной реакцией окисления хрома является получение хроматов и дихроматов. При окислении хрома кислотными растворами образуются соединения, которые широко используются в промышленности, включая хромирование поверхностей и производство красителей.
Реакции окисления хрома особенно важны в биологических системах. Один из самых распространенных примеров - окисление хрома в организмах с помощью ферментов. Эти реакции позволяют организмам использовать энергию, содержащуюся в пищевых продуктах, и поддерживать жизнедеятельность.
Образование комплексных соединений с хромом

Хром является элементом блока d периодической системы и обладает свойством образования комплексных соединений. Комплексные соединения с хромом представляют собой соединения, в которых центральный атом хрома связан с другими атомами или группами атомов, называемыми лигандами. Образование комплексных соединений характеризуется обменом электронами между хромом и лигандами, что приводит к образованию ковалентных связей.
Комплексные соединения с хромом имеют разнообразные свойства и находят применение в различных областях науки и техники. Например, комплексы хрома используются в качестве катализаторов реакций окисления и гидролиза. Благодаря своей активности, они могут ускорять химические процессы, происходящие в органических и неорганических веществах.
Одним из наиболее известных комплексных соединений с хромом является дихромат калия (K2Cr2O7), широко применяемый в аналитической химии для окраски и детекции различных веществ. Другим примером является сульфат хрома(III) (Cr2(SO4)3), который используется в процессе крашения тканей и кожи, а также в производстве красок и пигментов.
Образование комплексных соединений с хромом играет важную роль не только в химии, но и в биологии. Например, хром является необходимым микроэлементом для нормальной работы организма человека и играет важную роль в обмене веществ. Также комплексы хрома используются в медицине для лечения различных заболеваний, таких как сахарный диабет и анемия.
Применение хрома в промышленности

Хром является важным элементом в различных отраслях промышленности благодаря своим уникальным химическим свойствам. Одним из основных применений хрома является его использование в производстве стали. Хром добавляется в сталь для повышения ее прочности, устойчивости к коррозии и термической стойкости. Также хром способствует формированию защитной оксидной пленки на поверхности стали, предотвращающей ржавление.
Хром также широко используется в производстве сплавов, которые находят применение в авиационной, автомобильной и судостроительной промышленности. Эти сплавы отличаются высокой прочностью и стойкостью к различным воздействиям, таким как высокие температуры и коррозия. Благодаря этим свойствам хромовые сплавы находят широкое применение в производстве двигателей, рам для автомобилей и судов, а также различных частей для авиационных и космических аппаратов.
В промышленности также используются растворы хрома для проведения различных покрытий и отделочных работ. Хромовые покрытия имеют высокую стойкость к коррозии, обладают эстетическим видом и могут быть сделаны с различными оттенками, в том числе зеркальным или матовым финишем. Такие покрытия применяются в автомобильной, электронной и мебельной промышленности, а также для создания ювелирных изделий.
Кроме того, хром используется в производстве красок и пигментов. Хромовые красители характеризуются яркой и насыщенной окраской, а также высокой стойкостью к внешним воздействиям, таким как ультрафиолетовое излучение или химические реактивы. Это делает их популярными в производстве красок для автомобилей, строительных материалов, текстиля и других товаров.
Вопрос-ответ

Какие процессы происходят при окислении хрома?
При окислении хрома происходит потеря электронов, что приводит к изменению его валентности. В результате образуются оксиды, такие как трехвалентный оксид хрома (Cr2O3) или шестивалентный оксид хрома (CrO3).
Как хром взаимодействует с кислородом?
Хром может образовывать различные оксиды при взаимодействии с кислородом. Одним из наиболее известных является трехвалентный оксид хрома (Cr2O3), который имеет красновато-коричневый цвет и широко используется в производстве красок и лаков.
Какие составные части содержит хром?
Хром может образовывать комплексные соединения. Одним из наиболее известных является хроматы (CrO4^2-). Хроматы являются сильными окислителями и часто используются в аналитической химии для определения различных веществ.
Какие соединения хрома наиболее ядовиты?
Некоторые соединения хрома могут быть ядовитыми при попадании в организм. Например, шестивалентный хромат (CrO3) и шестивалентный дихромат (Cr2O7^2-) являются сильными окислителями и могут вызвать ожоги или ядовитое отравление. Поэтому необходимо соблюдать осторожность при работе с такими веществами.
