Металлы - это вещества, которые обладают характерными свойствами: твердость, блеск, проводимость тепла и электричества. Каждый металл обладает своей степенью активности, которая определяет его способность участвовать в химических реакциях. В данной презентации мы рассмотрим активность металлов и их взаимодействие с другими веществами.
Активность металлов можно представить в виде ряда активности, где металлы располагаются в порядке убывания их химической активности. Самыми активными металлами являются щелочные металлы, такие как литий, натрий, калий и др. Они очень реакционны и способны взаимодействовать с водой, выделяя горючие газы и образуя щелочные растворы.
Водород, несмотря на то, что он химически является неметаллом, также имеет высокую активность и может вступать в реакцию с металлами. При взаимодействии металлов с водородом образуются металлогидриды, которые часто используются в промышленности, например, в процессах хранения и транспортировки водорода.
Взаимодействие металлов с кислотами является одним из наиболее известных и распространенных примеров химических реакций. Металлы реагируют с кислотами, образуя соли и выделяя водородный газ. Например, при взаимодействии цинка с серной кислотой образуется сульфат цинка и выделяется водородный газ по общему уравнению: Zn + H₂SO₄ → ZnSO₄ + H₂.
Активность металлов определяет их способность вступать в окислительно-восстановительные реакции. Некоторые металлы легко окисляются, т.е. отдают электроны, а другие металлы легко восстанавливаются, т.е. принимают электроны. Этот процесс происходит при взаимодействии металлов с кислородом, одним из самых распространенных окислителей. Например, железо при окислении образует ржавчину, а алюминий не окисляется на воздухе.
Металлы и их значения

Металлы - это химические элементы, обладающие способностью проводить тепло и электричество, выраженной металлическими свойствами.
Металлы имеют большую электропроводность, что делает их незаменимыми в конструкциях, например, в электрических проводах и контактах.
Металлы также обладают высокой теплопроводностью, что позволяет им применяться в производстве нагревательных элементов и теплообменников.
Отдельно следует отметить, что металлы обладают высокой пластичностью и прочностью, что делает их идеальными для создания различных металлических конструкций.
Металлы часто используются в производстве различных предметов повседневного пользования, таких как посуда, инструменты, монеты и т.д.
- Алюминий - легкий, прочный и коррозионностойкий металл, широко используется в авиационной и автомобильной промышленности.
- Железо - один из самых распространенных металлов, используется в строительстве, машиностроении, производстве стали и др.
- Медь - хороший проводник электричества и тепла, используется в электротехнике и в производстве различных медных изделий.
- Свинец - имеет высокую плотность и низкую плавкость, используется в производстве аккумуляторов и волоконно-оптических кабелей.
- Цинк - применяется для защиты других металлов от коррозии и в производстве сплавов.
Классификация металлов
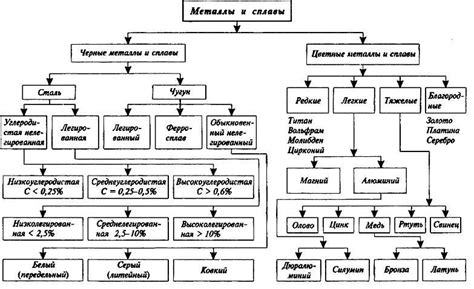
Металлы — это группа химических элементов, которые обладают определенными физическими и химическими свойствами. Все металлы можно разделить на две основные группы: благородные и обычные металлы.
Благородные металлы — это металлы, которые обладают высокой химической стойкостью и реактивностью. К этой группе относятся золото, серебро и платина. Они имеют высокую плотность и отличаются особым блеском, что делает их привлекательными для использования в ювелирных изделиях и монетах.
Обычные металлы — это металлы, которые широко распространены в природе и имеют множество различных применений. В эту группу входят алюминий, железо, медь, цинк, олово и другие. Они легко обрабатываются и имеют высокую электропроводность, что делает их идеальными для использования в различных отраслях промышленности.
Также металлы можно классифицировать по их химическим свойствам. Эта классификация включает легкоплавкие, тяжеловесные и щелочноземельные металлы. Легкоплавкие металлы, такие как натрий и калий, имеют низкую температуру плавления и используются, например, в процессе сварки. Тяжеловесные металлы, например, свинец и ртуть, обладают высокой плотностью и используются в различных индустриях, включая электронику и аккумуляторы. Щелочноземельные металлы, такие как магний и кальций, являются основными компонентами земной коры и находят широкое применение в сельском хозяйстве и строительстве.
Классификация металлов играет важную роль в изучении их свойств и применении в различных областях человеческой деятельности. Понимание различий между разными типами металлов позволяет нам лучше использовать их потенциал и создавать новые материалы и технологии.
Свойства металлов

Проводимость электричества: Одно из главных свойств металлов - их способность проводить электрический ток. Это объясняется наличием свободных электронов в их структуре, которые могут свободно перемещаться и образовывать электрический ток.
Теплопроводность: Металлы обладают также высокой способностью проводить тепло. Это связано с высокой подвижностью электронов, которые переносят тепловую энергию с одного места на другое.
Пластичность: Металлы обладают способностью изменять свою форму без разрушения. Их можно легко прокатывать, ковать, растягивать и формировать. Это обусловлено наличием свободных электронов, которые способствуют деформации металла без образования трещин и разрывов.
Прочность: Металлы обычно обладают высокой прочностью и устойчивостью к механическим воздействиям. Их кристаллическая структура и наличие свободных электронов позволяют им выдерживать большие нагрузки без разрушения.
Сверхпроводимость: Некоторые металлы при очень низких температурах становятся сверхпроводниками, то есть способны проводить электрический ток без сопротивления. Это свойство находит широкое применение в современной электротехнике и медицине.
Окисление: Металлы могут окисляться при контакте с кислородом воздуха или веществами, содержащими окислители. Окисление может привести к образованию покрытия (пленки) на поверхности металла, которое защищает его от дальнейшей коррозии.
Плотность: Металлы обычно обладают высокой плотностью, что означает, что их масса в единице объема может быть достаточно большой. В связи с этим металлы обычно тяжелые и плотные материалы.
Влияние металлов на окружающую среду

Металлы являются важным элементом для различных отраслей промышленности и применяются в производстве множества товаров, но, к сожалению, их использование также оказывает негативное влияние на окружающую среду.
Одним из основных источников загрязнения окружающей среды является выбросы металлов в атмосферу. При сжигании угля, нефтепродуктов и других топлив, в атмосферу попадают оксиды металлов, которые способны вызывать серьезные заболевания у человека и животных. Также выбросы металлов в атмосферу являются главными причинами кислотных дождей и изменения климата.
Окружающая среда также страдает от загрязнения воды металлами. Промышленные предприятия сбрасывают отходы, содержащие тяжелые металлы, в реки, озера и океаны. Это приводит к отравлению водных организмов и ухудшению качества питьевой воды.
Кроме того, производство и переработка металлов требуют использования большого количества энергии и водных ресурсов. Это приводит к эксплуатации природных ресурсов и увеличению выбросов парниковых газов, что имеет негативное влияние на климат.
Для снижения негативного влияния металлов на окружающую среду необходимо применять методы очистки выбросов и стоков. Это может быть использование фильтров и сорбентов, обработка отходов перед их сбросом в водоемы, а также эффективное использование ресурсов и повышение энергоэффективности процессов производства.
В целом, понимание влияния металлов на окружающую среду и поиск способов его минимизации является важным шагом в направлении устойчивого развития и сохранения природы для будущих поколений.
Применение металлов в быту и промышленности

Металлы являются неотъемлемой частью нашего повседневного быта. Они применяются в различных сферах жизни и имеют множество практических применений. Один из наиболее известных и распространенных металлов - железо. Оно используется для изготовления строительных конструкций, автомобилей, бытовой техники и многого другого.
Алюминий, благодаря своей легкости и прочности, широко используется в промышленности и быту. Он является основным материалом для производства автомобилей, самолетов и упаковки различных товаров. Также алюминий применяется в строительстве для производства оконных рам, дверей и каркасов зданий.
Другим распространенным металлом, применяемым в быту и промышленности, является медь. Этот металл отличается хорошей электропроводностью, поэтому широко используется в электротехнике и строительстве. Медные провода и кабели используются для передачи электроэнергии, а также для соединения и монтажа электрических устройств.
Олово и свинец применяются в производстве аккумуляторов и батарей. Они используются как материалы для создания электродов и электролитов, что позволяет иметь надежные и долговечные источники энергии. Кроме того, свинец используется в производстве пулевых и грузовых патронов, а олово - во многих других отраслях промышленности, включая пищевую и электронную промышленность.
Металлы также применяются в машиностроении, судостроении, производстве оружия, мебели и многих других отраслях промышленности. Их особенности и свойства позволяют создавать прочные, надежные и функциональные изделия, которые используются в повседневной жизни и способствуют развитию промышленности.
В заключение, металлы играют важную роль в нашей жизни, применяясь в различных сферах быта и промышленности. Благодаря своим уникальным свойствам, они стали неотъемлемой частью современного мира и продолжают использоваться для создания различных предметов и конструкций, которые облегчают и улучшают нашу жизнь.
Реакция металлов с кислотами

Реакция металлов с кислотами — это химические процессы, при которых металлы вступают во взаимодействие с кислотами, образуя соли и выделяя газы.
Металлы, такие как цинк, железо, алюминий, магний, натрий и калий реагируют с различными кислотами, включая соляную, серную и уксусную кислоты.
В результате реакции образуется соль и выделяется водородный газ. Соль можно получить в виде раствора или осадка. Водородный газ обычно выделяется в виде пузырьков и может быть зажигаемым.
Реакция между металлом и кислотой основана на смене водородных ионов. Металл вытесняет водород из кислоты и занимает его место, образуя соль.
Реакция металлов с кислотами имеет практическое применение, так как она может использоваться для получения различных веществ и для очистки металлов от оксидов и загрязнений.
Примеры реакций металлов с кислотами:
- Цинк + серная кислота → сульфат цинка + водород
- Железо + соляная кислота → хлорид железа + водород
- Магний + уксусная кислота → ацетат магния + водород
Итак, реакция металлов с кислотами является важным процессом, который позволяет получать соли и очищать металлы, а также имеет широкое применение в химической промышленности и научных исследованиях.
Окисление металлов

Окисление металлов – это процесс, при котором металл взаимодействует с кислородом воздуха или другими веществами, что приводит к образованию окиси металла.
Одним из наиболее известных примеров окисления металлов является ржавление железа, при котором на его поверхности образуется слой ржавчины – оксида железа. Это происходит из-за реакции железа с водой и кислородом, содержащимся в воздухе.
Окисление металлов может влиять на их структурные и химические свойства. Некоторые металлы, такие как золото и платина, устойчивы к окислению и не образуют оксидные слои на поверхности. Однако большинство металлов, например, алюминий и медь, подвержены окислению и на их поверхности образуется оксидное покрытие.
Чтобы предотвратить окисление металлов, на их поверхность наносят защитные покрытия или проводят специальные химические обработки. Также применяют специальные антикоррозийные покрытия, которые предотвращают попадание кислорода и влаги к металлу.
Экспериментальные методики изучения активности металлов

Экспериментальное изучение активности металлов является важной частью химических исследований и помогает нам понять, как металлы взаимодействуют с другими веществами и средами. Существует несколько методик, которые позволяют определить активность металлов.
Одним из наиболее распространенных методов является использование водорода для изучения активности металлов. Для этого металл погружают в кислоту или раствор соли металла. Если металл является активным, то происходит реакция, в результате которой выделяется водород. По количеству выделенного водорода можно судить об активности металла.
Еще одним методом изучения активности металлов является их реакция с кислородом. Металлы могут гореть в кислороде, что свидетельствует об их активности. Некоторые металлы (например, калий и магний) горят ярким пламенем, а другие металлы (например, железо) медленно окисляются, образуя окиси металлов.
Также активность металлов можно изучать с помощью электрохимических методов. Реакция металлов с электролитами позволяет определить их окислительно-восстановительные свойства. Методы, такие как измерение потенциала, позволяют сравнить активность различных металлов и установить их положение в электрохимическом ряду.
Использование различных экспериментальных методик позволяет ученым изучить активность металлов и получить более полное представление о их свойствах. Эти методы помогают проанализировать реакции металлов и понять, как они взаимодействуют с другими веществами, что имеет широкое применение в индустрии, медицине и научных исследованиях.
Вопрос-ответ

Что такое активность металлов?
Активность металлов - это способность металла вступать в химические реакции с другими веществами. Металлы могут быть активными или пассивными в зависимости от их способности вступать во взаимодействие с окружающей средой.
Какие металлы считаются активными?
К активным металлам относятся металлы, которые легко окисляются, т.е. вступают в реакцию с кислородом. Например, натрий, калий, магний, алюминий и т.д. Эти металлы обычно имеют ярко выраженные химические свойства и активно взаимодействуют с водой и кислородом.
Какова роль активных металлов в нашей жизни?
Активные металлы играют важную роль в нашей жизни. Например, натрий и калий являются необходимыми элементами для нашего организма и участвуют в регуляции водно-солевого баланса. Магний используется в производстве сплавов и легких конструкций. Алюминий - один из самых распространенных металлов, который используется в строительстве, транспорте, а также для производства упаковочных материалов и посуды.
