Оксиды – это соединения, которые образуются при соединении металла с кислородом. В зависимости от степени окисления металла и его явной связи с кислородом, оксиды могут быть кислыми, основными или нейтральными.
Важно отметить, что только основные оксиды способны образовывать металлы ряда. Основные оксиды являются соединениями, в которых металл находится в положительном окислительном состоянии и связан с кислородом.
Металлы ряда обладают свойством образовывать стойкие соединения с кислородом и такие соединения имеют основной характер. Благодаря этому, металлы ряда активно взаимодействуют с кислородом, образуя оксиды, и именно эти оксиды являются ключевыми в процессе получения металлов через их восстановление.
Таким образом, основные оксиды обладают особым значением в химии металлов и являются необходимыми компонентами в процессе получения металлов ряда.
Роль оксидов в составе ряда металлов

Состав оксидов играет важнейшую роль в определении положения металлов в ряду химической активности. Оксиды могут быть кислотными, основными или амфотерными, в зависимости от их реакции с водой.
Только основные оксиды, такие как Na2O, K2O, CaO, растворяются в воде и образуют щелочные растворы. Они действуют как основания, принимая на себя H+ и образуя OH-. Эти оксиды образуют металлы рядов щелочных металлов и щелочноземельных металлов.
Другие металлы, такие как Fe, Cu, Zn, образуют кислые оксиды, которые не растворяются в воде и не проявляют кислотные свойства. Поэтому они не образуют щелочи, а образуют кислотные оксиды, которые растворяются в кислотах.
Если металл способен образовывать разные оксиды, его положение в ряду металлов будет определяться самым основным оксидом. Например, CuO - кислый оксид меди, но поскольку Cu2O - основный оксид, медь входит в ряд щелочноземельных металлов.
Таким образом, состав оксидов является ключевым фактором, определяющим положение металлов в ряду химической активности и их способность образовывать различные соединения.
Типы оксидов в металлах ряда
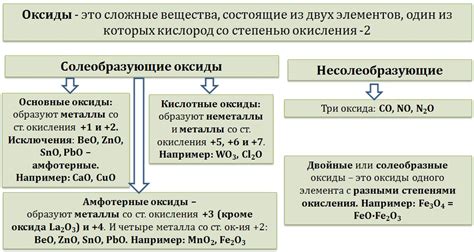
Металлы ряда могут образовывать различные типы оксидов в зависимости от их валентности и способности изменять валентность при взаимодействии с кислородом. Базовые оксиды - это основные оксиды, которые образуются металлами при взаимодействии с кислородом. Они растворяются в воде, образуя щелочные растворы. Примерами базовых оксидов являются оксиды натрия, калия и кальция.
Кислотные оксиды - это оксиды, которые образуются металлами с валентностью 2 или выше. Они проявляют кислотные свойства, растворяясь в воде и образуя кислотные растворы. Эти оксиды могут реагировать с основаниями, образуя соли. Примерами кислотных оксидов являются оксиды алюминия, железа и меди.
Амфотерные оксиды - это оксиды, которые могут проявлять как кислотные, так и щелочные свойства. Они реагируют как с кислотами, так и с основаниями, образуя соли. Примерами амфотерных оксидов являются оксиды алюминия и цинка.
Нейтральные оксиды - это оксиды, которые не образуют ни кислотные, ни щелочные растворы при растворении в воде. Они не проявляют ни кислотные, ни щелочные свойства. Примерами нейтральных оксидов являются оксиды углерода и оксиды некоторых металлов ряда переходных элементов.
В зависимости от типа образующихся оксидов, металлы ряда могут проявлять различные химические свойства и применения. Понимание типов оксидов помогает в изучении и применении металлов в различных отраслях промышленности и научных исследованиях.
Как образуются основные оксиды
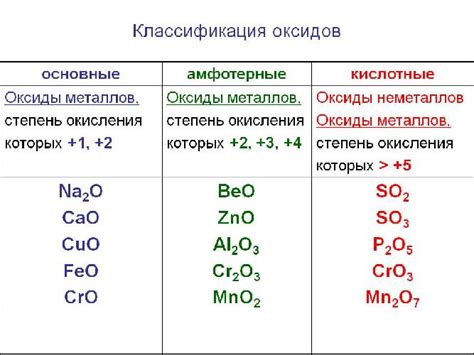
Основные оксиды – это химические соединения, образуемые металлами с кислородом. Образование основных оксидов происходит в результате реакции металла с воздухом или кислородом.
Оксид металла образуется при окислении металла, то есть его соединении с кислородом. В процессе реакции происходит передача электронов от металла к кислороду. Металл образует положительный ион, а кислород – отрицательный. Таким образом, образуется неорганическое вещество – основной оксид.
Основные оксиды обладают щелочными свойствами, то есть они способны образовывать щелочные растворы, реагируя с водой. Эта реакция называется гидратацией. При гидратации оксид металла реагирует с водой, образуя гидроксид металла и выделяя большое количество теплоты.
Многие основные оксиды широко используются в промышленности. Например, оксид кальция (известный как известь) применяется в строительстве для производства растворов и штукатурки. Оксид цинка используется в производстве косметики, лакокрасочных материалов и других товаров. Оксид железа, в свою очередь, является одним из самых распространенных оксидов и используется во многих отраслях промышленности.
Характеристика основных оксидов

Основные оксиды - это бинарные соединения, состоящие из кислорода и металла. Они образуются при реакции металла с кислородом или воздухом. Основные оксиды обычно обладают щелочными свойствами и растворяются в воде, образуя основания.
Основные оксиды широко распространены в природе, их можно найти в виде минералов или использовать в промышленности для получения металлов. Некоторые основные оксиды, такие как оксид магния и оксид алюминия, используются в производстве огнеупорных материалов и керамики.
Химические свойства основных оксидов:
- Они реагируют с водой, образуя основания - гидроксиды металлов. Например, оксид натрия реагирует с водой, образуя гидроксид натрия (щелочь).
- Они реагируют с кислотами, образуя соли и воду. Например, оксид кальция реагирует с соляной кислотой, образуя хлорид кальция и воду.
- Они обладают свойством нейтрализовать кислоты. Это связано с их щелочными свойствами.
- Они могут взаимодействовать с другими веществами, образуя сложные соединения. Например, оксид алюминия может образовывать сульфаты алюминия.
Основные оксиды имеют широкое применение в различных отраслях науки и промышленности. Они являются важными компонентами в производстве стекла, керамики и металлов. Также они играют важную роль в различных химических реакциях, таких как нейтрализация, окисление и восстановление.
Влияние основных оксидов на свойства металлов

Основные оксиды, образуемые металлами, имеют существенное влияние на их физические и химические свойства. Эти соединения могут изменить структуру металлов и их поверхность, вызывая различные эффекты.
Присутствие основных оксидов на поверхности металлов может оказывать защитное действие и увеличивать их коррозионную стойкость. Эти оксиды образуют прочные пленки, которые могут предотвращать дальнейшую окислительную реакцию с окружающей средой. Например, оксид алюминия (Al2O3) образует непроницаемую и защитную пленку на поверхности алюминия, предотвращая его окисление.
Основные оксиды также могут влиять на проводимость металлов. Некоторые из них обладают полупроводниковыми свойствами и могут используются в различных электронных устройствах. Например, оксид меди (Cu2O) может быть использован в солнечных батареях или в электронных компонентах.
Другой важной характеристикой, которая может изменяться под влиянием основных оксидов, является магнитная свойство металлов. Множество металлов становятся магнитными при взаимодействии с определенными оксидами. Например, оксид железа (Fe3O4) может превратить обычное железо в магнитный материал.
В целом, основные оксиды образуютые металлами, существенно влияют на их свойства, делая их более стойкими к окислительным процессам, изменяя проводимость электричества и даже влияя на магнитные свойства. Эти эффекты широко используются в различных отраслях, от электроники до материаловедения.
Примеры металлов, образующих только основные оксиды
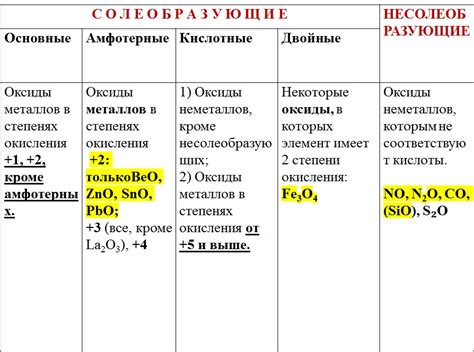
У металлов есть различные способы взаимодействия с кислородом. Одним из них является образование оксидов. Основные оксиды образуются только некоторыми металлами, которые обычно находятся в левой части периодической системы элементов.
Один из примеров металлов, образующих только основные оксиды, - это щелочные металлы, такие как натрий (Na) и калий (K). Они образуют основные оксиды, такие как Na2O и K2O. Эти оксиды растворяются в воде, образуя щелочные растворы.
Еще один пример - это металлы алкалиноземельных металлов, такие как магний (Mg) и кальций (Ca). Они образуют основные оксиды, такие как MgO и CaO. Эти оксиды также реагируют с водой, образуя щелочные растворы.
Значительное количество металлов способно образовывать как основные, так и кислотные оксиды в зависимости от условий их образования. Однако щелочные металлы и металлы алкалиноземельных металлов являются основными примерами металлов, образующих только основные оксиды.
Вопрос-ответ

Какие оксиды считаются основными?
Основными оксидами считаются оксиды металлов, которые реагируют с кислородом и образуют щелочные гидроксиды.
Почему только основные оксиды образуют металлы ряда?
Основные оксиды образуют металлы ряда потому, что они способны реагировать с водой и образовывать щелочные растворы, а щелочной раствор единственный известный способ получения металла. Другие оксиды, такие как амфотерные и кислотные, не могут образовывать металлы ряда в результате своих химических реакций.
Какие металлы образуются в результате реакции основного оксида с кислородом?
Многие металлы образуются в результате реакции основного оксида с кислородом. Например, натрий, калий, кальций и другие щелочные металлы образуются при реакции оксидов Na2O, K2O, CaO с кислородом. Кроме того, реакция оксида алюминия Al2O3 с кислородом позволяет получить алюминий. Это лишь некоторые из металлов, которые могут образовываться в результате таких реакций.
