Щелочноземельные металлы – это группа химических элементов, которые обладают сходными химическими свойствами и находятся во втором периоде таблицы Менделеева. В этой группе включены: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Решение задач по щелочноземельным металлам может быть вызывающим, однако с применением простых и эффективных стратегий можно освоить основные принципы и получить успешные результаты. Важно понимать особенности реакций и свойства каждого элемента группы, а также уметь применять правила решения задач химической кинетики, синтеза соединений и растворимости.
Ключевым фактором для эффективного решения задач по щелочноземельным металлам является обратное применение химических уравнений, чтобы найти неизвестные факторы. Необходимо уметь правильно собирать математические уравнения и решать их с учетом всех известных данных. Определение растворимости соединений и степени ионизации также может быть полезным навыком при решении задач.
Например, решение задачи по определению степени ионизации щелочноземельных металлов может потребовать применение законов химической термодинамики и расчета электрофоретической мобильности ионов. Также важно учитывать факторы, влияющие на стабильность ионов и их формирование в растворе, такие как концентрация, температура и pH.
В целом, решение задач по щелочноземельным металлам требует внимательного анализа и логического мышления. Применение основных принципов химических реакций и химической термодинамики, а также умение установить связь между различными свойствами элементов этой группы, поможет развить навыки решения задач и достичь успеха в изучении щелочноземельных металлов.
Определение щелочноземельных металлов

Щелочноземельные металлы – это группа химических элементов, включающая в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы расположены во второй группе периодической таблицы и обладают сходными физическими и химическими свойствами.
Щелочноземельные металлы обладают относительно низкой электроотрицательностью и высокой термической и электропроводностью. Они являются малоактивными химическими элементами и образуют соединения, в основном, с отрицательно заряженными радикалами. Металлы этой группы сильно реагируют с водой, образуя гидроксиды и выделяя водород.
Щелочноземельные металлы широко применяются в различных отраслях. Например, бериллий используется в производстве специальных сталей и легких сплавов, а магний находит применение в авиационной и автомобильной промышленности. Кальций используется в производстве строительных материалов и удобрений, а барий и стронций применяются в радиологии для создания рентгено-контрастных веществ.
Для определения щелочноземельных металлов в химическом анализе используют различные методы. Например, их присутствие можно выявить с помощью газовых или пламенных испытаний, а также используя методы электрохимического анализа. Также важным является использование химических реактивов и методов экстракции, которые позволяют получить чистые образцы щелочноземельных металлов для дальнейших исследований и применений.
Практическое применение щелочноземельных металлов

Щелочноземельные металлы, такие как магний, кальций, стронций и барий, широко используются в различных областях промышленности и научных исследований. Вот некоторые примеры их практического применения:
- Авиационная и автомобильная промышленность: Магний и его сплавы используются для изготовления легких и прочных компонентов авиационных и автомобильных двигателей и трансмиссий. Это позволяет снизить массу транспортных средств и повысить их эффективность.
- Строительство: Кальций используется для производства строительных материалов, таких как цемент и гипс, которые широко применяются в строительстве зданий и инфраструктуры. Стронций используется в производстве светоотражающих красителей для дорожной разметки.
- Энергетика: Барий используется в производстве электродов для дуговых ламп и рентгеновских трубок. Кальций-силикатные материалы используются в производстве изоляторов для высоковольтных электрических систем.
- Медицина: Магний и его соединения используются в медицине как антациды, слабительные средства и миорелаксанты. Кальций используется для профилактики и лечения остеопороза и как добавка в пищевые продукты. Барий используется в качестве контрастного агента при рентгенологических исследованиях.
- Производство сплавов и специальных материалов: Магний и его сплавы используются для производства легких и прочных материалов, таких как литейные сплавы и металлические компоненты для электронных устройств. Кальций и барий добавляются в различные сплавы для изменения их свойств.
Это лишь некоторые примеры практического применения щелочноземельных металлов. Благодаря своим уникальным свойствам, эти металлы находят широкое применение в различных отраслях промышленности, что делает их важными компонентами современного общества.
Основные свойства щелочноземельных металлов

Щелочноземельные металлы - это группа химических элементов, которые входят во вторую группу периодической системы. К ним относятся бериллий, магний, кальций, стронций, барий и радий. Щелочноземельные металлы обладают несколькими основными свойствами, которые делают их уникальными и полезными в различных областях науки и промышленности.
Во-первых, щелочноземельные металлы являются хорошими проводниками тепла и электричества. Это свойство делает их отличными материалами для использования в электронике, электротехнике и других областях, где требуется передача энергии.
Во-вторых, щелочноземельные металлы обладают низкой плотностью, что делает их легкими и прочными материалами. Это свойство позволяет использовать эти металлы в авиационной промышленности, а также для создания легких конструкций и сплавов.
В-третьих, щелочноземельные металлы образуют устойчивые оксиды и гидроксиды, что делает их щелочными. Их растворы являются щелочными и могут использоваться для нейтрализации кислот. Также, благодаря этим свойствам, щелочноземельные металлы используются в процессах очистки воды и производства щелочей.
И, наконец, щелочноземельные металлы обладают высокой реактивностью и способностью образовывать ионы с положительным зарядом. Именно это свойство делает их такими полезными в процессах синтеза органических соединений и производства различных химических соединений.
Таким образом, основные свойства щелочноземельных металлов - это хорошая проводимость тепла и электричества, низкая плотность, щелочность растворов и высокая реактивность. Эти свойства делают эти металлы важными и необходимыми во многих сферах науки и промышленности.
Простые способы решения задач по щелочноземельным металлам

Решение задач, связанных с щелочноземельными металлами – это задача, которую можно разбить на несколько простых шагов. Во-первых, необходимо определить, о каком металле идет речь. Далее, следует рассмотреть свойства данного металла и его химические реакции.
Одним из первых шагов может быть составление списка свойств и характеристик щелочноземельного металла. Это может включать его атомную массу, номер в периодической таблице, электронную конфигурацию и основные химические реакции.
Далее следует изучить влияние щелочноземельного металла на окружающую среду и взаимодействие с другими веществами. Например, можно рассмотреть его реакцию с водой, с кислотами или с кислородом. Эти знания позволят более точно предсказывать химические реакции и свойства щелочноземельных металлов.
Для решения задач по щелочноземельным металлам полезно знать их расположение в периодической таблице и сравнить их свойства с другими металлами. Например, можно сравнить щелочноземельные металлы с щелочными металлами и выявить общие закономерности или отличия в их химических свойствах.
Также, для решения задач можно использовать таблицу стандартных электродных потенциалов. Зная значения потенциалов редокс-реакций щелочноземельных металлов, можно предсказать направление и возможность их реакций с другими веществами.
В итоге, ключевым аспектом решения задач по щелочноземельным металлам является комплексный подход, включающий изучение свойств самого металла, его реакций с другими веществами и использование таблиц и закономерностей из химии.
Эффективные стратегии решения задач по щелочноземельным металлам

Щелочноземельные металлы включают в себя группу элементов второй группы периодической системы. Для эффективного решения задач, связанных с этой темой, необходимо усвоить следующие стратегии.
1. Знание основных свойств щелочноземельных металлов. Важно помнить, что щелочноземельные металлы обладают высокой химической активностью и хорошо растворяются в воде. Они также обладают способностью образовывать двухвалентные ионы, что следует учитывать при решении задач.
2. Правильное использование химических уравнений. При решении задач по щелочноземельным металлам необходимо уметь составлять химические уравнения для реакций, связанных с этими элементами. Важно учитывать балансировку уравнений и правильное написание реагентов и продуктов.
3. Учет реакций щелочноземельных металлов с кислотами. Щелочноземельные металлы реагируют с кислотами, образуя соответствующие соли и выделяя водород. При решении задач следует учитывать эти реакции и правильно записывать баланс ионов в реакции.
4. Знание особенностей соединений щелочноземельных металлов. Щелочноземельные металлы формируют различные соединения с другими элементами. Понимание этих особенностей, включая способность образовывать ионы разной валентности и образование осадков при реакции соединений, поможет эффективно решать задачи.
5. Практика решения задач на основе примеров. Для эффективного решения задач по щелочноземельным металлам рекомендуется много практиковаться на различных примерах. Это поможет закрепить знания и развить умение применять стратегии решения задач.
Используя эти стратегии, можно значительно повысить эффективность решения задач, связанных с щелочноземельными металлами, и достичь хороших результатов при их изучении.
Влияние щелочноземельных металлов на окружающую среду

Щелочноземельные металлы, такие как магний, кальций и стронций, имеют значительное влияние на окружающую среду. Они являются ключевыми компонентами многих геологических и биологических процессов и присутствуют в различных экосистемах. Однако, несмотря на их важность, они также могут оказывать вредное воздействие на окружающую среду.
Магний является основным компонентом многих минералов, таких как доломит и магнезит, и широко распространен в земной коре. Он играет роль в регулировании pH почвы и влияет на доступность питательных веществ для растений. Однако, избыток магния в почве может привести к ее закислению и негативно сказаться на росте и развитии растений.
Кальций является важным элементом для формирования костей и зубов у животных, и осуществляет регуляцию свертываемости крови. В природной среде кальций присутствует в виде минералов, таких как известняк и мрамор. Однако, избыток кальция в водных системах может вызывать образование отложений и приводить к загрязнению водных ресурсов.
Стронций является радиоактивным изотопом, который образуется в результате распада радия. Он широко распространен в окружающей среде, особенно в почвах и грунтах. Стронций может накапливаться в организмах живых существ и приводить к ионизирующему излучению, что может вызывать различные заболевания и повреждения ДНК.
В целом, щелочноземельные металлы играют важную роль в экологических процессах, однако необходимо контролировать их уровень на протяжении всей экосистемы. Это поможет избежать негативного влияния на окружающую среду и поддерживать ее устойчивость.
Сравнение щелочноземельных металлов с другими группами элементов
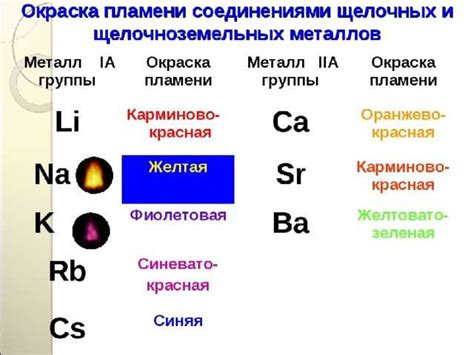
Щелочноземельные металлы представлены второй группой периодической системы элементов. В этой группе находятся металлы, которые обладают особыми свойствами и имеют сходство друг с другом. Однако, при сравнении с другими группами элементов, щелочноземельные металлы отличаются определенными характеристиками.
Электронная конфигурация: Щелочноземельные металлы имеют два электрона в своем внешнем энергетическом уровне. Это отличает их от щелочных металлов, которые имеют один электрон, и от переходных металлов, у которых наибольшее количество электронов в d-оболочке.
Реактивность: Щелочноземельные металлы являются более реактивными, чем щелочные металлы. Они способны реагировать с водой, причем реакция щелочноземельных металлов более сильная и энергичная. Это связано с их более высокой электронной аффинностью и энергией ионизации.
Свойства: Щелочноземельные металлы обладают высокой электропроводностью, низкой температурой плавления и кипения. Они легко образуют ионы положительной заряды и обладают металлическим блеском. В то же время, они более мягкие и менее плотные, чем металлы из группы переходных элементов.
Использование: Щелочноземельные металлы имеют множество практических применений. Например, магний используется для производства сплавов и легких металлических конструкций. Кальций используется в строительстве и медицине. Бериллий используется в производстве высокоточных приборов и сплавов.
В целом, щелочноземельные металлы обладают уникальными химическими и физическими свойствами, отличающимися от других групп элементов. Изучение этих металлов является важным для понимания их взаимодействия с другими веществами и для создания новых материалов и технологий.
Вопрос-ответ

Какие вещества относятся к щелочноземельным металлам?
К щелочноземельным металлам относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
В чем особенность щелочноземельных металлов?
Особенностью щелочноземельных металлов является их большая реактивность и активность в химических реакциях, а также легкость их окисления и образования ионов с положительным зарядом.
Какие стратегии решения задач по щелочноземельным металлам существуют?
Существует несколько стратегий решения задач по щелочноземельным металлам. Можно использовать принцип сохранения массы, уравнение реакции и стехиометрический расчет, а также знание свойств и химической активности этих металлов.
