Соль и металл - два вещества, которые могут проявлять химическую реакцию замещения. Реакция замещения происходит, когда один металл замещает другой из соединения соли, что приводит к образованию нового металлического соединения и освобождению соли. Такая реакция играет важную роль в химии и используется в различных областях, например, в производстве металлов и в пищевой промышленности.
Примером реакции замещения между солью и металлом является реакция между хлоридом натрия и алюминием. При взаимодействии этих веществ образуется хлорид алюминия и натрий выделается в виде свободного металла. Эта реакция можно представить следующим образом:
2 NaCl + 2 Al → 2 Na + AlCl3
Также существуют множество других примеров реакции замещения солями и металлами. Например, реакция между сульфатом меди и цинком приводит к образованию сульфата цинка и освобождению меди в виде металла:
CuSO4 + Zn → ZnSO4 + Cu
Такие реакции имеют важное практическое применение. Например, реакция замещения используется в гальванических элементах для получения электрической энергии из химических реакций. Кроме того, реакция замещения может быть использована для получения чистого металла из его соли, что важно для промышленного производства металлов.
Соль и металл: реакция замещения

Реакция замещения – это химическая реакция, при которой один металл может замещать другой из его соли. Эта реакция основана на различных электрохимических свойствах металлов.
Во время реакции замещения ион металла из соли вытесняет другой металл и формирует новое вещество. При этом первоначальный металл окисляется и переходит в ионное состояние, а вытесняющий металл восстанавливается и образует новое соединение.
Пример реакции замещения можно наблюдать при взаимодействии меди и железа. Если кусочек меди поместить в раствор железной соли, то она будет растворяться, а на ее месте окажется элементарное железо.
Подобными реакциями замещения можно описать взаимодействие различных солей и металлов. Например, медь может замещать серебро из его солей, цинк может замещать медь или железо, алюминий – цинк и т.д.
Реакция замещения широко применяется в различных областях химии и промышленности. Например, она используется для получения различных металлических сплавов, проведения электролиза, получения металлических покрытий и даже в химическом анализе.
Реакция замещения металла в соли

Реакция замещения металла в соли является одним из фундаментальных процессов в химии. Происходит она при взаимодействии металла с солью, в результате которой металл замещает другой металл в соли, образуя новый продукт. Одним из примеров такой реакции является реакция железа с соляной кислотой.
Например, при взаимодействии железа с соляной кислотой, происходит реакция замещения, в результате которой образуется соль железа и выделяется водород. Это можно представить следующим химическим уравнением:
Fe + 2HCl → FeCl2 + H2
В данном случае, железо замещает водород в соли соляной кислоты, образуя соль железа и выделяя водород.
Другим примером реакции замещения металла в соли является реакция меди с серной кислотой. В результате этой реакции образуется соль меди и выделяется диоксид серы:
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Такие реакции замещения металла в соли имеют широкое применение в различных областях химии и технологии, например, в производстве металлов, катализе, электрохимии и многих других.
Второе слово: замещения
В химии реакция замещения - это химическое превращение, при котором один элемент замещает другой в химическом соединении. Такая реакция происходит, когда металлы или не металлы стремятся занять место другого элемента в соединении, чтобы образовать более стабильную смесь. Реакция замещения может быть одним из способов получения солей.
Процесс замещения может происходить как в растворе, так и в твердом состоянии. В случае раствора вода является средой, в которой протекает реакция замещения. В твердом состоянии замещение может происходить, если элементы находятся в контакте и могут взаимодействовать химически.
Пример реакции замещения - реакция между хлором и натрием. В ходе этой реакции металлический натрий замещает хлор в химическом соединении и образуется хлорид натрия. Такая реакция может происходить при нагревании или под действием электричества.
Реакция замещения может происходить не только с натрием и хлором, но и с другими солями и металлами. Например, реакция между кислородом и железом приводит к образованию оксида железа. Или реакция между серой и цинком приводит к образованию сульфида цинка.
Примеры с другими солями и металлами:

Медь и серная кислота: Реакция между медью и серной кислотой приводит к образованию сульфата меди и выделению диоксида серы. Эта реакция часто используется для получения сульфата меди в лабораторных условиях.
Цинк и хлорид натрия: При взаимодействии цинка с хлоридом натрия образуется хлорид цинка и освобождается хлорид натрия. Эта реакция является типичной реакцией замещения и может быть использована для получения хлорида цинка.
Алюминий и соляная кислота: Встреча алюминия и соляной кислоты приводит к образованию хлорида алюминия и выделению водорода. Эта реакция демонстрирует эффективное взаимодействие между кислотой и металлом, которое может быть использовано в промышленности.
Железо и серная кислота: Взаимодействие железа с серной кислотой приводит к образованию сульфата железа и выделению водорода. Эта реакция широко применяется в лаборатории и промышленности для получения сульфата железа.
Марганец и хлорид кальция: При реакции марганца с хлоридом кальция образуется хлорид марганца и освобождается кальций. Эта реакция также является примером реакции замещения и может быть использована для получения хлорида марганца.
Примеры

Пример 1: Реакция замещения между металлом цинком (Zn) и солью меди (CuSO4) приводит к образованию цинка сульфата (ZnSO4) и осаждению меди (Cu):
- Исходное соединение: CuSO4
- Металл, замещающий медь: цинк (Zn)
- Образовавшееся соединение: ZnSO4
- Осажденный металл: медь (Cu)
Пример 2: Реакция замещения между металлом железом (Fe) и солью свинца (Pb(NO3)2) приводит к образованию железа(II) нитрата (Fe(NO3)2) и осаждению свинца (Pb):
- Исходное соединение: Pb(NO3)2
- Металл, замещающий свинец: железо (Fe)
- Образовавшееся соединение: Fe(NO3)2
- Осажденный металл: свинец (Pb)
Пример 3: Реакция замещения между металлом магнием (Mg) и солью алюминия (AlCl3) приводит к образованию магния хлорида (MgCl2) и осаждению алюминия (Al):
- Исходное соединение: AlCl3
- Металл, замещающий алюминий: магний (Mg)
- Образовавшееся соединение: MgCl2
- Осажденный металл: алюминий (Al)
Пример 4: Реакция замещения между металлом натрием (Na) и солью калия (KCl) приводит к образованию натрия хлорида (NaCl) и осаждению калия (K):
- Исходное соединение: KCl
- Металл, замещающий калий: натрий (Na)
- Образовавшееся соединение: NaCl
- Осажденный металл: калий (K)
Второе слово: солями

Соли - это химические соединения, образующиеся в результате реакции замещения металлов с кислотами. Они представляют собой кристаллические вещества, обладающие определенными физическими и химическими свойствами.
Примером реакции замещения солями может служить образование хлорида натрия (NaCl) при реакции металла натрия (Na) с кислородом (Cl). В результате этой реакции натрий замещает водород в кислоте, что приводит к образованию соли.
Соли широко используются в различных областях, например, в пищевой промышленности для улучшения вкусовых качеств продуктов, в медицине как лекарственные препараты, а также в химической промышленности для производства различных химических соединений.
Одним из примеров солей, используемых в пищевой промышленности, является хлорид натрия (поваренная соль). Она добавляется в пищевые продукты для придания им соленого вкуса и улучшения их сохранности.
Другим примером соли является сернокислый натрий (Na2SO4), который используется в производстве стекла, мыла, бумаги и других промышленных товаров.
Также соли широко применяются в медицине, например, йодид калия (KI) применяется в комплексной терапии заболеваний щитовидной железы, а ацетат кальция (CaAc2) используется для улучшения свертываемости крови.
Третье слово: металлами

Металлы - это вещества, обладающие способностью проводить тепло и электричество, имеющие блестящую поверхность и способные образовывать ионы. В реакции замещения металлы могут обмениваться ионами соляной кислоты, что приводит к образованию соли и выделению водорода.
Один из примеров реакции замещения металла с солью - реакция алюминия с раствором медного(II) хлорида. В результате этой реакции происходит замещение меди алюминием, образуется соль алюминия и медь выпадает в осадок. Схема реакции выглядит следующим образом:
2Al + 3CuCl2 -> 2AlCl3 + 3Cu
Другим примером реакции замещения металла с солью является реакция цинка с раствором серной кислоты. В этой реакции цинк замещает водород в серной кислоте, образуется соль цинка и выделяется водород. Схема реакции выглядит следующим образом:
Zn + H2SO4 -> ZnSO4 + H2
Такие реакции замещения металлами широко применяются в химической промышленности и в лабораторных условиях для синтеза различных соединений и получения ценных металлов.
Соль и металл в химических реакциях

Соль и металл могут вступать в реакции замещения, которые являются распространенными и важными химическими процессами. В этих реакциях один металл заменяет другой в солевом соединении, что приводит к образованию новых соединений и изменению свойств исходных веществ.
Реакция замещения между солью и металлом может происходить при контакте и образовании нового соединения, соли, и освобождении газа или тепла. Например, реакция между хлоридом натрия и медью приводит к образованию хлорида меди и освобождению газа хлора:
2NaCl + Cu → CuCl2 + 2Na
В другом примере, магний может заместить металл цинк в химической реакции сульфата цинка:
Mg + ZnSO4 → MgSO4 + Zn
Реакции замещения с солью и металлом могут быть полезными в различных промышленных и научных областях, таких как производство металлов, производство сольвентов и катализаторов, а также в химическом анализе и синтезе новых материалов.
Эти реакции имеют важное практическое значение и являются основой для изучения и понимания химической реактивности солей и металлов. Они позволяют установить последовательность активностей различных металлов и предсказывать результаты химических превращений.
Химических реакций замещения и примеры с другими солями и металлами

Химическая реакция замещения - это химическое превращение, при котором один элемент смещается другим элементом в химическом соединении. Данная реакция происходит между металлами и их соединениями.
Примером химической реакции замещения является реакция между цинком и кислотой. При этой реакции цинк смещает водород из кислоты, образуя соль и выделяя газ:
- Цинк + соляная кислота → хлорид цинка + водород
Также химические реакции замещения возможны между другими солями и металлами. Например, реакция между медью и серной кислотой:
- Медь + серная кислота → сульфат меди + диоксид серы
Другим примером является реакция между железом и соляной кислотой:
- Железо + соляная кислота → хлорид железа + водород
Такие химические реакции могут использоваться в промышленности, например, для получения различных металлических соединений или для очистки металлов от окиси и ржавчины. Они также применяются в лабораторных условиях для определения присутствия и реактивности различных металлов.
Реакции замещения второго слова и примеры с другими солями и металлами
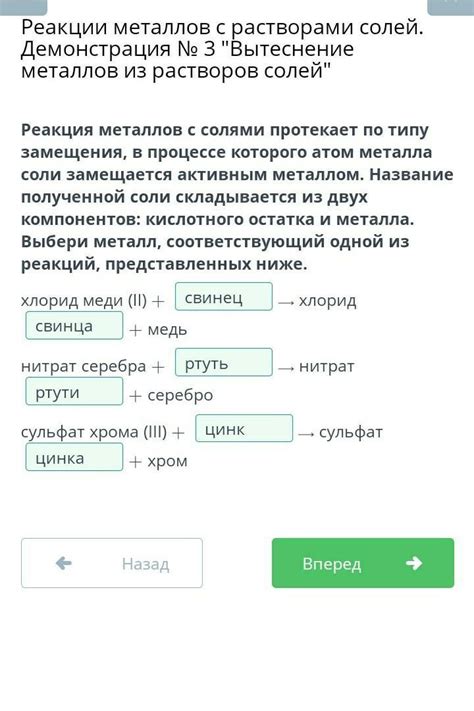
Реакции замещения являются одними из основных химических реакций, которые происходят между металлами и солями. В таких реакциях металлы замещают другие металлы в соли, образуя новые продукты. Эти реакции происходят благодаря активности металлов, которая определяется их положением в электрохимическом ряду.
Примером реакции замещения может быть реакция между цинком и медной солью. При этом цинк замещает медь в соли, образуя цинковую соль и осаждая медь. Такая реакция может быть представлена следующим уравнением:
Zn + CuSO4 → ZnSO4 + Cu
Также существуют другие примеры реакций замещения со множеством различных металлов и солей. Вот некоторые из них:
- Реакция между железом и медной солью:
- Реакция между алюминием и железной солью:
- Реакция между свинцом и серебряной солью:
Fe + CuCl2 → FeCl2 + Cu
Al + FeCl3 → AlCl3 + Fe
Pb + AgNO3 → Pb(NO3)2 + Ag
Такие реакции замещения широко используются в промышленности и лабораторных условиях для получения различных соединений и металлов.
Вопрос-ответ

Что такое реакция замещения?
Реакция замещения - это химическая реакция, при которой один элемент замещается другим элементом в химическом соединении. В данном случае мы говорим о реакции замещения металлов в солях.
Как происходит реакция замещения металлов в солях?
Реакция замещения металлов в солях происходит путем образования нового соединения, когда более реактивный металл вытесняет менее реактивный металл из его соли.
Какие примеры реакции замещения металлов в солях можно привести?
Примеры реакции замещения металлов в солях включают реакцию замещения меди из раствора соли меди цинком, реакцию замещения железа из раствора соли железа алюминием и реакцию замещения меди из раствора соли меди железом.
Какой металл может заместить другой металл в соли?
Более реактивный металл может заместить менее реактивный металл в его соли.
Для чего полезна реакция замещения металлов в солях?
Реакция замещения металлов в солях полезна, потому что она позволяет изучать относительные активности металлов и исследовать их реакционную способность.
