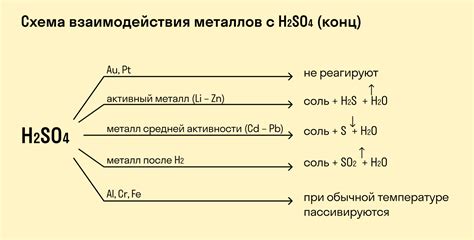
Хлор – это химический элемент широкого применения, который обладает высокой реактивностью и активностью. Металлы, в свою очередь, также обладают характеристиками, которые делают их подходящими для реакции с хлором. Поэтому взаимодействие хлора с металлами порождает реакции, приводящие к образованию различных соединений.
Когда хлор соединяется с металлом, образуется хлорид – соединение, состоящее из хлора и металла. Такие реакции обычно иллюстрируются уравнениями реакции, которые показывают, как именно происходит взаимодействие.
Примером такого уравнения может служить реакция хлора с натрием, в результате которой образуется хлорид натрия:
2Na + Cl2 → 2NaCl
В данном уравнении две молекулы натрия реагируют с одной молекулой хлора, образуя две молекулы хлорида натрия.
Уравнения реакций хлора с другими металлами могут выглядеть по-разному, в зависимости от характеристик каждого металла и условий реакции. Взаимодействие хлора с металлами может привести к образованию различных соединений и проявлению различных физических и химических свойств.
Химия: реакция хлора с металлами
Хлор – химический элемент, который встречается в природе в виде солей и используется во многих отраслях промышленности. Один из важнейших процессов, связанных с хлором, это его реакция с металлами.
Хлор обладает высокой активностью и способен образовывать соединения с различными металлами. При воздействии хлора на металлы происходит химическая реакция, в результате которой образуются соответствующие хлориды.
Например, реакция хлора с натрием приводит к образованию натриевого хлорида (NaCl). При этом хлор реагирует с натрием, отбирая у него один электрон и образуя ион хлорида Cl-. Это обусловлено высоким окислительным потенциалом хлора, который способствует его реакции с металлами.
Подобные реакции можно наблюдать и с другими металлами, например, с магнием, алюминием, цинком, железом и др. Каждый металл образует свой хлорид, например, магниевый хлорид (MgCl2), алюминиевый хлорид (AlCl3), цинковый хлорид (ZnCl2) и т.д.
Реакция хлора с металлами может проходить по нескольким механизмам, включая обменные реакции и окислительно-восстановительные процессы. Каждая такая реакция сопровождается освобождением энергии и может протекать с выделением тепла и света.
Реакция хлора с щелочными металлами
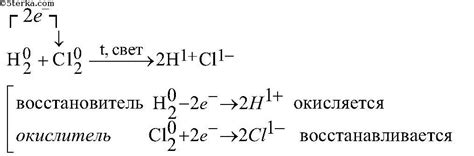
Хлор (Cl2) является химическим элементом из группы галогенов и обладает высокой активностью. Щелочные металлы, такие как натрий (Na), калий (K) и литий (Li), также являются очень реакционными и образуют сильно основные оксиды.
Взаимодействие хлора с щелочными металлами приводит к образованию солей, которые являются ионами металла и хлорида. Например, реакция хлора с натрием приводит к образованию хлорида натрия (NaCl):
2Na + Cl2 → 2NaCl
При этой реакции натрий окисляется, а хлор восстанавливается. Реакция происходит с выделением большого количества тепла и света, что свидетельствует о ее экзотермическом характере.
Аналогичные реакции происходят и с другими щелочными металлами, например:
- 2K + Cl2 → 2KCl
- 2Li + Cl2 → 2LiCl
Образование солей при реакции хлора с щелочными металлами имеет множество практических применений. Например, хлорид натрия используется в пищевой промышленности как пищевая добавка, а хлорид калия используется в медицине в качестве средства для замещения калия в организме.
Таким образом, реакция хлора с щелочными металлами является важным процессом в химии и имеет большое применение в промышленности и медицине.
Реакция хлора с щелочноземельными металлами
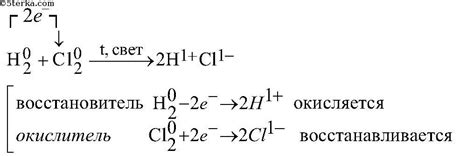
Хлор – это весьма активный элемент, который образует многочисленные соединения с различными металлами. Одна из таких реакций – взаимодействие хлора с щелочноземельными металлами. Щелочноземельные металлы включают в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Образование соединений между хлором и щелочноземельными металлами может происходить по разным сценариям, в зависимости от условий реакции. В одном из вариантов образуется хлорид металла, например, хлорид магния (MgCl2) или хлорид кальция (CaCl2), который обычно является белым кристаллическим веществом.
В другом варианте хлор может вступать в реакцию с щелочноземельным металлом, образуя металлический хлорид, к примеру, магниевый хлорид (MgCl2) или кальциевый хлорид (CaCl2). Эти вещества обладают высокой термостабильностью и применяются в различных областях промышленности, медицины и науки.
Важно отметить, что реакция хлора с щелочноземельными металлами может быть сопровождена образованием солей с различными кислотами. Например, при реакции хлора с кальцием может образоваться кальциевый хлорид (CaCl2), а также кислота хлористоводородная (HCl), которая может быть получена в ударении с водой.
Таким образом, реакция хлора с щелочноземельными металлами является важным процессом в химии и имеет широкий спектр применений в различных областях. Уравнения реакций позволяют охарактеризовать взаимодействие хлора с каждым из щелочноземельных металлов и понять особенности образующихся соединений.
Вопрос-ответ

Что происходит при взаимодействии хлора с металлами?
При взаимодействии хлора с металлами образуются соли металлического хлорида, при этом металлический ион замещает один или несколько атомов водорода в молекуле хлора.
Можно ли использовать хлор для очистки металлических поверхностей?
Да, хлор можно использовать для очистки металлических поверхностей. Хлор является сильным окислителем и может окислять органические загрязнения на поверхности металла, а также растворять ржавчину и другие органические соединения. Однако, необходимо использовать хлор с осторожностью, так как он является токсичным веществом и может быть опасен для здоровья.
