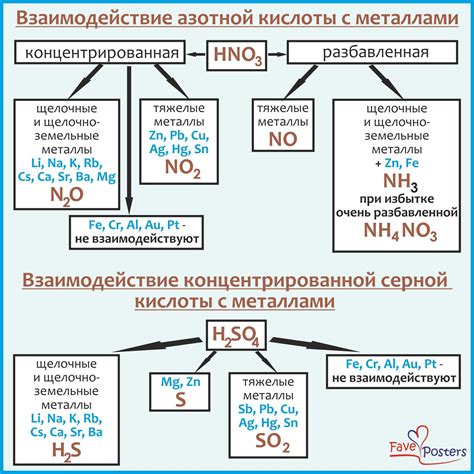
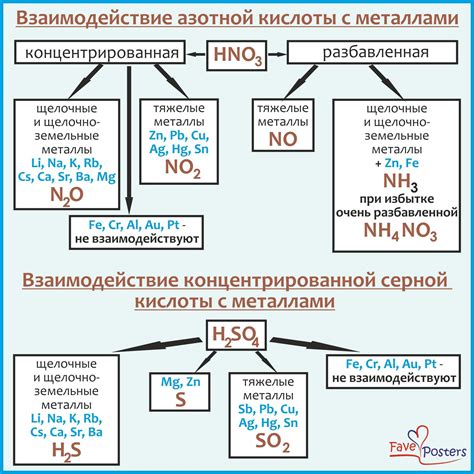
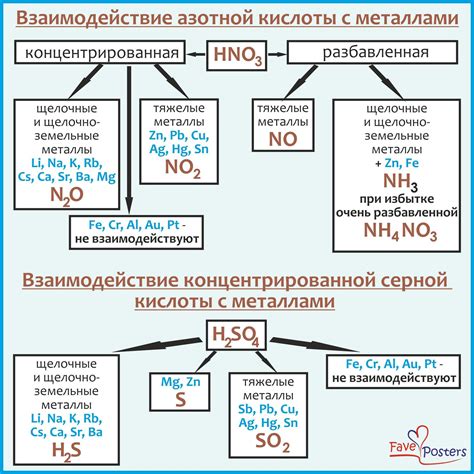
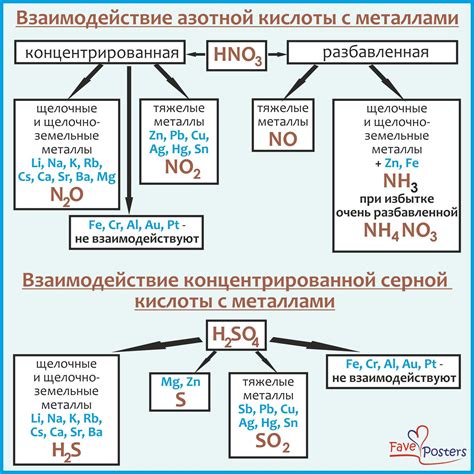
Серная кислота является одной из самых распространенных и важных химических соединений. Взаимодействие серной кислоты с металлами после водорода представляет собой процесс, при котором серная кислота взаимодействует с металлами, образуя соли и выделяя водород. Этот процесс имеет важные химические свойства и применение в различных областях промышленности и науки.
Взаимодействие серной кислоты с металлами после водорода основано на активности металла и его способности давать электроны. Как правило, только активные металлы, такие как цезий, калий и натрий, могут реагировать с концентрированной серной кислотой, образуя соли и выделяя водород. Однако, более реактивные металлы, такие как железо и алюминий, могут реагировать с разведенной серной кислотой.
Взаимодействие серной кислоты с металлами после водорода имеет большое практическое применение. Соль серной кислоты, полученная в результате реакции с металлом, называется сульфатом. Сульфаты используются в различных отраслях промышленности, таких как производство удобрений, стекла, бумаги и текстиля. Кроме того, серная кислота и сульфаты имеют широкое применение в лабораторных условиях, а также в производстве батареек и очистке сточных вод.
Таким образом, взаимодействие серной кислоты с металлами после водорода является важным процессом с большим потенциалом в различных отраслях промышленности и науки. Изучение химических свойств этого процесса позволяет разрабатывать новые методы синтеза, а также оптимизировать существующие технологии для улучшения эффективности и экологической безопасности процессов производства.
Серная кислота: основные свойства и состав

Серная кислота (H2SO4) - одно из наиболее распространенных химических соединений. Она представляет собой бесцветную или слегка желтоватую жидкость с характерным запахом. Серная кислота является сильным дипротическим кислотным соединением, что означает, что она может отдать два протона.
Состав серной кислоты включает атом серы, два атома водорода и четыре атома кислорода. Она является одним из основных продуктов сгорания серы и многих серосодержащих веществ. Серная кислота образуется при контакте серы с кислородом и медленном окислении сернистого газа, SO2.
Серная кислота обладает рядом уникальных химических свойств:
- Она является сильной кислотой и может взаимодействовать с множеством веществ, образуя соли или эстеры.
- Серная кислота обладает окислительными свойствами и может взаимодействовать с некоторыми металлами, выделяя при этом сернистый газ и образуя соли серы.
- Она способна протекать экзотермические реакции, освобождая большое количество энергии.
Использование серной кислоты находит широкое применение в различных отраслях, включая производство удобрений, пластмасс, текстиля, лекарственных препаратов и многих других. Она также используется для очистки воды, синтеза органических соединений и в процессах гальванического покрытия. Благодаря своим уникальным свойствам и широкому спектру применения, серная кислота остается одним из наиболее важных химических веществ в современной промышленности.
Возможности взаимодействия серной кислоты с металлами:
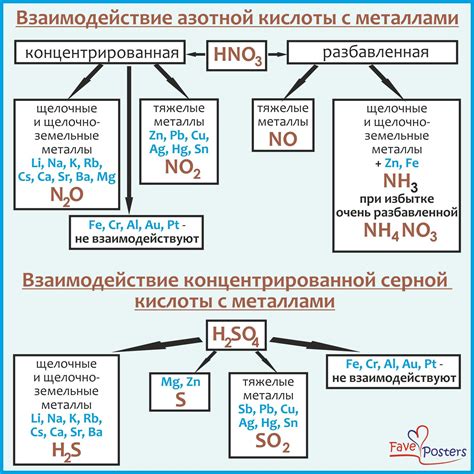
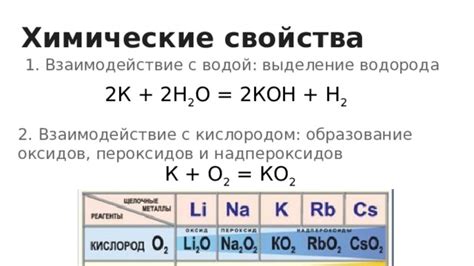
Серная кислота является сильным окислителем и проявляет активность при взаимодействии с многими металлами. Она способна реагировать с различными металлами, включая железо, алюминий, цинк, медь, свинец, никель, хром и др.
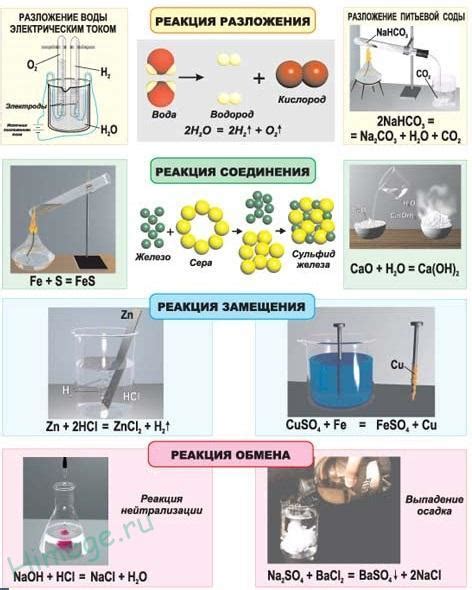
При взаимодействии серной кислоты с металлами образуется соль серной кислоты и выделяется водород. Такая реакция называется реакцией с образованием соли и выделением водорода или реакцией разложения.
Взаимодействие серной кислоты с металлами имеет важное практическое применение. Образующиеся соли серной кислоты часто используются в химической промышленности, фармацевтике, а также в процессе производства удобрений. Кроме того, водород, выделяющийся при реакции, может быть использован как источник энергии или в качестве среды для реакций в других химических процессах.
Важно отметить, что при взаимодействии серной кислоты с некоторыми металлами может возникать не только соль серной кислоты, но и соответствующее металлосульфатное соединение. Такие реакции имеют свои особенности и могут применяться для получения определенных продуктов в химической промышленности.
Последствия реакции серной кислоты с металлами после водорода
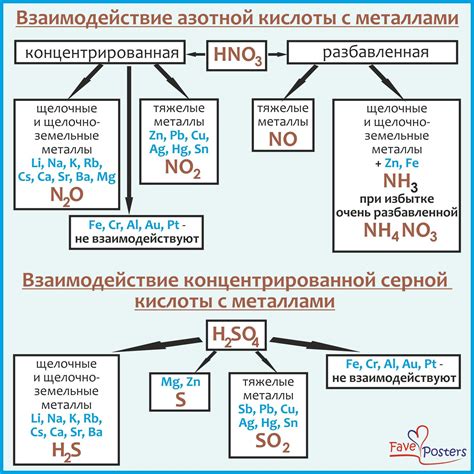
Реакция серной кислоты с металлами после водорода может иметь опасные последствия, особенно при неправильном или неконтролируемом протекании. При контакте серной кислоты с металлами может происходить выделение взрывоопасного газа – сероводорода (H2S). Это газ имеет зловонный запах, раздражает органы дыхания и может вызвать отравление.
Взаимодействие серной кислоты с металлами после водорода может вызывать также коррозию материалов. Соль серной кислоты, образовавшаяся в результате реакции, разрушает поверхность металла, ведя к его разрушению и потере свойств. Коррозия может происходить как на поверхности металла, так и внутри его структуры, что приводит к снижению прочности и надежности конструкций.
Реакция серной кислоты с металлами после водорода также может приводить к образованию взрывоопасных смесей. Серная кислота действует на металлы, выделяясь из раствора, и может образовывать пары, которые в сочетании с кислородом воздуха становятся взрывоопасными. При неправильной обработке или накоплении таких пар может возникнуть взрыв или пожар.
Поэтому при работе с серной кислотой и металлами необходимо соблюдать правила безопасности. Рекомендуется использовать специальное оборудование и средства защиты, проводить реакцию в хорошо вентилируемом помещении, предотвращать возможность образования взрывоопасных смесей. Также следует учитывать химические свойства конкретных металлов и их реактивность с серной кислотой, чтобы избежать непредвиденных последствий.
Применение реакции серной кислоты с металлами в промышленности

Реакция серной кислоты с металлами имеет широкое применение в промышленности благодаря своим уникальным химическим свойствам.
Кислотное обезжиривание металлической поверхности: Процесс обезжиривания металлических поверхностей перед нанесением покрытий представляет собой одну из важных стадий производства. Серная кислота используется для удаления жиров и примесей с поверхности металла, обеспечивая эффективное сцепление между покрытием и металлической основой.
Процесс гальванического осаждения: Реакция серной кислоты с металлами может служить одной из стадий процесса гальванического осаждения. Серная кислота используется как электролит в электрохимических процессах, обеспечивая надежное осаждение металла на поверхности изделия.
Процесс травления металлов: Травление металлов, таких как алюминий и медь, осуществляется с помощью серной кислоты. Реакция между серной кислотой и металлом позволяет удалить припуски, оксиды и другие загрязнения с поверхности, обеспечивая равномерное и эстетически привлекательное покрытие.
Производство удобрений: Одним из основных применений серной кислоты является производство удобрений. Серная кислота используется для получения сульфата аммония, который является основным компонентом многих удобрений.
Процесс очистки и обеззараживания воды: Серная кислота применяется для очистки и обеззараживания воды. Реакция серной кислоты с загрязнениями в воде позволяет устранить бактерии, вирусы и другие микроорганизмы, обеспечивая безопасность питьевой воды.
Таким образом, реакция серной кислоты с металлами имеет множество важных применений в промышленности, от кислотного обезжиривания поверхностей до производства удобрений и обеззараживания воды.
Химические свойства серной кислоты в процессе взаимодействия с металлами
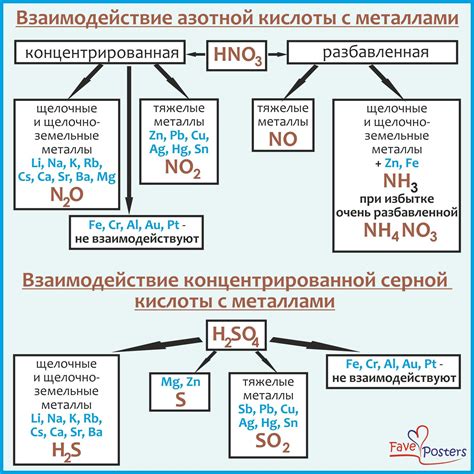
Серная кислота (H2SO4) обладает высокой активностью и способна взаимодействовать с большим числом металлов. Это связано с ее кислотными свойствами и способностью образовывать соли, называемые сульфатами.
Процесс взаимодействия металлов с серной кислотой происходит с образованием соответствующих сульфатов и выделением водорода:
- Металл реагирует с серной кислотой, образуя сульфат металла и молекулы водорода газа;
- Выделение водорода при этой реакции обусловлено окислительными свойствами серной кислоты;
- Скорость реакции и ее интенсивность зависят от активности металла и концентрации серной кислоты.
Примечательно, что некоторые металлы могут восстанавливать серную кислоту:
- Например, железо в реакции с серной кислотой может образовывать сульфат железа (II) и сернистый ангидрид;
- Это свойство определяет широкое применение серной кислоты в процессе восстановления различных веществ и реакций;
- Кроме того, серная кислота может являться катализатором в некоторых важных процессах взаимодействия металлов, например, в реакции окисления металлов.
Таким образом, свойства серной кислоты взаимодействовать с металлами определяют ее роль в различных химических процессах, а также обеспечивают ее применение в различных отраслях промышленности и научных исследований.
Важность контроля и безопасности при взаимодействии серной кислоты с металлами
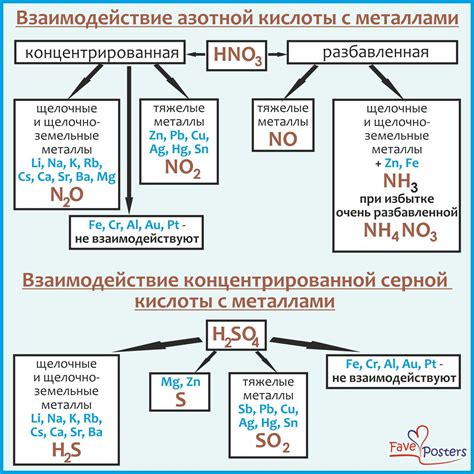
Взаимодействие серной кислоты с металлами может быть опасным и требует строгого контроля и соблюдения мер безопасности. Эта реакция сопровождается выделением водорода, что может привести к образованию взрывоопасной смеси воздуха и паров кислоты.
При работе с серной кислотой необходимо использовать соответствующие меры защиты, например, специальную защитную одежду, респираторы и очки, чтобы предотвратить попадание кислоты на кожу, в глаза или органы дыхания.
Контроль за взаимодействием серной кислоты с металлами требует также точного измерения и регулирования концентрации кислоты, температуры и смешивания. Контролировать показатели можно с помощью химических анализаторов и применения других приборов и инструментов.
Безопасность при взаимодействии серной кислоты с металлами особенно важна в промышленных процессах, где эта реакция может применяться для очистки поверхностей металла или для производства серных соединений. Важно соблюдать все рекомендации и правила безопасности, чтобы предотвратить возможные аварии и несчастные случаи.
Вопрос-ответ

Каким образом происходит взаимодействие серной кислоты с металлами после водорода?
После водорода серная кислота может взаимодействовать с металлами, образуя соли серных кислот. При этом происходит окисление металла, а серная кислота восстанавливается.
Какие химические свойства обладает серная кислота при взаимодействии с металлами после водорода?
Серная кислота является сильным окислителем при взаимодействии с металлами после водорода. Она способна окислять металлы до положительного заряда, при этом сама восстанавливается.
Какие применения имеет взаимодействие серной кислоты с металлами после водорода?
Взаимодействие серной кислоты с металлами после водорода имеет широкое применение. Например, серная кислота используется в электролитических процессах для получения металлов или при производстве батарей. Она также может использоваться в качестве катализатора в реакциях окисления металлов.
Какие особенности имеют химические свойства серной кислоты при взаимодействии с металлами после водорода?
При взаимодействии серной кислоты с металлами после водорода происходит активное окисление металла. Серная кислота может образовывать с металлами соли серных кислот, при этом она сама восстанавливается. Это свойство является основой многих промышленных процессов, использующих серную кислоту.