Реакция металла с оксидом меди является одной из фундаментальных химических реакций, которая широко исследуется и применяется в различных отраслях науки и техники. Оксид меди (CuO) - это неорганическое соединение, состоящее из атомов меди и кислорода, которое обладает свойствами, позволяющими проявить активность в реакции с металлами.
Принцип реакции металла с оксидом меди основан на термическом разложении оксида меди и образовании металла и кислорода. При нагревании оксида меди в присутствии металла происходит постепенное поглощение кислорода металлом и выделение меди в виде металлического элемента. Это позволяет образовать соединение металла с медью, которое обладает определенными свойствами и может быть использовано в различных целях.
Характеристики реакции металла с оксидом меди включают возможность использования различных металлов в качестве реакционного агента, образование стабильного соединения металла с медью и присутствие выделения кислорода в результате реакции. Данные свойства позволяют использовать данную реакцию в различных областях, включая производство материалов, электрохимию, катализ и др.
Применение реакции металла с оксидом меди находит свое применение в различных отраслях и научных исследованиях. Например, данная реакция может быть использована для получения меди из ее оксидов, что важно в производстве металлических изделий и оборудования. Также реакция металла с оксидом меди может быть использована в электрохимических процессах, катализаторах и других химических реакциях, требующих наличия меди в активной форме.
Принципы реакции
Реакция металла с оксидом меди основана на принципе обмена ионами между реагентами. В данной реакции металл вытесняет медь из оксида меди, переходя сам в ионное состояние, а медь, в свою очередь, освобождается и образует металлическое осаждение.
Оксид меди, как вещество, является нестабильным и легко разлагается при действии высоких температур на металл и кислород. Поэтому, при взаимодействии с металлом, медь освобождается из оксида и образует новое вещество с металлом, называемое соединением металла с медью.
Реакция металла с оксидом меди является редокс-реакцией, в которой происходит одновременное окисление металла и восстановление меди. Металл, выступая в качестве восстановителя, отдает свои электроны меди, которая, в свою очередь, принимает электроны от металла, проявляя свой окислительный характер.
Принципы реакции металла с оксидом меди легко представить в виде химического уравнения, в котором указаны общие формулы и состояния реагентов и продуктов:
- Металл (М) + Оксид меди (CuO) → Металлическое соединение (CuM) + Избыточный кислород (O2)
- Металл (М) + Избыточный кислород (O2) → Металлическое соединение (MO)
Реакция металла с оксидом меди обладает важным свойством - способностью протекать практически при любом давлении и температуре, однако скорость реакции может быть увеличена при повышении температуры или использовании катализатора, такого как платина или никель.
Характеристики реакции

Реакция металла с оксидом меди является типичным примером реакции обмена, при которой два вещества обмениваются компонентами и образуются новые соединения. В этом случае металл обменивается с кислородом из оксида меди, превращая его в металлический оксид, а сам металл вступает в реакцию с оксидом, образуя медь и выделяя кислород.
Реакция металла с оксидом меди характеризуется высокой экзотермической реакцией, что означает, что она сопровождается выделением тепла. Это связано с тем, что образование новых связей в реакционной смеси является энергетически более выгодным процессом, чем разрыв связей в исходных веществах.
Применение реакции металла с оксидом меди включает несколько областей. В области производства меди эта реакция используется для восстановления оксидных руд меди. В химической промышленности она применяется для получения меди и медных солей. Кроме того, реакция металла с оксидом меди широко используется в учебных целях для демонстрации принципов реакции обмена и в качестве одного из примеров реакции металла с несамостоятельным оксидом.
Применение реакции

Реакция металла с оксидом меди находит широкое применение в различных областях. Одним из основных применений этой реакции является получение чистого металла из его оксида. Путем прямой реакции металла с оксидом меди можно получить медь, которая имеет широкое применение в промышленности и технологии.
Кроме того, реакция металла с оксидом меди может использоваться для получения различных сплавов с заданными свойствами. Например, сплавы меди с алюминием, которые получаются в результате этой реакции, обладают высокой прочностью и теплопроводностью, и широко используются в электротехнике и машиностроении.
Также, реакция металла с оксидом меди может быть использована в аналитической химии для определения содержания металла в исследуемом образце. Путем контакта металла с оксидом меди и анализа полученного продукта реакции можно определить, сколько металла присутствует в образце и его концентрацию.
Более того, реакция металла с оксидом меди имеет важное практическое применение в процессе пайки и припоя. Медь, получаемая в результате этой реакции, может служить в качестве основного материала для припоя, который является неотъемлемой частью припойных соединений и широко используется при пайке электронных компонентов и металлических конструкций.
Влияние металла на характеристики реакции
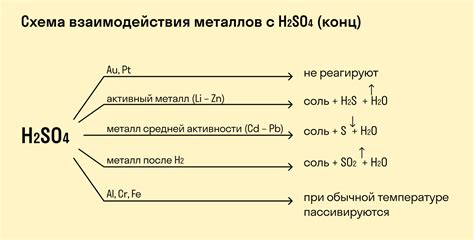
Выбор металла при проведении реакции металла с оксидом меди существенно влияет на характеристики данной реакции и ее применение.
Первым фактором, который следует учитывать при выборе металла, является его активность. Более активные металлы, такие как алюминий или цинк, будут обладать большей реакционной способностью и энергией, что приведет к быстрому и интенсивному протеканию реакции с оксидом меди. Более пассивные металлы, например, медь или железо, могут проявлять меньшую реакционную активность и более медленно взаимодействовать с оксидом меди.
Вторым фактором, который следует учитывать, является степень образования меди в результате реакции. Некоторые металлы, такие как цинк или алюминий, реагируют с оксидом меди до конца, образуя медную плоскость и выделяя большое количество тепла. Другие металлы, например, железо или никель, могут образовывать оксиды металла и осаждать небольшое количество меди при реакции.
Третьим фактором, который следует учитывать, является селективность металла при взаимодействии с оксидом меди. Некоторые металлы, такие как цинк или алюминий, обладают способностью реагировать только с оксидом меди, оставляя другие оксиды металла нетронутыми. Другие металлы, например, железо или никель, могут реагировать не только с оксидом меди, но и с другими оксидами, что может привести к образованию множества осадков и изменению химической структуры реакционной смеси.
Таким образом, выбор металла при проведении реакции металла с оксидом меди играет важную роль в определении характеристик реакции, таких как скорость протекания, количество осадка и селективность реакции. Эти факторы могут быть использованы в различных практических применениях, таких как производство меди и ее соединений, катализаторы и энергетические устройства.
Потенциал реакции в различных условиях

Потенциал реакции между металлом и оксидом меди зависит от ряда факторов, включая состояние исходных веществ, температуру и концентрацию реагентов. В различных условиях можно наблюдать различные результаты этой реакции.
Одним из факторов, влияющих на потенциал реакции, является состояние оксида меди. Если оксид меди находится в твердом состоянии, то реакция может протекать медленнее и требует высоких температур для активации. Однако, если оксид меди представлен в жидком или газообразном состоянии, реакция может протекать более быстро и эффективно.
Также температура играет важную роль в потенциале реакции. При повышении температуры, скорость реакции обычно увеличивается. Высокие температуры способствуют более активному взаимодействию металла и оксида меди, что приводит к более полному протеканию реакции.
Концентрация реагентов также может влиять на потенциал реакции. Повышение концентрации металла или оксида меди может способствовать увеличению скорости реакции. Более высокая концентрация реагентов обеспечивает большую вероятность их столкновения, что способствует более интенсивному протеканию реакции.
В итоге, потенциал реакции металла с оксидом меди в различных условиях может быть разным, и учитывать все факторы, влияющие на эту реакцию, является важным для оптимизации ее протекания и получения желаемых результатов.
Вопрос-ответ

Как происходит реакция металла с оксидом меди?
Реакция металла с оксидом меди происходит с выделением меди и образованием металлического оксида. Металл замещает медь в оксиде, то есть медь переходит в ионное состояние, а металл вступает в реакцию с кислородом, образуя оксид. Например, реакцией меди(II) оксида (CuO) с цинком (Zn) образуется цинковый оксид (ZnO) и медь (Cu): Zn + CuO → ZnO + Cu.
Какие основные характеристики реакции металла с оксидом меди?
Основные характеристики реакции металла с оксидом меди включают изменение оксидационных степеней меди и металла, образование металлического оксида и выделение меди в металлическом состоянии. Реакция проходит при высокой температуре, обычно с применением обогревающего элемента. В результате реакции получается металлический оксид, который может использоваться в различных областях, например, в производстве электроники, керамики и газовых сенсоров.
