Кислоты – это химические соединения, которые могут образовывать положительные ионы в растворе. Оксиды металлов, с другой стороны, являются химическими соединениями, состоящими из металлических и неметаллических элементов, где оксидный ион выступает в качестве аниона. Вопрос о реакции кислоты с оксидом металла интересует многих, поскольку эта реакция может иметь различные последствия и эффекты.
Реакция между кислотой и оксидом металла – это, вероятно, одна из наиболее изученных химических реакций. В большинстве случаев, когда кислота вступает в контакт с оксидом металла, происходит химическая реакция, и оба соединения изменяют свои свойства.
Примером такой реакции может служить реакция между соляной кислотой и оксидом цинка. В результате реакции образуется хлорид цинка и вода. Другой пример – реакция между серной кислотой и оксидом меди, в результате которой образуется сульфат меди и вода.
Интересно отметить, что не все кислоты реагируют с оксидами металлов. Некоторые кислоты, такие как азотная кислота или серная кислота, могут реагировать только с определенными оксидами металлов. Это связано с активностью кислоты и реакционной способностью оксида металла.
Взаимодействие кислот с оксидами металлов: возможны ли реакции?

Кислоты – это соединения, способные отдавать протоны и образовывать ионы водорода (H+), а оксиды металлов – это неорганические соединения, содержащие кислород и металлический элемент. Вопрос о возможности реакции между кислотами и оксидами металлов имеет ответ, зависящий от их свойств и структуры.
В ряде случаев кислоты могут реагировать с оксидами металлов, образуя соли и воду. Это происходит при образовании нейтральной среды, когда ионы водорода и ионы оксида металла соединяются, образуя молекулы воды.
Однако не все кислоты способны реагировать с оксидами металлов. Реактивность кислоты зависит от ее силы, а также от структуры и свойств оксида металла. Например, сильные кислоты, такие как серная или соляная кислота, могут реагировать со многими оксидами металлов, образуя соли и воду.
Слабые кислоты, вроде уксусной или угольной кислоты, могут реагировать только с определенными оксидами металлов, например, оксидом цинка или оксидом меди. Реакция в этом случае может быть менее интенсивной и происходить в медленном темпе.
Выводы можно сделать следующие: реакции между кислотами и оксидами металлов возможны, но их возможность и интенсивность зависят от свойств и структуры соединений. Для реакции необходимо наличие свободных протонов в кислоте и способность оксида металла принять эти протоны. Однако, нельзя говорить о всеобщем взаимодействии кислот с оксидами металлов, так как это зависит от конкретных соединений и условий реакции.
Реакция между оксидами металлов и кислотами: базовые принципы

Реакция между оксидами металлов и кислотами – это химический процесс, при котором оксид металла взаимодействует с кислотным раствором, образуя соль и воду. В ходе такой реакции происходит обмен ионами между оксидом металла и ионами водорода в кислоте.
Внешний вид оксида металла и реакция, которая происходит между ним и кислотами, зависит от множества факторов, включая свойства металла и тип кислоты. Кислоты могут быть сильными или слабыми, а оксид металла может быть щелочным, амфотерным или кислым.
Если оксид металла является щелочным или амфотерным, то реакция с кислотами протекает более интенсивно, поскольку ионизация оксида металла происходит более легко. В результате такой реакции образуется соль и вода. Примером такой реакции является реакция щелочного оксида натрия (Na2O) с соляной кислотой (HCl).
Если оксид металла является кислым, то реакция с кислотами протекает медленнее и требует дополнительного нагревания или добавления катализатора для активизации процесса. В результате такой реакции образуется соль и вода. Примером такой реакции является реакция кислого оксида серы (SO2) с серной кислотой (H2SO4).
В целом, взаимодействие оксидов металлов с кислотами является одним из основных способов образования солей, который широко применяется в химической промышленности и лабораторных условиях для получения различных продуктов.
Какие кислоты могут реагировать с оксидами металлов?
Оксиды металлов являются химическими соединениями, состоящими из одного или нескольких металлических элементов и кислорода. Они могут быть кислотными или основными в зависимости от своей реакционной способности. Кислотные оксиды реагируют с водой, образуя кислоты. В данном контексте будем рассматривать реакцию кислотных оксидов с кислотами.
Реакция между кислотами и оксидами металлов представляет собой образование соли и воды. Какой тип оксида металла будет реагировать с конкретной кислотой зависит от их химической природы и взаимной реакционной способности.
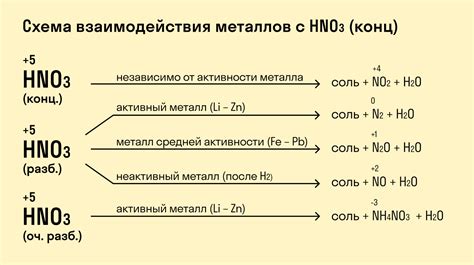
Например, с большинством кислот могут реагировать оксиды неметаллов, такие как оксиды серы (SO2 и SO3), оксиды азота (NO и NO2) и оксиды серы (SO2 и SO3). Оксиды металлов, такие как оксиды алюминия (Al2O3), железа (Fe2O3) и марганца (MnO), обычно реагируют с сильными кислотами, такими как серная (H2SO4), соляная (HCl) и азотная (HNO3) кислоты.
Однако, не все оксиды металлов реагируют с кислотами. Например, оксид меди (CuO), оксид цинка (ZnO) и оксид свинца (PbO) не сильно реакционны с кислотами. Поэтому, для того чтобы узнать, реагируют ли конкретные оксиды металлов с кислотами, нужно обратиться к химическим таблицам и справочникам.
Реакция гидроксидов металлов с кислотами: возможны ли аналогичные процессы?

Гидроксиды металлов представляют собой соединения, которые образуются при реакции металлов с гидроксидом. Гидроксиды металлов являются основаниями и, в реакции с кислотами, они могут образовывать соль и воду.
В отличие от оксидов металлов, реакция гидроксидов металлов с кислотами проходит более интенсивно и обычно сопровождается выделением тепла. Для проведения реакции гидроксидов металлов с кислотами необходимо добавить гидроксид металла в раствор кислоты и тщательно перемешать.
Подобная реакция приводит к образованию соли и воды. Вода, образующаяся в результате реакции, обычно остается в растворе, а соль может выпадать на дно или образовывать осадок. В зависимости от видов металлов и кислот, участвующих в реакции, образующиеся соли могут иметь различные свойства и структуру.
Таким образом, реакция гидроксидов металлов с кислотами является возможным процессом. Она происходит с образованием соли и воды и может быть использована для получения различных соединений металлов.
Экспериментальные данные: какие реакции кислот с оксидами металлов удалось наблюдать?

Исследования позволили выявить несколько реакций, которые происходят между кислотами и оксидами металлов. Во время экспериментов были получены следующие результаты:
- Взаимодействие сульфатной кислоты с оксидом железа(II). В результате реакции образуется сульфат железа(II) и вода.
- Взаимодействие соляной кислоты с оксидом натрия. При этой реакции образуется хлорид натрия и вода.
- Взаимодействие азотной кислоты с оксидом меди(II). Результатом реакции является нитрат меди(II) и вода.
- Взаимодействие серной кислоты с оксидом кальция. При этой реакции образуется сульфат кальция и вода.
В экспериментах было обнаружено, что реакции между кислотами и оксидами металлов протекают с образованием новых веществ и сопровождаются выделением энергии в виде тепла. Результаты этих реакций подтверждают законы химии и являются важным фундаментом для понимания свойств различных соединений и их применения в различных областях науки и промышленности.
Практическое применение реакций кислот с оксидами металлов

Реакции кислот с оксидами металлов имеют широкое практическое применение в различных областях. Одним из наиболее известных примеров таких реакций является получение солей металлов. Кислоты дают ионы водорода, которые замещают ионы металлов в оксидах, образуя соли металлов. Эти соли могут быть использованы в производстве различных материалов и продуктов, включая лекарства, удобрения и красители.
Реакции кислот с оксидами металлов также широко используются в металлургической промышленности. Оксиды металлов, взаимодействуя с кислотами, образуют соли, которые далее могут быть использованы в процессе плавки и получения металлических сплавов. Это позволяет улучшить качество и свойства полученных материалов.
С использованием реакций кислот с оксидами металлов связано и получение различных веществ в химической промышленности. Например, реакция кислоты с оксидом цинка позволяет получить водород, который может быть использован в различных технологических процессах. Также эта реакция может быть использована для очистки газов от примесей.
В дополнение к вышеперечисленному, реакции кислот с оксидами металлов имеют важное значение в области аналитической химии. Эти реакции могут быть использованы для определения наличия и концентрации определенных металлов в различных образцах. Таким образом, реакции кислот с оксидами металлов способствуют развитию методов анализа и контроля качества в различных отраслях промышленности и научных исследований.
Особенности реакций кислот с оксидами металлов при различных условиях
Реакции кислот с оксидами металлов имеют свои особенности и могут протекать по-разному в зависимости от условий, в которых происходит взаимодействие.
При нормальных условиях оксид металла обычно не реагирует с кислотой, так как его поверхность покрыта защитной пленкой оксида, которая не позволяет кислоте проникнуть к металлу. Однако, при нагревании или взаимодействии сильной кислоты, это препятствие может быть преодолено.
В случае реакции оксида металла с минеральной кислотой, например, соляной или серной, происходит образование соли и воды. При этом, оксид металла выступает в роли основания, принимая на себя протон от кислоты и образуя ион водорода. Эти реакции обычно сопровождаются выделением тепла.
При взаимодействии оксида металла с карбоновыми кислотами, такими как уксусная или молочная, образуется соль металла и углекислый газ. В этом случае, оксид металла действует как основание и принимает на себя протон от кислоты, образуя ион ацетата или лактата и освобождая углекислый газ.
Реакции кислот с оксидами металлов имеют большое применение в промышленности и лаборатории. Они позволяют получать соли металлов и другие соединения, а также применяются в синтезе органических и неорганических веществ.
Обзор литературы: что говорят ученые о взаимодействии кислот с оксидами металлов?
Вопрос о взаимодействии кислот с оксидами металлов является предметом изучения множества научных исследований. Ответ на него имеет большое значение для понимания реакционных способностей и химических свойств данных веществ.
В результате анализа литературы можно сделать вывод, что кислоты и оксиды металлов могут взаимодействовать между собой. При взаимодействии образуются соли и вода. Это связано с тем, что кислоты содержат ионы водорода, которые могут реагировать с оксидами металлов, образуя ионы металла и воду.
Известно, что реакция кислоты с оксидом металла происходит при наличии воды. Важную роль играет также концентрация кислоты и оксида металла, а также температура и время воздействия. Кроме того, способность кислоты реагировать с оксидом металла зависит от их химической природы и особенностей взаимодействия ионов водорода и ионов металла.
Однако, стоит отметить, что не все оксиды металлов реагируют с кислотами. Некоторые оксиды металлов обладают высокой устойчивостью и не реагируют с кислотами, даже в присутствии воды. Это связано с их структурой и химическими свойствами.
Таким образом, взаимодействие кислот с оксидами металлов представляет собой важную область исследований в химии. Дальнейшие работы и эксперименты помогут более подробно раскрыть механизмы реакций и выявить особенности взаимодействия различных кислот с оксидами металлов. Это позволит расширить наши знания о химических свойствах данных веществ и их применении в различных областях науки и промышленности.
Вопрос-ответ

Какие реакции происходят между кислотами и оксидами металлов?
Реакции между кислотами и оксидами металлов протекают с образованием солей и воды. Кислоты отдают протоны (водородные ионы) оксидам металлов, образуя соли. В результате образования солей выделяется вода.
Могут ли реагировать все кислоты с оксидами металлов?
Далеко не все кислоты могут реагировать с оксидами металлов. Реакция зависит от активности и свойств конкретной кислоты и оксида металла. Только кислоты с высокой активностью могут реагировать с оксидами металлов.
Можно ли использовать эту реакцию в химическом анализе?
Да, реакция кислот с оксидами металлов может быть использована в химическом анализе для определения наличия и концентрации металлов. Путем измерения количества образовавшейся соли или сопровождающих реакций можно установить тип и количество металла в образце.
